Введение
Гиперфосфатемия – независимый фактор риска общей смерти и смерти вследствие сердечно-сосудистых событий у больных, получающих заместительную почечную терапию [1, 2]. Ее влияние реализуется в условиях нормопаратиреоидемии, но с формированием гиперпаратиреоза только усиливается [3]. Применение диетических мероприятий служит обязательным пунктом фосфат-снижающей терапии, однако эффективность данного вида немедикаментозного лечения ограничена [4]. Старт диализной терапии решает проблему гиперфосфатемии лишь частично, сохраняя актуальность диетических мероприятий и отдавая пальму первенства по эффективности фосфат-связывающим препаратам [4]. В последних рекомендациях международного общества нефрологов рекомендуется сокращать применение Са-содержащих ФСП, расширяя возможности для применения при гиперфосфатемии не содержащих Са препаратов [5], к числу которых относится новый ФСП – комплекс оксигидроксида железа. Применение последнего за счет самой высокой среди существующих ФСП способности связывать фосфаты (260 мг P/1 г) позволяет добиваться целевых значений фосфатемии при сокращении лекарственной нагрузки с назначением 3–4 таблеток в сутки [6]. Это обстоятельство служит важным фактором повышения комплаентности лечения по сравнению с другими ФСП, эффективность которых обеспечивается применением 9–12 таблеток в сутки. К преимуществам применения препарата относятся также отсутствие влияния комплекса оксигидроксида железа на концентрацию большинства совместно применяемых препаратов, назначаемых перорально больным ХБП, а также на эффекты ряда препаратов (в частности, в отношении снижения концентрации изолированного паратиреоидного гормона при совместном назначении с пероральными агонистами рецепторов витамина D, антиатеросклеротической активности аторвастатина); неспособность его вызывать гиперкальциемию и повышать риск развития сосудистой кальцификации в отличие от Са-содержащих ФСП [7, 8]. Быстрорастущей популяцией больных на гемодиализе являются пациенты с диабетической нефропатией и иными болезнями почек, ассоциирующимися с сахарным диабетом, отличающиеся наличием высокой коморбидности и, соответственно, высокой лекарственной нагрузки. В связи с этим наш интерес распространился на категорию больных диабетической хронической болезнью почек (ХБП) 5-й стадии на старте гемодиализного лечения. Среди многочисленных публикаций, посвященных изучению антигиперфосфатемической активности комплекса оксигидроксида железа, мы не нашли данных для этой группы больных.
Цель. Оценить эффективность, безопасность и переносимость применения комплекса оксигидроксида железа при лечении гиперфсфатемии у больных диабетической ХБП 5Д-стадии.
Материал и методы. В исследование были включены 30 больных диабетической ХБП 5Д-стадии (из них 18 мужчин и 12 женщин, средний возраст обследованных составил 58,6±11,5 лет). Медиана продолжительности ХБП составила 13 лет [3; 28], ХБП 3А–5-й стадий – 3,8 года [1; 6,2], сахарного диабета 2 типа – 18 лет [6; 32,5]. Большинство больных получали инсулинотерапию (28 из 30 больных, в т.ч. в сочетании с линаглиптином – 17 из 28), линаглиптин в качестве самостоятельной терапии (2 из 30 больных). Все больные проходили инициацию гемодиализного лечения с последующим наблюдением в течение 2 месяцев. На додиализной стадии пациенты не получали никаких ФСП, проводилась только фосфат-снижающая диетотерапия. При этом у всех пациентов наблюдалась гиперфосфатемия по результатам трех исследований уровня фосфата крови с интервалом в одну неделю. С целью коррекции гиперфосфатемии был назначен комплекс оксигидроксида железа в начальной дозе 1 таблетка на 1 прием пищи (3 табл./день) с последующей коррекцией дозы через 1, 2, 4 и 8 недель.
Пациентам проведено физическое обследование: собирался анамнез заболевания. Из лабораторных методов обследования при подготовке данного исследования учитывались следующие показатели: определение сывороточного уровня фосфата на стадии до старта диализа, через неделю, две; один и два месяца после старта диализа. Паратгормон, кальций крови, показатели липидограммы, показатели гликемии определялись до старта диализа и через один и два месяца после. Оценивалась характеристика стула больного.
Статистический анализ полученных результатов проведен с помощью программ Microsoft Office Excel 2010 (Microsoft Corp., США). С целью оценки типа распределения показателей в группе применяли критерии Шапиро–Уилка. При значениях p>0,05 распределение считали не отличающимся от нормального. Описательная статистика включала следующие статистические показатели: Me [Q1;Q3] (Me – медиана, Q1 и Q3 – первый и третий квартили). При нормальном распределении выборки при сравнении двух независимых выборок использовали критерий Стьюдента, а при отличии от нормального – критерий χ2.
Результаты и обсуждение
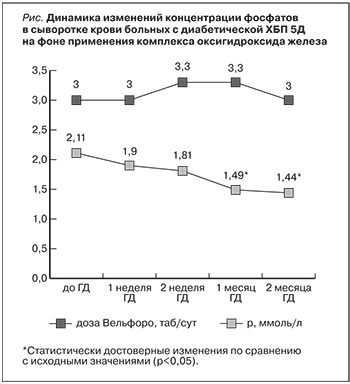 Среднее значение фосфата в крови у больных на додиализной стадии по результатам трех измерений составило в среднем 2,11 ммоль/л, что существенно превышало верхнюю границу нормы. Исходно количество таблеток комплекса оксигидроксида железа, назначаемых больным ежедневно, составило 3 в сутки (см. рисунок).
Среднее значение фосфата в крови у больных на додиализной стадии по результатам трех измерений составило в среднем 2,11 ммоль/л, что существенно превышало верхнюю границу нормы. Исходно количество таблеток комплекса оксигидроксида железа, назначаемых больным ежедневно, составило 3 в сутки (см. рисунок).
Постепенно по мере снижения уровня фосфата крови нами сохранялась прежняя доза препарата в отношении 28 больных (средняя доза – 3,3 табл./сут). Двум больным терапия осуществлялась в дозе 4 таблеток ввиду необходимости достижения целевых значений фосфата крови. К концу наблюдения количество таблеток комплекса оксигидроксида железа было снижено до 3 таблеток.
На фоне терапии наблюдалось снижение уровня фосфатов начиная с первой недели применения, целевой уровень фосфатов менее 1,49 ммоль/л был достигнут к концу первой недели у двух больных. К концу второй недели терапии целевой уровень был достигнут уже у 8 из 30 больных, к концу первого месяца – у 26 из 30 (87%), к концу второго месяца – у 29 из 30. У одного больного уровень фосфатов составил на конец наблюдения 1,51 ммоль/л, при этом исходно он имел уровень фосфатов крови 3,6 ммоль/л.
На фоне терапии комплексом оксигидроксида железа не происходило значимых изменений в уровне общего кальция крови (до лечения – 2,34±0,4, через месяц – 2,32±0,3, через 2 месяца – 2,30±0,4 ммоль/л). Паратиреоидный гормон имел тенденцию к снижению с 680±124 до 438±190 пг/мл, что было обусловлено параллельным применением антигиперпаратиреоидной терапии.
Анализ возможных неблагоприятных эффектов при назначении комплекса оксигидроксида железа показал, что диарея наблюдалась в 2 случаях из 30, что составило 6,7%, при этом стул был оформленным, жидковатым, четырежды за сутки у одного пациента и 3–6 раз в сутки у другого. У первого больного диарея продлилась в течение суток, у второго – в течение 3 суток, и это не потребовало отмены препарата. Среди других проявлений, описанных возможных нежелательных реакций со стороны желудочно-кишечного тракта, нами не наблюдалось запоров, рвоты, болей в животе, метеоризма, изменения цвета эмали зубов. У четырех больных отмечалась тошнота, но в двух случаях мы связывали ее возникновение с проявлениями хронической панкреатопатии, наблюдавшейся у пациентов в течение последних нескольких лет и прием препарата не прекращали. В двух случаях тошнота представлялась нам в качестве проявления уремической интоксикации и по мере проведения диализной терапии регрессировала полностью. Из других нежелательных явлений, ассоциирующихся с применением комплекса оксигидроксида железа, но не обязательно возникающих по причине его применения, следует отметить повышенную утомляемость, кожный зуд, сыпь, головную боль, одышку. Повышенная утомляемость сопутствовала почти всем нашим пациентам, она предшествовала назначению комплекса оксигидроксида железа и не увеличивалась после его назначения, более того, у 20 пациентов она заметно снизилась уже к концу второй недели диализной терапии, а у 6 пациентов исчезла полностью, у 4 – не изменилась. Кожный зуд как проявление уремической интоксикации присутствовал у трех больных и регрессировал к концу первого месяца диализной терапии полностью, таким образом, мы не связывали его наличие с приемом комплекса оксигидроксида железа. Сыпь и одышка не наблюдались у наших больных, головная боль отмечалась у трех пациентов еще до приема комплекса оксигидроксида железа и ее характер, частота и интенсивность не изменились на фоне приема препарата.
Поскольку ФСП способны вступать в межлекарственные взаимодействия с некоторыми лекарственными препаратами, нами был проанализирован спектр получаемых больными препаратов и оказалось, что среди них наиболее часто фигурирует аторвастатин.
Как известно, совместное применение комплекса оксигидроксида железа с аторвастатином не приводит к снижению эффективности последнего, несмотря на описанное в литературе межлекарственное взаимодействие in vitro. Это положение было подтверждено в нашем наблюдении: 14 из 30 больных получали аторвастатин в дозе 5 мг/сут и 10 – в дозе 10 мг/сут. Уровень общего холестерина крови на протяжении двух месяцев терапии повысился недостоверно – с 5,1±0,8 до 5,2±1,2 ммоль/л, при этом уровень холестерина липипротеидов низкой плотности снизился также недостоверно – с 4,3±1,6 до 4,1±1,1 ммоль/л. Произошло повышение уровня холестерина высокой плотности, обладающего антиатерогенными свойствами, с 0,8±0,9 до 1,1±0,4 ммоль/л, однако также недостоверное.
Важно отметить, что на терапии комплексом оксигидроксида железа не наблюдалось колебаний уровня гликемии, которые были бы обусловлены приемом препарата. Также не было отмечено необходимости в повышении дозы инсулина.
Заключение
Применение комплекса оксигидроксида железа у больных с гиперперфосфатемией при диабетической ХБП 5Д-стадии в диапазоне суточных доз 1,5–2,0 г (3–4 табл.) обеспечивает достижение целевых концентраций фосфатов в сыворотке крови у большинства пролеченных больных в течение двух месяцев наблюдения.
Комплекс оксигидроксида железа обладает хорошим профилем переносимости и безопасности. Среди описанных нежелательных эффектов при применении препарата нами наблюдалась только кратковременная диарея у двух больных.
Отмечено отсутствие влияния комплекса оксигидроксида железа на антигиперлипидемическую и антигипергликемическую активность при совместном применении с аторвастатином и противодиабетическими средствами.
Таким образом, применение комплекса оксигидроксида железа можно рассматривать в качестве выбора для стартовой терапии гиперфосфатемии больными диабетической ХБП-5Д.

