Введение
В настоящее время туберкулез мочеполовых органов (ТМПО) продолжает занимать лидирующее место среди внелегочных форм этого заболевания. Его доля в структуре вновь выявленных больных занимает от 23 до 70 % [1–6]. Специфическое поражение мочеполовых органов регистрируется у 26,5–38,3 % больных с генерализованными или полиорганными процессами [7–9, 4].
За последние два десятилетия в мире отмечен значительный рост заболеваемости ТМПО [10–13], частота его достигает 13 случаев на 100 тыс. населения. Но и этот показатель не достоверен, т.к. реальная заболеваемость ТМПО существенно превышает регистрируемую [14–16]. В европейских странах более половины случаев ТМПО прижизненно не диагностируется [17].
Изучение контингента больных туберкулезом показало, что специфическое поражение органов мочевой системы регистрируется у 26,5–38,3 % больных генерализованными или полиорганными процессами [18, 8, 9, 4].
Деструктивные формы ТМПО при впервые выявленном процессе составляют до 62,5 % [19, 15]. Соответственно, на начальных стадиях болезни эти пациенты выявлены не были, противотуберкулезного лечения не получали и по сути являлись резервуаром инфекции. Так, в слаборазвитых странах только у 15–20 % населения в моче обнаруживают МБТ [20].
Среди больных ТМПО 60–89,4 % составляют лица трудоспособного возраста [21]. Основное число (46,3 %) больных находится в возрасте наибольшей трудовой активности (41–60 лет). Поздняя диагностика и несвоевременное начало лечения ТМПО обусловливают высокий процент потери трудоспособности. Около 30 % больных запущенными формами ТСПО теряют ее уже в ходе первичного этапа лечения вследствие хронической почечной недостаточности, развивающейся у 33,0–66,6 % больных [22, 23, 15].
Анализ причин диагностических ошибок при ТМПО показывает, что чаще всего они возникают из-за отсутствия надежных диагностических критериев и характерных симптомов, отличающих туберкулезное поражение от неспецифических заболеваний почек [24–26]. Кроме того, важной причиной поздней диагностики ТМПО врачами общей лечебной сети служат недоучет анамнестических, клинических и параклинических данных, а также недостаточная настороженность врачей [27, 6].
На современном этапе диагностика ТМПО предусматривает использование клинических и лабораторных данных, а также проведение ряда инструментальных исследований. При этом есть два пути установления туберкулезной этиологии процесса: 1) исключение других очевидных заболеваний мочевыводящей системы; 2) выявление наиболее вероятных признаков, свойственных именно нефротуберкулезу.
Целью настоящего исследования было провести анализ структуры больных ТМПО и определить клиническую симптоматику заболевания на современном этапе.
Материал и методы. Материалом настоящего исследования послужило изучение клинического течения и результатов хирургического лечения 112 больных ТМПО и 74 – с неспецифическими заболеваниями мочевой системы, осложненными стриктурами мочеточников, оперированных в туберкулезном отделении для больных урогенитальным туберкулезом ФГБУ УНИИФ МЗ РФ, в туберкулезном отделении для больных урогенитальным туберкулезом ФГБУ СПбНИИФ МЗ РФ и в отделении урологии МБУ «Городская клиническая больница № 14» Екатеринбурга с 1986 по 2011 г. Критерием включения в исследование служило наличие специфического поражения мочевых органов и/или стриктуры мочеточника на разных стадиях ее развития (n = 186).
Среди всех больных с такими поражениями было 72 (38,7 %) мужчины и 114 (61,3 %) женщин. Возрастной диапазон колебался от 18 до 77 лет и в среднем составил 51,8 ± 0,8 в группе больных ТМПО и 48,2 ± 3,0 – с неспецифическими стриктурами мочеточника.
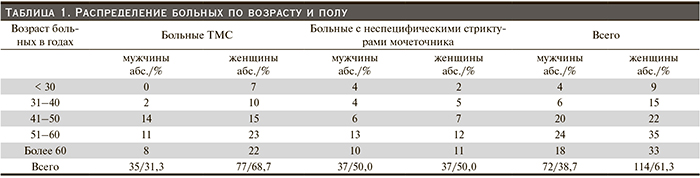
Распределение больных по возрасту и полу приведено в табл. 1.
 Среди обследованных пациентов представлены все возрастные группы. Как следует из таблицы, большинство больных были в трудоспособном возрасте до 60 лет – 135 (72,6 %) человек. Следует отметить, что мужчин трудоспособного возраста было в полтора раза меньше, чем женщин: 54 (29,0 %) против 81 (44,0 %). Каждый четвертый (27,4 %) пациент был пожилого и старческого возраста.
Среди обследованных пациентов представлены все возрастные группы. Как следует из таблицы, большинство больных были в трудоспособном возрасте до 60 лет – 135 (72,6 %) человек. Следует отметить, что мужчин трудоспособного возраста было в полтора раза меньше, чем женщин: 54 (29,0 %) против 81 (44,0 %). Каждый четвертый (27,4 %) пациент был пожилого и старческого возраста.
В зависимости от этиологии заболевания и наличия обструкции мочеточников все пациенты разделены на три группы.
В первую вошли 48 (25,8 %) больных нефротуберкулезом без распространения на мочеточник в возрасте от 27 до 72 лет, который в среднем составил 51,7 ± 2,2 года. Преобладали женщины: 40 против 8 мужчин.
Вторая группа состояла из 64 (34,4 %) пациентов (37 женщин и 27 мужчин), страдавших туберкулезом почек с вовлечением мочеточника. Диагностический интервал у больных этой группы от появления первых клинических признаков до выявления ТМПО колебался от 6 месяцев до 15 лет, в среднем 3,3 + 0,6 года. Диагноз верифицирован гистологическими у 42 (65,6 %), бактериологическими – у 17 (26,6 %) и у 5 (7,8 %) пациентов – клинико-рентгенологическими исследованиями.
Третью группу составили 74 (39,8 %) больных (37 женщин и 37 мужчин) со стриктурами мочеточников неспецифического происхождения в возрасте от 18 до 80 (48,5 ± 1,7) лет.
Для анализа состояния почек и мочеточников использовано понятие почечно-мочеточниковой единицы (ПМЕ) – renal unit, соответствующей одной функционирующей почке и одному мочеточнику. Структура ТМПО представлена в табл. 2.
Как видно из табл. 2, на 112 пациентов приходилось 209 локализаций ТМПО. Почти в трети случаев заболевание носило билатеральный характер и распространялось на мочеточники и мочевой пузырь. Частота туберкулезного уретерита составила 57,1 % от числа больных со специфическим поражением почек и 30,6 % – от всех локализаций ТМПО. В структуре этих поражений преобладал туберкулезный папиллит – в 24,4 % случаев, несколько реже встречался кавернозный и поликавернозный туберкулез почек – в 20,1 и 12,9 % случаев соответственно. Каждый случай ТМПО подтвержден гистологическим исследованием операционного материала и/или бактериологически.
Из 112 больных ТМПО 53 (47,3 %) пациента имели очаги специфического процесса других локализаций, причем у 5 (4,5 %) – зарегистрировано одновременно 2 из них, у 3 (2,7 %) – 3 и у 2 (1,8 %) – 4. Всего отмечено 70 случаев экстраренального туберкулеза (табл. 3).
Как видно из табл. 3, преобладали пациенты с туберкулезом органов дыхания и гениталий. В целом активность процесса наблюдали у каждого третьего из оперированных.
Структура туберкулеза органов дыхания представлена в табл. 4.
Табл. 4 наглядно показывает, что наиболее часто регистрировали инфильтративный туберкулез легких (42,3 %), втрое реже наблюдали туберкулез внутригрудных лимфатических узлов и еще реже – другие его формы.
Большинство наблюдаемых больных оперированы при наличии сопутствующих, часто сочетанных заболеваний. Сведения о них представлены в табл. 5.
Табл. 5 демонстрирует, что доминировали болезни сердечно-сосудистой системы. Нередким интеркуррентным заболеванием был хронический пиелонефрит, который встречался у половины больных.
Наличие серьезных сопутствующих заболеваний, объем и тяжесть оперативных вмешательств требовали соответствующего ведения послеоперационного периода, а некоторым больным приходилось ограничиваться только пособиями по отведению мочи из-за высокой степени операционного и анестезиологического риска.
У 58 (51,2 %) больных специфическое поражение почек, нарушение уродинамики ВМП и наличие сопутствующего пиелонефрита приводили к развитию хронической почечной недостаточности (ХПН). ХПН классифицирована по 4 стадиям (Лопаткин Н.А., 1978): латентная (I), компенсированная (II), интермиттирующая (III) и терминальная (IV). Критерии установления той или иной стадии ХПН: уровень креатинина крови, показатели клубочковой фильтрации и клинические проявления.

Данные распределения больных по стадиям ХПН до оперативного лечения отражены в табл. 6.
Как можно отметить по данным табл. 6, более четверти пациентов имели ХПН в латентной стадии, почти каждый пятый – в компенсированной, 4,5 % – в интермиттирующей и только у 1,8 % отмечена терминальная стадия нарушения функции почек.
Методы обследования больных
Наблюдаемые больные подвергнуты клиническим, лабораторным, радионуклидным, рентгенологическим, ультразвуковым, инструментальным и эндоскопическим методам исследования.
Клинические данные включали изучение жалоб, анамнеза заболевания и объективного обследования.
Больным один раз в 3–5 дней (по показаниям и чаще) выполняли клинические анализы крови и мочи, подсчет форменных элементов мочи в 1 мл по методу Де-Альмейда – А.З. Нечипоренко.
Осуществляли бактериоскопическое исследование мокроты, мочи и их посев на плотные питательные среды Левенштейна–Йенсена и Новая – для выявления микобактерий туберкулеза с определением чувствительности штаммов МБТ к специфическим препаратам.
Бактериологическое исследование мочи на неспецифическую микрофлору неоднократно выполнено всем больным. Забор материала проведен до начала антибактериальной терапии, а также на протяжении курса лечения. Посев мочи осуществлен на питательные среды: питательный агар, 5 %-ный кровяной агар и сахарный бульон. Определена и чувствительность к антибактериальным препаратам. Достоверной степенью бактериурии считалась 104 и выше. При трактовке исследования учитывалось, что при нарушении оттока мочи и ее низком удельном весе может наблюдаться низкая степень бактериурии, поэтому важен вид выделенного микроорганизма. Выделение ассоциаций микроорганизмов также коррелирует с низкой степенью бактериурии.
У 55 (29,6 %) пациентов выделена патогенная неспецифическая микрофлора в моче. По данным литературы, наиболее частыми возбудителями неспецифической мочевой инфекции при туберкулезе мочевой системы являются кишечная палочка, протей и стафилококк. Соотношение видов микроорганизмов по полученным результатам представлено в табл. 7.
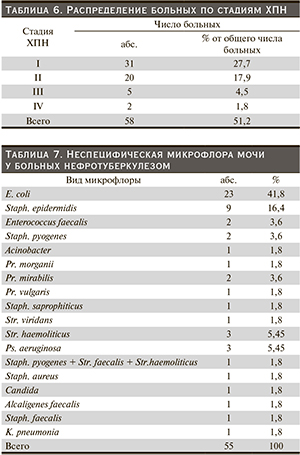 Из табл. 7 следует, что у наблюдаемых больных в моче преобладала E. сoli, Staph. epidermidis, а также протейная флора.
Из табл. 7 следует, что у наблюдаемых больных в моче преобладала E. сoli, Staph. epidermidis, а также протейная флора.
Изучение функционального состояния почек произведено на основании комплекса исследований, включившего определение концентрационной способности почек по пробе С.С. Зимницкого, величины клубочковой фильтрации и канальцевой реабсорбции воды по пробе Реберга–Тареева, уровня креатинина (метод Поппера) и мочевины (метод с диацетилмонооксидом) сыворотки крови.
Рентгенологические исследования, включившие обзорную и экскреторную урографию с нисходящей цистографией, обзорную рентгенографию легких и ультразвуковое исследование почек, выполнены всем больным.
Для оценки нарушений почечной функции пользовались классификацией ХПН, предложенной академиком Н.А. Лопаткиным и профессором И.Н. Кучинским (1978), которую приводим ниже.
В I стадии (начальная, латентная) отсутствуют клинические симптомы. Характерна нормальная концентрационная функция почек, значительное снижение клубочковой фильтрации (50 % от нижней нормы). Незначительное увеличение креатинина в крови 1,6 мг% (норма – 1,2). Снижен синтез аммиака и его выделение. Осмолярность мочи снижена до 400–500 мосм/л. Ренограмма изменена незначительно.
II стадия – компенсированная, полиурическая. Характеризуется появлением жалоб: утром слабость, жажда, снижение температуры. Клубочковая фильтрация снижена до 30–40 мл/мин, осмолярность – до 400 мосм/л. Выраженная полиурия, полидипсия, никтурия. Азотемии нет, мочевина на верхней границе нормы. Креатинин крови увеличивается до 2,7 мг% (0,35 ммоль/л), компенсация за счет функции печени и других органов. Ренограмма пологая. Гипертензия и анемия или отсутствуют, или слабо выражены. Кислотно-основное состояние практически не изменено, щелочной резерв крови снижен до 19,5 (в норме 21,5).
III стадия (интермиттирующая) характеризуется декомпенсацией основной почечной функции, моча изотонична, увеличено ее количество (при уменьшении до нормы или менее нормы – неблагоприятный признак). Остаточный азот, мочевина увеличены в 2 раза, резко снижена клубочковая фильтрация (до 20–30 мл/мин), резко нарушены секреция ионов водорода и образование аммиака, рН мочи – щелочная. Уровень креатинина крови повышен до 4,5 мг% (0,44 моль/л), щелочной резерв снижен до 14 мэкв/л, метаболический ацидоз выражен, кальций и калий снижены. Концентрация ионов магния увеличена в 2 раза по сравнению с нормой (норма – 1,7–2,0 мэкв/л). Мышечная слабость, изменения сухожильных рефлексов, мышечные подергивания, тетанические судороги вследствие уменьшения кальция и фосфора. Анемия резко выражена, артериальная гипертензия, кожные покровы сухие, землистые, может быть геморрагический синдром, тошнота, рвота, анорексия, отвращение к животным белкам, стул неустойчивый, запоры, понос, вздутие живота, икота. Легко присоединяется вторичная инфекция.
Для IV стадии (терминальной) характерны гибель всех нефронов, резкое нарушение клубочковой фильтрации до 5–10 мл/мин, реабсорбции, уремический синдром. Больные апатичны, вялы, резко нарушен сон. Сонливость днем, ночью не спят, негативны, возможны психические реакции (Брайтово безумие), резкий зуд кожи, подергивания мышц. Прогрессируют симптомы гастроэнтероколита, уремический псевдоперитонит, может быть гипотермия даже при присоединении инфекции. Анемия прогрессирует, сывороточное железо низкое, уменьшение коагуляционной способности крови, удлинение времени кровотечения, резкий лейкоцитоз (до 60–80,000), нейтрофилез со сдвигом влево, тромбоцитопения, снижение протромбинового индекса, фибриногена, типичны носовые кровотечения. По данным ЭКГ – дистрофия миокарда. Рентгенография – округлые тени в легких, сетчатость (уремические пневмониты). Задержка жидкости. Изостенурия – 1002–1005. Увеличение креатинина – более 0,6 ммоль/л, мочевины, остаточного азота, калия, натрий снижен. Щелочной резерв резко снижен до 12 мэкв/л.
При оценке нарушений уродинамики использовали классификацию А.С. Переверзева, В.С. Карпенко (1987), которые выделили пять стадий развития гидроуретеронефроза (ГУН) в результате нарушения проходимости тазового отдела мочеточника, положив в основу классификации изменения тонуса и перистальтики чашечно-лоханочно-мочеточниковой системы и влияние их на функцию почки.
Первая стадия характеризуется снижением тонуса мышц тазовой части мочеточника без нарушения функции почки. Почка хорошо и своевременно выделяет контрастное вещество. Отчетливо прослеживаются чашки, лоханка и мочеточник на всем протяжении. Расширение выявляется только в тазовой части мочеточника протяженностью не более 10–12 см над участком сужения. При рентгеноскопии и рентгенокинематографии отчетливо видно чередование систол и диастол лоханки; перистальтика мочеточника активная – 6–8 раз в минуту, контрастированная моча перемещается до места сужения. Максимальное расширение просвета тазовой части мочеточника над препятствием наблюдалось в момент сокращения средней трети мочеточника.
Вторая стадия – снижение тонуса и перистальтики мочеточника осложняется нарушением выделительной функции почки. Почка выделяет контрастное вещество с некоторым опозданием. Отчетливое изображение лоханки и мочеточника наступает через 25–30 минут от начала исследования. Сокращения лоханки и мочеточника еще несколько учащены (5–6 раз в минуту). Перистальтические волны глубокие. Верхняя половина мочеточника во время сокращения освобождается от контрастированной мочи, и стенки его смыкаются. В нижней половине мочеточник расширен и заполнен остаточной мочой. Периодически наблюдается забрасывание контрастированной мочи через суженный участок мочеточника в мочевой пузырь. Временами отчетливо видны антиперистальтика и рефлюкс мочи в верхние отделы мочеточника.
Третья стадия – выраженное снижение тонуса и перистальтики чашечно-лоханочно-мочеточниковой системы, а также снижение секреторной и выделительной функций. Несмотря на значительное снижение выделительной функции почки, контрастирование верхних мочевых путей хорошее благодаря окклюзии тазовой части мочеточника. При рентгенотелескопии через 60–90 минут после внутривенного введения контрастного вещества наблюдается отчетливое изображение лоханки и мочеточника. Над препятствием отмечается расширение всего мочеточника, лоханки и чашек. Наблюдаются перегибы мочеточника. Сократительная деятельность мочеточника и лоханки вялая, перистальтические волны иногда едва заметны (3–4 раза в минуту). Контрастированная моча поступает в мочевой пузырь не после каждой систолы. Катетеризация сопровождается появлением глубокой частой перистальтики и смыканием стенок мочеточника на всем протяжении.
Четвертая стадия – дальнейшее снижение тонуса и моторно-эвакуаторной функции верхних мочевых путей, которое осложняется повышением интралюминального давления и резким нарушением функции почки. В этой стадии во время экскреторной и инфузионной урографии даже в течение 1–2-часового наблюдения хорошего контрастирования мочевых путей не отмечено. Исследование уродинамики ВМП проведено путем ретроградной и антеградной пиелоуретерографии. После освобождения лоханки и мочеточника от мочи удается отметить сужение их просветов, появление перистальтики и чередование систол и диастол до 4–5 раз в минуту.
Пятая (терминальная) стадия – снижение тонуса верхних мочевых путей привело к необратимым нарушениям секреторной, выделительной и резорбционной функций почки. При внутривенном введении контрастного вещества заполнения чашечно-лоханочной системы не происходит в течение 4–6 часов. Путем антеградного введения контрастного вещества выявляется значительное расширение полостей почки и мочеточника без признаков моторно-эвакуаторной функции. Перистальтика не появляется и после снижения внутрипочечного давления, которое у этих больных уменьшается до 0,44 кПа, что также свидетельствует о глубоких изменениях в почечной паренхиме.
Определение функции ВМП и почек больных произведено по трехбалльной системе [28]: хороший, удовлетворительный и неудовлетворительный. Хорошим считали результат лечения, когда через 6–12 месяцев после выполнения реконструктивно-восстановительной операции пациент чувствовал себя здоровым, жалоб не предъявлял, анализы мочи за все время диспансерного наблюдения были нормальными. Рентгенологический контроль установил полную проходимость мочеточников, значительное сокращение расширенных полостей почки и мочеточника, хорошее состояние паренхимы почки по данным ультразвукового исследования. При этом определено значительное улучшение или нормализация функции мочевыводящих путей и почек, основанные на данных экскреторной урографии, радионуклидных методах исследования и клиренс-тестах. Удовлетворительным расценен результат лечения, когда через 6–12 месяцев после выполнения реконструктивно-восстановительной операции у пациента отсутствовали жалобы, улучшалась функция ВМП и почек, но при этом определялась умеренная лейкоцитурия без обострений сопутствующего пиелонефрита, отсутствовали или незначительно сокращались полости почки и мочеточника, а также при наличии таких осложнений, которые не вызывали нарастания суправезикальной обструкции мочеточника и устранение которых привело к полному выздоровлению больного. Результат считали неудовлетворительным, когда после выполнения операции функция почки не восстанавливалась, происходило прогрессирование ГУН и ХПН и приходилось выполнять повторные операции по коррекции стриктуры мочеточника, реконструктивно-восстановительные вмешательства или производилась нефрэктомия.



