Введение
Распространенность болезней системы кровообращения (БСК), как и смертность от них, остается высоким на протяжении последних десятилетий и имеет отчетливую тенденцию к росту. Существенный вклад в смертность от БСК вносит ведущий модифицируемый фактор риска атеросклероза – дислипидемия, способствующая его прогрессированию. Известно, что пациенты с острым коронарным синдромом (ОКС) имеют высокий риск сердечной смерти и развития кардиоваскулярных осложнений, острый инфаркт миокарда остается основной причиной смерти от БСК [1].
Вместе с тем в работе B. Zheng и соавт. продемонстрировано существенное повышение риска развития сердечно-сосудистых событий у пациентов, перенесших острый инфаркт миокарда (ОИМ), с атеросклеротическим стенозом почечных артерий (ПА). Отмечено, что стеноз ПА более 70% является важным неблагоприятным предиктором комбинированных конечных точек, включая смерть, нефатальный инфаркт миокарда, ишемический инсульт и внутричерепное кровотечение [2]. В другом ретроспективном исследовании A. Burlacu (et al., 2015) у пациентов с ОИМ, подвергшихся первичному ЧКВ, стеноз ПА (более 50%) встречался у 16,6% респондентов. В этой группе больных чаще наблюдались метаболические нарушения, расстройства водного обмена и задержка жидкости, эндотелиальная дисфункция, что было ассоциировано с массой крупных сердечно-сосудистых катастроф [3].
С учетом имеющихся научных фактов учеными из Пекинского университета Ma Q. была разработана специальная шкала прогнозирования развития стеноза ПА у пациентов с ИБС [4].
Вместе с тем в Европейских рекомендациях по заболеваниям периферических артерий (2017) отмечается, что реваскуляризация ПА значимо не влияет на уровень артериального давления, а также почечные и сердечно-сосудистые исходы [5].
Однако не вызывает сомнений, что своевременная диагностика ишемической нефропатии может предопределять успех лечения таких пациентов, позволяя не только замедлить скорость прогрессирвоания ХБП, но и уменьшить количество осложненных форм ИБС [6].
Несмотря на имеющиеся работы по проблеме мультифокального атеросклеротического поражения сосудов, убедительных данных по влиянию атеросклероза ПА на сердечно-сосудистые исходы при ОКС недостаточно ввиду небольших выборок исследуемых групп, а подобных исследований в нашей стране практически не проводилось.
Целью данного исследования стало изучение влияния стеноза ПА на риск развития сосудистых событий у пациентов с ОКС.
Материал и методы
В исследование включены 323 пациента с ОКС, находившихся на лечении в кардиологическом отделении регионального сосудистого центра ГБУ РО РОКБ, из них 217 (67,1%) мужчин, 106 (32,9%) женщин. Средний возраст обследованных больных составил 59,6±9,2 года.
Всем пациентам были проведены стандартные биохимические исследования, включившие оценку показателей липидного обмена: общий холестерин (ХС); ХС липопротеидов высокой и низкой плотности – ЛПВП и ЛПНП; индекс атерогенности – ИА; триглицериды (ТГ), уровни креатинина, мочевины. СКФ рассчитывали по формулам Кокрофта–Голта и CKD-EPI [6]. Комплекс инструментальных исследований включил регистрацию ЭКГ в покое, холтеровское мониторирование ЭКГ, ультразвуковое исследование сердца, ультразвуковое исследование почек, коронароангиографию (КАГ) для оценки степени поражения коронарных сосудов, селективную ангиографию почечных сосудов.
Статистический анализ полученных результатов проведен с помощью набора прикладных статистических программ Microsoft Office Excel 2010 (Microsoft Corp., США) и STATISTICA 10.0 (StatSoft Inc., США). С целью оценки типа распределения данных применяли анализ Колмогорова–Смирнова, при значениях p>0,05 распределение считали не отличающимся от нормального.
Описательная статистика проведена с определением следующих особенностей: данные представлены в виде M±SD (M – среднее арифметическое, SD – стандартное отклонение) при нормальном распределении и в виде Me [Q1;Q3] (Me – медиана, Q1 и Q3 – первый и третий квартили) при ненормальном распределении. При нормальном распределении выборки при сравнении двух независимых выборок использовали критерий Стьюдента, при отличии от нормального – критерии Манна–Уитни и χ2 или тест Левена с определением F. Также применялся логистический регрессионный анализ с расчетом относительных рисков (OR) и определением χ2, связь считалась статистически значимой при значении р<0,05.
ROC-анализ с построением операционных характеристических кривых и расчетом коэффициента площади кривой (AUC) применялся для оценки прогностической информативности используемых методов.
Результаты
Согласно полученным результатам селективной ангиографии ПА, у 24,8% больных ОКС выявлено атеросклеротическое поражение ПА, при этом односторонний стеноз наблюдался у 58,8% пациентов, двусторонний – у 41,2%. У больных с односторонним атеросклеротическим поражением стеноз левой ПА встречался в 57,5% случаев, правой ПА – в 42, 5%. При одностороннем поражении ПА средний процент стеноза составил 56,1%, тогда как при двустороннем поражении стеноз был более выраженным – 76,7% (р<0,05).
При проведении двухфакторного логистического регрессионного анализа в качестве одного фактора был выбран стеноз ПА или двусторонний стеноз ПА, в качестве другого – те признаки, которые ранее продемонстрировали свое влияние на риск развития сосудистых событий. Атеросклеротическое поражение ПА вместе с величиной ФВ или размером ЛП, ПЖ, а также толщиной МЖП влияли на риск развития нефатальных сосудистых событий (χ2=7,46, р=0,024; χ2=7,37, р=0,025; χ2=11,1, р=0,004; χ2=9,52 р=0,009 соответственно) (табл. 1). Также обсуждаемый риск повышался в случае прироста СКФ после проведенной КАГ, χ2=9,83, р=0,007.
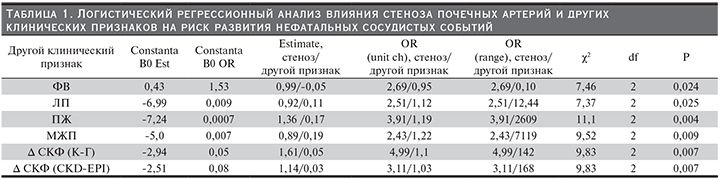
Полученные уравнения логистического регресса позволили разработать прогнозные таблицы, одна из которых в качестве примера представлена в табл. 2.
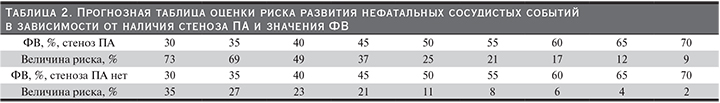
Так, например, при наличии стеноза ПА и ФВ 60%-ный риск развития нефатальных сосудистых событий составил 17%, при ФВ 45%-ный указанный риск был равен 21%, в то время как у больных без поражения ПА – 6 и 21% соответственно. Согласно данным ЭхоКГ, было установлено, что при значении ЛП 38 мм у обследованных пациентов с наличием стеноза ПА обсуждаемый риск был равен 11%, при 54 мм – 44%, при этом у больных без атеросклеротического поражения ПА эти показатели составили 3 и 19% соответственно.
При включении в таблицу риска таких факторов, как стеноз ПА и размеры ПЖ, вероятность развития нефатальных сосудистых событий может достигать 84%, в то время как у больных без поражения ПА – 63%. При анализе сердечно-сосудистого риска у пациентов с атеросклеротическим поражением ПА и МЖП 10-мм риск равен 4%, у больных же без поражения – 2%, при МЖП 22-мм – 38 и 18%.
В ходе исследования установлено, что среди больных с наличием атеросклеротического поражения ПА и Δ СКФ (CКD-EPI)-40 риск развития нефатальных сосудистых событий составил 38%, у больных же без поражения ПА – 10%, при Δ СКФ (CКD-EPI)-60 риск равен 57 и 14% (табл. 3).
Двусторонний стеноз ПА, а также ряд признаков, в частности размер ЛП, МЖП, значения ОХС крови, повышали риск развития фатальных сосудистых событий (табл. 4).
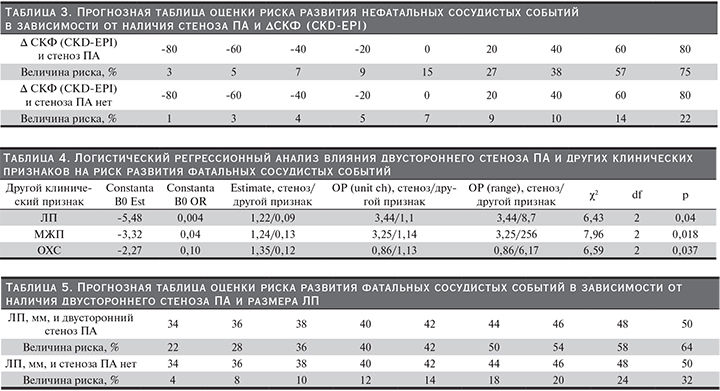
Так, риск развития фатальных сосудистых событий у пациентов с двусторонним стенозом ПА и размером ЛП 36 мм был равен 28%, у больных без стеноза ПА – 8% (табл. 5).
У лиц с двусторонним поражением ПА и МЖП 18-мм вероятность развития фатальных сосудистых событий составила 47%, в то время как у пациентов без атеросклеротического поражения ПА данный риск был равен 18%. Помимо этого было установлено, что величина риска развития фатальных сосудистых событий у больных двусторонним поражением ПА и значением ОХС 10 ммоль/л равна 54%, у пациентов без стеноза ПА сердечно-сосудистый риск был существенно ниже и составил 16%.
Двустороннее поражение ПА влияло на риск развития фатальных и нефатальных сосудистых исходов, однако факторы, оказывающие влияние на эту точку, несколько отличались от таковых, влияющих только на фатальные сосудистые события. В ходе двуфакторного логистического анализа было установлено, что такие факторы, как стадии ХБП (р=0,034, χ2=6,78), уровень СКФ до КАГ (р=0,0001, χ2=18,3), а также выраженность стеноза проксимального и дистального участков ПМЖВ (р=0,005, χ2=10,6)(р=0,027, χ2=7,2), оказывали влияние на риск развития сердечно-сосудистых событий (табл. 6).
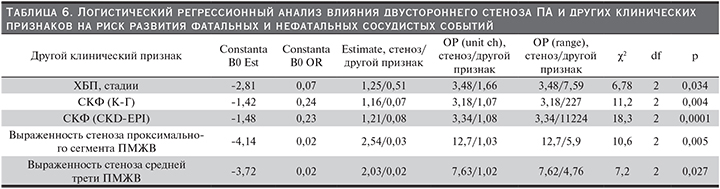
В ходе работы установлено, что больные с двусторонним поражением ПА и ХБП 3-й стадии имели риск развития фатальных и нефатальных сосудистых событий 45%, у пациентов без стеноза ПА он был существенно ниже и составил 18%.
При использовании в качестве прогностического критерия наличие стеноза в проксимальном участке ПМЖВ установлено, что у больных с двусторонним поражением ПА и при гемодинамически значимом стенозе проксимальной трети ПМЖВ обсуждаемый выше риск был равен 63%, у пациентов же без поражения ПА данный риск оказался существенно ниже и составил 8%. У лиц со стенозом средней трети ПМЖВ и двусторонним поражением ПА риск развития фатальных и нефатальных сосудистых событий достигал 78%, у больных без стеноза ПА – 17%.
Используемые инструменты прогнозирования, несмотря на свою статистическую значимость, требуют оценки их информативности. Для этого нами был использован ROC-анализ, в ходе которого отдельно анализировали информативность инструментов прогнозирования по трем конечным точкам: нефатальные сосудистые события, фатальные сосудистые события и фатальные/нефатальные сосудистые события. В отношении первой конечной точки комбинация признаков: наличие стеноза ПА, величина ФВ, размеры ЛП, ПЖ, толщина МЖП, Δ СКФ (CКD-EPI), позволила повысить AUC до 0,78, увеличив чувствительность методики до 75%, при этом сохранив специфичность на уровне 70%.
В ходе ROC-анализа влияния факторов на фатальные сосудистые события была продемонстрирована более высокая информативность, чем в ходе предыдущего анализа. В частности, комбинация факторов: наличие двустороннего стеноза ПА, размер ЛП, толщина МЖП, значение ОХС, позволила повысить AUC до 0,93, чувствительность метода до 82%, а специфичность – до 95%.
Комбинированная точка: наличие двустороннего стеноза ПА, стадии ХБП, выраженность стеноза проксимальной и средней ПМЖВ, показала AUC, равную 0,92, при этом чувствительность метода была равной 90%, специфичность – 90%.
Обсуждение
По данным различных популяционных регистров и исследований, распространенность почечной патологии составляет 10–13%, достигая в группах высокого риска –20%. При этом рост числа больных с почечной патологией в последние годы происходит за счет их вторичного поражения, прежде всего на фоне СД и АГ [7].
Согласно проведенному исследованию, частота распространенности атеросклеротического поражения ПА у пациентов с ОКС составила 24,8%.
Наличие атеросклеротического поражения ПА и как следствие – снижение СКФ являются независимым фактором риска развития ССЗ и рассматривается в качестве маркера неблагоприятного прогноза сердечно-сосудистых событий [6]. Так, в ходе работы было установлено, что среди больных со стенозом ПА и Δ СКФ-40 риск развития нефатальных сосудистых событий составляет 58% при Δ СКФ-60, риск существенно выше и равен 75%. На сегодняшний день установлено, что риск сердечно-сосудистых осложнений резко возрастает по сравнению с общепопуляционным уровнем уже на стадии умеренного снижения функции почек [7]. В ходе исследования установлено, что пациенты с двусторонним поражением ПА и ХБП 3-й стадии имели риск развития фатальных и нефатальных сосудистых событий 45%, при наличии ХБП 5-й стадии риск составил 67%.
Наиболее эффективным инструментом прогнозирования сердечно-сосудистого риска является комплексный подход к выявлению всех существовавших ФР у каждого больного ОКС, опираясь не только на выявление традиционных ФР и маркеров почечной дисфункции, усугубляющих течение основного заболевания, но и индивидуальную оценку особенностей поражения коронарного кровотока [6, 7]. Атеросклероз ПМЖВ ЛКА в проксимальной трети ассоциируется с большим риском смерти по сравнения с атеросклеротическим процессом в ПКА или в дистальной трети ПМЖВ ЛКА [8]. Так, нами был отмечен тот факт, что у больных с двусторонним поражением ПА и гемодинамически значимым стенозом проксимальной трети ПМЖВ риск развития фатальных и нефатальных сосудистых событий составил 63%.
Выводы
Атеросклеротическое поражение ПА у больных ОКС обнаружено в 24,8% случаев.
Установлено влияние атеросклеротического стеноза ПА у пациентов исследуемой группы на риск развития сердечно-сосудистых событий.
Предложенная в ходе исследования модель прогнозирования является самостоятельным инструментом оценки риска развития фатальных и нефатальных сосудистых событий в данной группе пациентов. Данная модель риска может широко использоваться в комплексном обследовании больных ОКС и с атеросклеротическим поражением ПА.

