В настоящее время трансплантация почки позволяет полностью излечить больного от хронической болезни почек (ХБП) в терминальной стадии почечной недостаточности (ХБП-V). Число больных в данной стадии почечной недостаточности с каждым годом увеличивается. Однако число донорских почек, пригодных для трансплантации, остается на прежнем уровне [1]. Соотношение больных ХБП-V к изъятым донорским почкам составляет 4:1 в год, в связи с чем во всем мире предпринимаются попытки расширить показания к изъятию донорских органов, чтобы уменьшить период ожидания, физических и психологических осложнений больных, получающих заместительную почечную терапию [2, 3].
Аномалии развития изъятых донорских почек, такие как полное удвоение почки и как следствие – наличие двух мочеточников в одной почке, встречаются в 1% случаев [4]. Данная патология состоит в том, что один мочеточник начинает собирать мочу из верхнего отдела почки, второй – из нижнего, и каждый из них исходит из собственной лоханки. Одновременно один проток развивается обычным, другой – неестественным образом. Удвоение мочеточника может быть полным либо неполным и часто бывает односторонним. У большинства пациентов данную патологию обнаруживают случайно при профилактических осмотрах, никакими клиническими симптомами это не подкрепляется и не нуждается в хирургическом вмешательстве. Таким образом, при изъятии органов можно обнаружить донорскую патологию – удвоение почки и как следствие – наличие двух мочеточников, исходящих из одной почки.
Поскольку при трансплантации таких почек возможно увеличение числа осложнений со стороны донорских мочеточников, многие трансплантологи считают такие скомпрометированные почки относительным противопоказанием к трансплантации [5, 6].
Приводим описание двух случаев успешной трансплантации почек с двумя мочеточниками больных, находящихся на лечении заместительной почечной терапией.
Клинический случай 1
 Больная И. 32 лет поступила в ноябре 2017 г. в отделение трансплантации почки для экстренной операции трансплантации трупной почки по поводу хронического диффузного гломерулонефрита, терминальной стадии ХБП. Группа крови больной – 0(I) Rh-pos.
Больная И. 32 лет поступила в ноябре 2017 г. в отделение трансплантации почки для экстренной операции трансплантации трупной почки по поводу хронического диффузного гломерулонефрита, терминальной стадии ХБП. Группа крови больной – 0(I) Rh-pos.
Больна с 2014 г., когда после родов диагностирован хронический гломерулонефрит. В анамнезе аднексэктомия справа по поводу разрыва кисты правого яичника, вылущивание кисты левого яичника. До 2014 г. длительное время страдала артериальной гипертензией с артериальным давлением до 190/95 мм рт.ст. Консервативная терапия без эффекта. В связи со стойким снижением скорости клубочковой фильтрации (СКФ) до 8 мл/мин, повышением уровней креатинина крови до 580,6 мкмоль/л, мочевины крови до 28,3 ммоль/л больной была сформирована дистальная артериовенозная фистула на предплечье и с октября 2015 г. начато лечение программным гемодиализом. Больная обследована на системное заболевание, которое не подтвердилось.
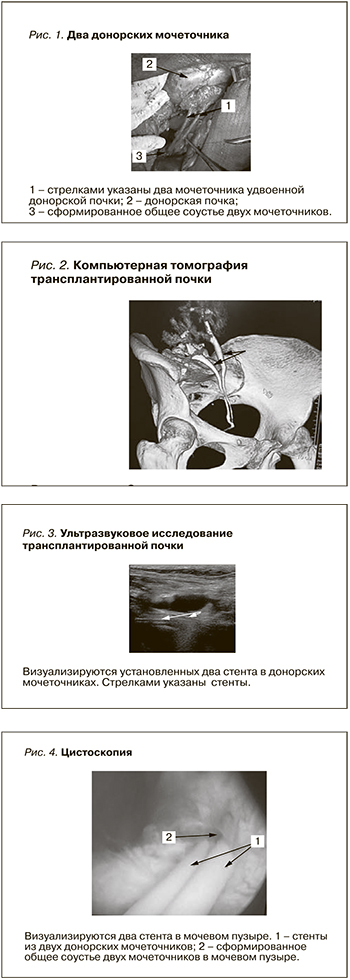
В ноябре 2017 г. выполнена трансплантация правой трупной почки. Совпадение по групповой принадлежности полное, по системе HLA – по трем лейкоцитарным антигенам: A2, DR 4, DR 7. Уровень антител – 0%. Донор – женщина 43 лет, причина смерти: черепно-мозговая травма, несовместимая с жизнью. Мультиорганное изъятие после констатации мозговой смерти. Время холодовой ишемии составило 12 часов. Почка увеличена в размере 12,1×8,3×5,5 см. Во время обработки донорской почки обнаружено два мочеточника, отдельно отстоящих друг от друга (рис. 1). Выделены и обработаны одна артерия, имеющая раннее деление, и одна вена трансплантата. Операция выполнена без технических осложнений. Оба мочеточника сшиты между собой в дистальных отделах по типу «двустволки» и имплантированы одним соустьем в переднебоковую стенку мочевого пузыря по экстравезикальной антирефлюксной методике Licht-Greguar. Мочеточники интубированы стентами № 6, Ch – 14 см. Перед операцией индукция Sol. Simulect 20 мг в/в инраоперационно введен Sol. Metilprednisoloni 500 мг.
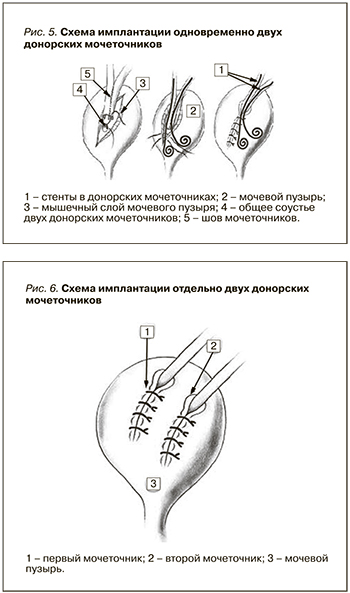
В послеоперационном периоде назначена трехкомпонентная иммуносупрессивная терапия: преднизолон 35,0; мофетила микофенолат 1000,0; адваграф 11,0. Функция трансплантата восстановилась немедленно. Послеоперационный период протекал без осложнений. Биохимия крови перед выпиской: креатинин крови – 0,14 мкмоль/л, мочевина крови – 12,1 ммоль/л, общий белок – 72 г/л, альбумин – 37,5 г/л, триглицериды – 2,28 ммоль/л. Скорость клубочковой фильтрации – 59,6 мл/мин. Анализ мочи: реакция: pH – 6,50, белок не обнаружен, лейкоциты – 2–5 в поле зрения, эритроциты не обнаружены, мицелий дрожжеподобного гриба и почкующихся клеток нет. Неоднократный посев мочи – роста нет. Рентгеновская компьютерная томография брюшной полости: полное удвоение донорской почки, визуализируются две лоханки, два донорских мочеточника, имплантированные в мочевой пузырь одним соустьем. Проходимость контраста по мочеточникам хорошая (рис. 2). При ультразвуковом сканировании размер донорской почки – 127×98×55 мм, толщина паренхимы – 18–25 мм, чашечно-лоханочная система и мочеточники не расширены, прослеживаются два донорских мочеточника, интубированные стентами (рис. 3) Вид двух стентов в просвете мочевого пузыря перед удалением при цистоскопии (рис. 4). Два стента одновременно удалены на 20-е сутки после трансплантации почки. Больная выписана домой. Схема операции имплантации одновременно двух мочеточников в мочевой пузырь приведена на рис. 5.
Клинический случай 2
Больная К. 46 лет. 0(I)Rh-pos. Поступила в отделение трансплантации в феврале 2015 г. для выполнения экстренной операции трансплантации почки.
 Больна с 3-летного возраста. Отмечала отечность лица, боли в суставах, субфебрилитет. С 6 лет диагностирован ревматоидный артрит. Проводилось противоревматическое лечение. С 2006 г. стойкое повышение артериального давления. С 2007 г. диагностирована терминальная стадия почечной недостаточности, СКФ – 11 мл/мин. Сформирована дистальная артериовенозная фистула на предплечье. С 10.06.2007 находится на лечении программным гемодиализом. В связи с деформацией суставов и костей неоднократно отмечались тромбозы артериовенозных фистул. В связи с невозможностью создания адекватного сосудистого доступа для гемодиализа больной имплантирован гортекс на правом бедре.
Больна с 3-летного возраста. Отмечала отечность лица, боли в суставах, субфебрилитет. С 6 лет диагностирован ревматоидный артрит. Проводилось противоревматическое лечение. С 2006 г. стойкое повышение артериального давления. С 2007 г. диагностирована терминальная стадия почечной недостаточности, СКФ – 11 мл/мин. Сформирована дистальная артериовенозная фистула на предплечье. С 10.06.2007 находится на лечении программным гемодиализом. В связи с деформацией суставов и костей неоднократно отмечались тромбозы артериовенозных фистул. В связи с невозможностью создания адекватного сосудистого доступа для гемодиализа больной имплантирован гортекс на правом бедре.
04.02.2015 выполнена трансплантация трупной почки слева. Донор – мужчина 51 года. Причина смерти – черепно-мозговая травма, не совместимая с жизнью. Эксплантация органов на фоне мозговой смерти. Совпадение по групповой совместимости полное, по системе HLA – по 3 антигенам: А4, В27, DR4. Уровень антител – 0%. Во время операции после обработки донорской почки выявлено, что имеются две артерии, отстоящие друг от друга на 4 см на одной площадке. Выявлены две вены с участком нижней полой вены, два мочеточника с общей брыжейкой. Иссечена артериальная площадка между двумя артериями до 0,5 см. Вены удлинены на одной площадке за счет участка нижней полой вены. Реконструированные сосуды анастомозированы с подвздошными сосудами. Каждый мочеточник имплантирован отдельно в мочевой пузырь по экстравезикальной антирефлюксной методике Lich–Greguar. Схема операции приведена на рис. 6. В оба мочеточника имплантированы стенты № 6, Сh – 14 см. Индукционная терапия – базиликсимаб. Во время операции в/в введен Sol. Metilprednisolon 500 мг. Назначена трехкомпонентная иммуносупрессивная терапия: метипред, такролимус, мофетила микофенолат. Послеоперационный период осложнился острой почечной недостаточностью трансплантата, потребовавшей проведения 5 сеансов гемодиализа. Восстановление функции трансплантата на 16-е сутки после операции. В связи с отсроченной функцией трансплантата 12.02.2015 выполнена биопсия пересаженной почки. Заключение: острый канальцевый некроз. С учетом признаков микроциркуляторного воспаления нельзя исключить гуморального отторжения трансплантата. В связи с отторжением трансплантата проведено три сеанса плазмафереза. Введен внутривенно Sol. Metilprednisoloni 250 мг. При ультразвуковом сканировании размер донорской почки составил 127×98×55 мм, толщина паренхимы – 18–25 мм. Чашечно-лоханочная система и мочеточники не расширены. Прослеживаются два донорских мочеточника, интубированные стентами (рис. 5). Удаление стентов из мочеточников проведено на 25-е сутки. Креатинин крови перед выпиской составил 0,15 мкмоль/л, мочевина крови – 18 ммоль/л, общий белок – 55 г/л, альбумин – 25,3 г/л. СКФ – 56 мл/мин. Количество мочи за сутки составило до 2500 мл. В посевах мочи роста нет. Анализ мочи: реакция – 6,50, белок – 0,87 г/л, лейкоциты – 10–15 ЕД в п/зр., эритроцитов нет, бактерий нет. Больная выписана домой.
Обсуждение
При выполнении трансплантации почки для восстановления мочевых путей наиболее подходящей стала уретероцистостомия [7]. Мочеточник анастомозируется или экстравезикальным, или интравезикальным методом с антирефлюксной или без антирефлюксной защиты. До настоящего времени нет единого мнения, какой тип уретероцистоанастомоза следует выполнять при трансплантации почки [8, 9]. Следует отметить, что выполнение уретероцистоанастомоза с антирефлюксной защитой наиболее физиологично для оттока мочи из пересаженной почки. Однако данный вид антирефлюксной защиты может вызывать различные урологические осложнения, по оценкам исследователей, составляющие от 3 до 20% от всех хирургических осложнений, причем среди этих осложнений преобладают мочевые свищи и стриктуры мочеточника [10–12]. Наиболее тяжелым осложнением служит некроз донорского мочеточника, что составляет 3% от всех урологических проблем [10, 13, 14].
К причинам большинства этих осложнений кроме технической ошибки относится и нарушение кровоснабжения донорского мочеточника, особенно дистальных его частей. Другой причиной уретеральных осложнений являются пороки развития мочевого тракта. Один из таких пороков – это дублирование мочеточника [13, 15]. У взрослого населения оно происходит с частотой 0,6 до 0,8% [16].
У описываемых больных имплантация донорских мочеточников выполнена различными методами. В первом случае создана дупликатура из двух мочеточников, имплантированная в мочевой пузырь по экстравезикальной методике Lich–Greguar. Во втором – по экстравезикальной антирефлюксной методике Politano–Leadbetter. При этом каждый донорский мочеточник имплантирован отдельно. В обеих методиках проведено стентирование донорских мочеточников. Ни в одном из случаев осложнений со стороны имплантированных мочеточников не было.
В настоящее время не определено, какая методика уретероцистоанастомоза наиболее адекватно подходит для одновременной имплантации двух мочеточников [9]. Опасения трансплантационных хирургов основываются на том, что кровообращение дистальных отделов донорских мочеточников значительно нарушено, в связи с чем число осложнений, связанных с мочеточниками, кратно возрастает [17, 18]. Однако часть трансплантологов сообщает об удовлетворительных результатах при имплантации двух мочеточников при использовании различных методик уретероцистостомии [19]. Большинство авторов применяют отдельную имплантацию каждого мочеточника в мочевой пузырь, используя методику Политано–Линдбетера (Politano–Leadbetter) или экстравезикальные методики по Lich, Witzel, Rohl и Sampson. D.D. Nghiem описал модификацию экстравизикальной методики с единичным туннелем, таким образом избегая второй миотомии [18, 20]. T. Nakatani описал методику экстравезикальной имплантации одновременно двух мочеточников без их сшивания в дистальном отделе с установкой стентов. Автор не отметил никаких урологических осложнений и рекомендовал описанную им методику как безопасный метод уретероцистостомии при наличии дупликатуры мочеточников [9]. Haferkamp et al. выполнили 19 операций по пересадке почек с удвоенными мочеточниками. У 9 больных мочеточники были анастомозированы с мочевым пузырем раздельно, у 10 – мочеточники были сшиты между собой в дистальном их отделе и вшиты в мочевой пузырь единым блоком с использованием антирефлюксной экстравезикальной уретероцистостомии. Мочеточники были стентированы. Разницы в осложнениях между двумя группами отмечено не было [18]. T. Sulikowski рекомендовал использование стентов мочеточника в случае всех уретероцистомий с дублированными мочеточниками [19]. M. Heidari описал 12 больных, которым была выполнена трансплантация почки с двумя мочеточниками, соединенными с использованием экстравезикальной уретероцистостомии с одним подслизистым тоннелем. Осложнений не было. Авторы отмечают, что эта техника уретероцистостомии с одним тоннелем – надежная и безопасная процедура для двойных мочеточников при трансплантации почки [21].
Заключение
Таким образом, обзор литературы и наши наблюдения позволяют заключить, что противопоказаний к трансплантации почки с двумя мочеточниками нет. Пересадка почки с двумя мочеточниками возможна. Нет единого мнения о характере имплантации двух мочеточников в мочевой пузырь. Наиболее часто выполняются два вида имплантации мочеточников: поэтапная пересадка каждого донорского мочеточника или соединение мочеточников в дистальном отделе с имплантацией их одним стволом в мочевой пузырь. Во всех случаях рекомендуется применять стентирование мочеточников. Решение о тактике выполнения имплантации удвоенных мочеточников решает хирург, осуществляющий трансплантацию почки.



