Введение
Проблема нарушений функции мочевого пузыря занимает одно из ведущих мест в детской нефрологии, урологии и неврологии. Распространенность нервно-мышечной дисфункции мочевого пузыря (НМДМП) составляет от 8 до 15% среди детского населения [1]. До 90% всех форм НМДМП у детей связаны с нарушением нейрогуморальной регуляции данного органа вследствие незрелости микционных центров [2]. Данная патология в большинстве случаев приводит к развитию и поддержанию вторичных изменений мочевыводящей системы, таких как рецидивирующий хронический пиелонефрит, цистит, а также пузырно-мочеточникового рефлюкса и уретерогидронефроза. К осложнениям относятся нефросклероз, артериальная гипертензия, хроническая почечная недостаточность, соответственно, ранняя инвалидизация и ухудшение качества жизни, что определяет социальную значимость болезней этой группы.
В значительной мере функция почек обусловлена эффективностью кровообращения в их сосудистом бассейне. Как при затруднении оттока крови от органа, так и при нарушении ее притока возникают расстройства ренальной гемодинамики. Темпы прогрессирования нарушения функции почек прямо пропорциональны степени гемодинамических нарушений в них [3]. На сегодняшний день информативным способом оценки состояния гемодинамики почек является допплерометрия ввиду ее высокой информативности, неинвазивности, относительной дешевизны, возможности многократного применения, отсутствия ионизирующей нагрузки на пациента, что особенно важно в педиатрической практике. С помощью допплерометрии проводят качественную и количественную оценку кровотока во всех сосудах почки и косвенно оценивают функциональную сохранность почечной паренхимы, характер патологического процесса, его прогноз и эффективность проводимой терапии [4]. Единичные работы посвящены оценке почечного кровотока при нарушениях мочеиспускания. Так, М.Ф. Абрамова, Н.Б. Гусева и соавт. (2014) при изучении морфофункциональных изменений органов малого таза у детей с сочетанием энуреза и хронического запора с применением допплерографии почечных артерий показали наличие сосудистой дисфункции в левой и правой почках. Индексы резистентности у этих больных в трех отделах почечной артерии значительно превышали соответствующий показатель здоровых детей [5].
При проведении объективного обследования детей с патологией мочевой системы и анализа их результатов часто диагностируются проявления дисплазии соединительной ткани (ДСТ), которые продолжают оставаться важной проблемой, потому что оказывают свое влияние на формирование хронической патологии, приводящей к инвалидности. Синдром ДСТ довольно часто сочетается с патологией почек [6]. И наоборот, почти у каждого третьего пациента с ДСТ наблюдаются симптомы, характерные для поражения мочевыделительной системы: частое мочеиспускание, чувство неполного опорожнения мочевого пузыря, никтурия, энурез, симптомы дисметаболической нефропатии, а при углубленном обследовании выявляются поликистоз, дивертикулез мочевого пузыря, нефроптоз, атония чашечно-лоханочной системы (ЧЛС), удвоение почки и/или мочевыводящих путей [7, 8]. Сложная организация соединительной ткани, ее повсеместное присутствие в органах и тканях организма и множество выполняемых ею функций приводят к тому, что клинические проявления дефектов соединительной ткани и прогноз заболеваний чрезвычайно многообразны. В том числе несомненно влияние феномена ДСТ на региональный кровоток. Это касается как почечного, так и брахиоцефального бассейнов. Больше изучены особенности брахиоцефального, чем почечного, кровотока на фоне ДСТ при разных нозологических формах. Так, В.Г. Арсеньев (2012) показал, что в целом для пациентов с ДСТ характерны артериальные и венозные гемодинамические особенности кровотока в экстракраниальных отделах магистральных сосудов: асимметрия и/или снижение скорости кровотока по позвоночным артериям (64%), асимметрия и/или нарушение венозного оттока по яремным венам (34%). Частота изменений, по данным ультразвукового исследования (УЗИ), составляет 1,79 на одного ребенка [9]. При этом исследования брахиоцефального и почечного кровотока на фоне ДСТ у пациентов с нейрогенными расстройствами мочеиспускания ранее не проводились.
Цель исследования: установить характер сосудистых дисфункций у детей с НМДМП с учетом выраженности проявления синдрома ДСТ.
Материал и методы
В исследование были включены 60 детей, страдавших НМДМП, в возрасте 5–15 лет. Диагноз НМДМП выставлен, согласно отраслевым стандартам и по классификации М.Д. Джавад-Заде и В.М. Державина (198). Выборку осуществляли среди пациентов, находившихся на стационарном обследовании в нефрологическом отделении. В контролируемое сравнительное исследование включались дети, соответствовавшие следующим критериям: возраст 5–15 лет; дети, направленные на стационарное обследование с редкими или частыми мочеиспусканиями днем; отсутствие наследственных форм ДСТ; информированное согласие родителей ребенка на участие в обследовании. Из исследования исключались дети с заболеваниями других систем, при которых была необходимость приема лекарственных препаратов на момент обследования, потенциально оказывающих влияние на вегетативные гомеостаз и брахицефальный кровоток; с заболеваниями мочевой системы, способными влиять на результаты исследования (пиелонефрит, гломерулонефрит, мочекаменная болезнь); отказом пациента или родителей участвовать в исследовании; при несоответствии критериям включения.
При диагностировании ДСТ у детей исключали наследственные нарушения соединительной ткани и выявляли 6 и более малых внешних или висцеральных проявлений с вовлечением 3 и более органов из разных систем. Оценку проводили по системе баллов, ранжированных по значимости, внешних и висцеральных признаков системного вовлечения соединительной ткани. Максимальное суммарное число баллов составило 66. При фенотипической диагностике значимой была сумма в 12 баллов и более, при висцеральной – вовлечение 3 и более органов в разные системы. Результат до 12 баллов расценивался как отсутствие дисплазии, 12–20 – дисплазия I степени тяжести, от 20 до 30 – дисплазия II степени, более 30 баллов – III степень.
В дальнейшем все пациенты были разделены на две группы: 1-я – ДСТ легкой (37 детей), 2-я – ДСТ средней степеней тяжести (23 ребенка). Далее сравнение проводили между данными группами. Для описания распределений применяли среднее арифметическое значение (М), стандартную ошибку среднего (m). Достоверность различий качественных признаков оценивали с помощью χ2-критерий Пирсона и критерия Фишера для больших и малых групп соответственно. Для оценки количественных признаков сравнение проводилось методом расчета критерия Манна–Уитни. Значения р<0,05 рассматривали как значимые.
Результаты исследования
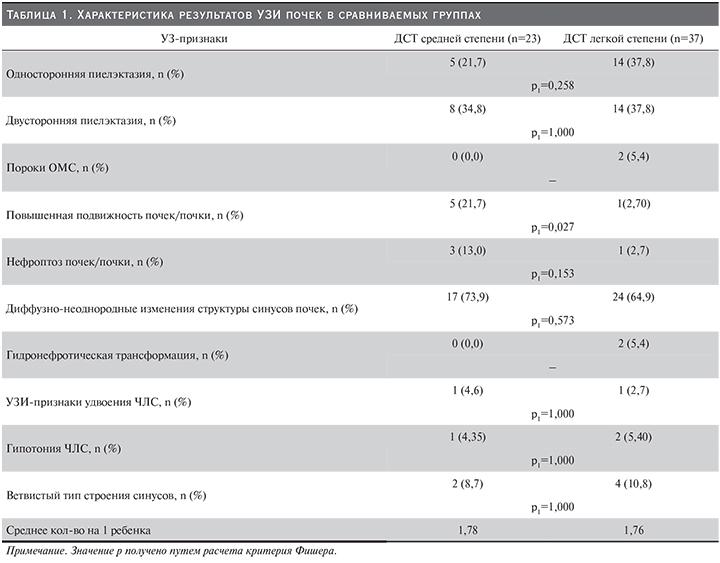
На первом этапе проведена сравнительная оценка результатов УЗИ почек в сравниваемых группах. В целом у детей с НМДМП с высокой частотой определены признаки дву- или односторонней пиелоэктазии (36,7%) и диффузно-неоднородные изменения структуры синусов почек (68,8%). Более грубые изменения по типу гидронефротической трансформации почки, нефроптоза, других пороков органов мочевой системы (ОМС) отмечены у 3–10% детей. В зависимости от степени выраженности признаков ДСТ при анализе установлено, что достоверные различия касаются только повышенной подвижности почек, которая чаще отмечается у больных ДСТ средней степени тяжести. Обращает на себя внимание тот факт, что более «грубые» изменения по типу гидронефротической трансформации почек, удвоение ЧЛС, другие пороки развития ОМС встречаются только в группе больных ДСТ легкой степени, что не позволяет однозначно трактовать феномен ДСТ как безусловно патологический. Результаты представлены в табл. 1.
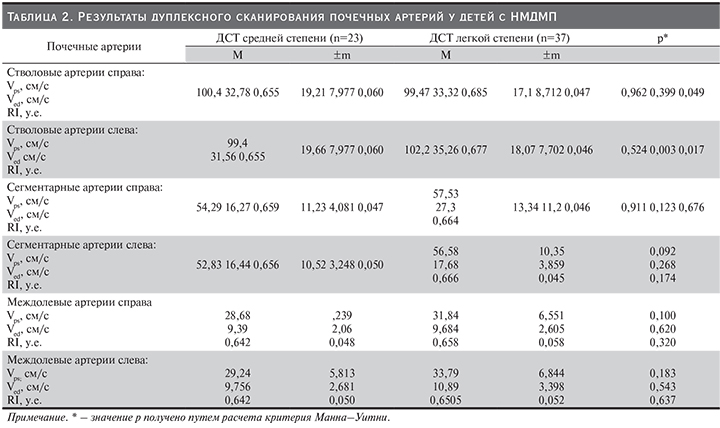
На втором этапе проведено дуплексное сканирование сосудов почек. По результатам сканирования почечных артерий показано достоверное снижение сосудистого сопротивления (индекса резистентности) на фоне ДСТ средней степени в крупных стволовых артериях с двух сторон по сравнению с больными ДСТ легкой степени, что ведет к снижению скорости кровотока по данным артериям. В более мелких артериях эта тенденция сохранялась, но различия недостоверны. Данные представлены в табл. 2.
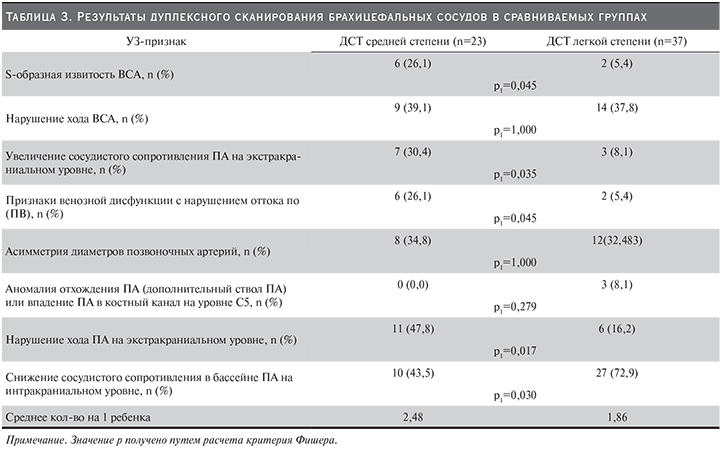
Более значимые различия выявлены при исследовании показателей брахиоцефального кровотока в сравниваемых группах. Это касается прежде всего структурных аномалий сосудов брахиоцефальной зоны. Так, S-образная извитость внутренних сонных артерий (ВСА) достоверно чаще встречалась у детей на фоне ДСТ средней степени тяжести (26,1%), чем на фоне ДСТ легкой степени (5,4%). Кроме того, у больных на фоне ДСТ средней тяжести также достоверно чаще выявляли увеличение сосудистого сопротивления позвоночных артерий на экстракраниальном уровне (30,4%), признаки венозной дисфункции с нарушением оттока по позвоночным венам (ПВ, 26,1%), нарушение хода позвоночных артерий (ПА) на экстракраниальном уровне (47,8%). Результаты представлены в табл. 3.
При сравнении выраженности гемодинамических нарушений на различных участках брахиоцефального кровотока у больных ДСТ легкой и средней степеней тяжести выявлен достоверный рост сосудистого сопротивления (индекса резистентности) на уровне ПА у пациентов на фоне ДСТ средней степени тяжести. Так, в группе больных ДСТ средней степени тяжести данный показатель составил 0,731±0,096 у/е слева и 0,7569±075 у/е справа, а при ДСТ легкой степени тяжести – 0,694±0,078 у/е слева (р=0,036) и 0,751±0,077 у/е справа (р=0,230).
Обсуждение
Таким образом, для больных НМДМП характерны множественные «малые» структурные аномалии, более значимые анатомические дефекты (гидронефротическая трансформация, удвоение ЧЛС, другие пороки ОМС) встречаются у 10% детей. В группе больных ДСТ средней степени тяжести достоверно выше доля пациентов с повышенной подвижностью почек.
Подобные данные получены В.Г. Арсентьевым (2012), в работе которого также не выявлено параллелизма при утяжелении комплекса признаков ДСТ с нарастанием числа находок на УЗИ почек, но установлено, что у детей с ДСТ выше уровень приобретенных аномалий, чем в контрольной группе: гиперподвижность (12,0 и 0%; p<0,005), нефроптоз (6,3 и 0%; p<0,02), пиелоэктазии (5,0 и 0%; p<0,05) [9].
Что касается нарушений гемодинамики, то они носят разнонаправленный характер. При оценке почечного кровотока у пациентов с более выраженными признаками ДСТ выявлено снижение резистентности магистральных сосудов, ведущее к снижению скорости кровотока. С другой стороны, при исследовании брахиоцефального кровотока выявлено увеличение сосудистого сопротивления ПА на экстракраниальном уровне (30,4%) и признаки венозной дисфункции с нарушением оттока по ПВ (26,1%).
В целом полученные результаты говорят в пользу данных Т.И. Кадуриной (2013), что при ДСТ повышается проницаемость эндотелия, происходит замещение сосудистых слоев соединительной тканью, развивается фиброз. Увеличение жесткости артерий в свою очередь стимулирует формирование и прогрессирование структурной патологии артерий разного калибра [10].
Заключение
У детей с НМДМП с высокой частотой определяются признаки дву- или односторонней пиелоэктазии (36,7%) и диффузно-неоднородные изменения структуры синусов почек (68,8%). Изменения по типу гидронефротической трансформации почки, нефроптоза, других пороков ОМС отмечены в целом у 3–10% детей. На фоне ДСТ средней степени тяжести повышенная подвижность почек и снижение сосудистого сопротивления (индекса резистентности) в крупных стволовых артериях выявляются достоверно чаще, чем при ДСТ легкой степени.
Наиболее характерны для ДСТ рост числа «малых сосудистых» аномалий: S-образная извитость и нарушения хода ВСА, нарушение хода ПА на экстракраниальном уровне и гемодинамические нарушения по типу увеличения сосудистого сопротивления ПА на экстракраниальном уровне и венозной дисфункции с нарушением оттока по ПВ.



