Введение
В настоящее время хроническая болезнь почек (ХБП) служит неоспоримым глобальным общественным приоритетом [1, 2]. В мировом масштабе общее число людей с ХБП, острым повреждением почек (ОПП) и лиц, получающих заместительную почечную терапию (ЗПТ), превышает 850 млн, что действительно вдвое превышает оценочное число людей с диабетом во всем мире и в 20 раз выше, чем число людей, страдающих синдромом приобретенного иммунодефицита (СПИД)/вирусом иммунодефицита человека (ВИЧ) во всем мире [3].
Темп прироста числа пациентов, получавших ЗПТ, в Российской Федерации в 2015 г. по сравнению с предыдущим составил 11,6%, превысив среднемировой, однако все еще уступая ряду стран с «быстрорастущей» обеспеченностью ЗПТ. По данным последних 5 лет, Россия входит в топ 10 стран с наиболее быстрым развитием ЗПТ (58 начинающих ЗПТ больн./млн в год), уступая Чили (180 больн./млн), Чехии (227 больн./млн), Южной Корее (289 больн./млн), Таиланду (338 больн./млн) и США (378 больн./млн) [4].
У большинства пациентов с ХБП не развивается прогрессирующая или терминальная почечная недостаточность (ТПН), но у них повышен риск сердечно-сосудистых заболеваний (ССЗ) [5]. Риск ССЗ возрастает обратно пропорционально уровню скорости клубочковой фильтрации (СКФ), и при СКФ<30 мл/мин превышает таковой при сохранной функции почек в 5,5 раза. Значительное число пациентов с ХБП умирают вследствие сердечно-сосудистых осложнений еще до ТПН [6].
Согласно международным рекомендациям [7], всех пациентов с ХБП следует рассматривать как лиц с повышенным риском развития ССЗ с уровнем доказательности 1А.
У пациентов с эссенциальной артериальной гипертензией (АГ) без каких-либо сердечно-сосудистых осложнений умеренное снижение СКФ сопровождается удвоением риска кардиальной смерти [8, 9]. У пациентов с хронической сердечной недостаточностью (ХСН) СКФ – такой же значимый прогностический фактор, как и величина фракции выброса левого желудочка или функциональный класс сердечной недостаточности по NYHA (New York Heart Association) [10]. Кроме того, выяснилось, что в общей популяции населения в возрасте 45–74 лет снижение СКФ ниже 60 мл/мин выступает в качестве независимого фактора риска острого инфаркта миокарда, общей и сердечно-сосудистой смертности [11].
Несмотря на то что распространенность ХБП и ее влияние на здоровье изучались в основном в экономически развитых странах, бремя этого заболевания еще больше в развивающихся странах [12, 13].
По разным данным, расходы на диализ и трансплантацию составляют 2–3% годового бюджета здравоохранения в странах с высоким уровнем дохода, которые расходуются менее чем на 0,03% от общей численности населения этих стран. В странах с низким и средним уровнями дохода большинство людей с почечной недостаточностью не имеют достаточного доступа к жизненно необходимым диализу и трансплантации почки [14].
Также были проведены исследования, изучавшие проблемы ССП у пациентов разных популяций с ХБП на гемодиализе. В т.ч. были изучены популяции городского и сельского населения и получены отличительные данные, подтвердившие актуальность изучения данной проблемы [15].
Цель работы: сравнительно изучить структуру сердечно-сосудистой патологии (ССП) сельского и городского населения Республики Узбекистан с ХБП 5-й стадии, получающего программный гемодиализ (ПГД).
Материал и методы
Обследованы 165 (90 мужчин и 75 женщин) пациентов с ХБП 5-й стадии, находившихся на ПГД. Средний возраст обследованных составил 48,1±14,2 года. В исследование были включены пациенты с клинически установленным диагнозом ХБП 5-й стадии [16] в исходе нефропатий различного генеза. СКФ рассчитывали, основываясь на концентрации креатинина сыворотки по формуле CKD-Epi [7]. Основные исходные заболевания: хронический гломерулонефрит (n=76), сахарный диабет – СД (n=44), мочекаменная болезнь (n=14), хронический пиелонефрит (n=10) и др. Исследования проводились в Республиканском специализированном научно-практическом медицинском центре нефрологии и трансплантации почки, Республиканском специализированном научно-практическом медицинском центре урологии (Ташкент) и Сырдарьинском областном многопрофильном медицинском центре (Гулистан). Длительность ПГД составила 29 (6–89) месяцев. ПГД проводился на аппаратах Fresenius Medical Care 4008S, диализаторами WEGO F15 LW и Diacap Polysulfone LOPS18 LW. Сеансы ГД проводили по схеме 4 часа 3 раза в неделю (720 ч/нед), согласно международным рекомендациям [17]. Для ГД использовали бикарбонатный раствор в качестве диализата. Показатели Kt/V соответствовали минимальным значениям целевого уровня, равного 1,4. Критерии для исключения из исследования: возраст до 18 лет, пациенты перенесшие трансплантацию почки, пациенты получавшие ПГД при острой почечной недостаточности. Всех пациентов в зависимости от постоянного местопроживания разделили на две группы: в группу Город включили 104 пациента городского населения, в группу Село – 61 пациент сельской местности.
Статистическая обработка данных проводилась с помощью стандартного пакета Statistica for Windows, версия 6.0. Для сравнения двух независимых групп использовали критерий Манна–Уитни, для сравнения более двух независимых групп – критерий Краскела–Уоллиса, при корреляционном анализе – критерий Спирмена, также проводили множественный линейный регрессионный анализ. Достоверными считали различия при p<0,05.
Результаты и обсуждение
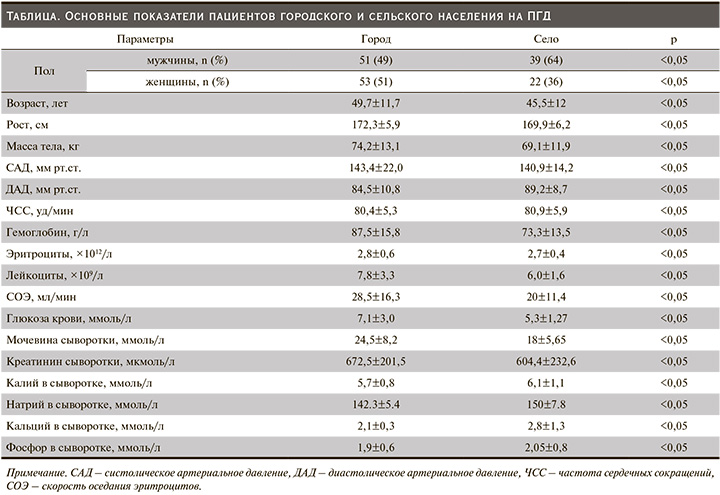
 Основные показатели пациентов обеих групп были сопоставимыми (пол, возраст, рост и масса тела, см. таблицу). Исходные нозологии в группах существенно не различались. В обеих группах ведущими нозологиями стали хронический гломерулонефрит (Город – 62%, Село – 37%), СД (32%, 18%), мочекаменная болезнь (11%, 5%) и пиелонефрит (4%, 10%). Стоит отметить большую разнообразность исходных нозологий у пациентов городского населения (10), в то время как у сельского населения было меньшее число нозологий (6).
Основные показатели пациентов обеих групп были сопоставимыми (пол, возраст, рост и масса тела, см. таблицу). Исходные нозологии в группах существенно не различались. В обеих группах ведущими нозологиями стали хронический гломерулонефрит (Город – 62%, Село – 37%), СД (32%, 18%), мочекаменная болезнь (11%, 5%) и пиелонефрит (4%, 10%). Стоит отметить большую разнообразность исходных нозологий у пациентов городского населения (10), в то время как у сельского населения было меньшее число нозологий (6).
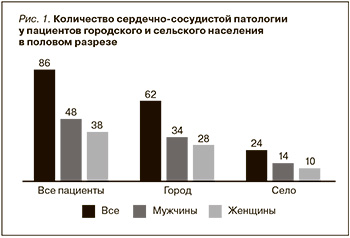
По результатам исследования, более чем у половины (86/52,1%) всех обследуемых пациентов была обнаружена ССП. В обеих группах преобладали мужчины (рис. 1). СД встречался у 44 (26,6%) всех обследованных пациентов. Также выявлено, что почти у 127 (77%) больных была диагностирована ренальная анемия.
Самой частой встречаемой ССП в обеих групп оказались АГ, ишемическая болезнь сердца (ИБС) и ХСН. ИБС наблюдался в виде стабильной стенокардии напряжения различных функциональных классов. Следует отметить, что в обеих группах эти патологии встречались как изолированно, так и в сочетании. Рассмотрим эти патологии по группам.
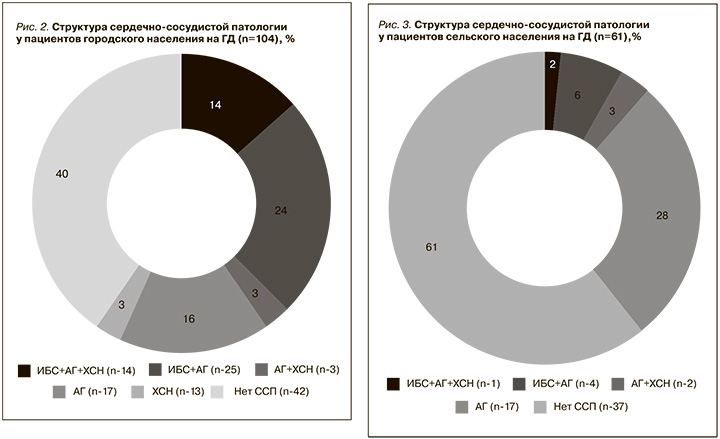
В группе Город у 62 (59,6%) обследованных пациентов была обнаружена ССП. Выявлено, что все (39 человек) больные, которым была диагностирована ИБС, также имели ХСН и/или АГ. Сочетание ИБС+АГ+ХСН имели 14 (13,5%) обследованных пациентов. Сочетание ИБС+АГ встречалось у 25 (24%) пациентов. «Изолированную» АГ имели 17 пациентов, и только у троих отмечено сочетание в виде АГ+ХСН. Также выяснилось, что ХСН чаще встречается в сочетанном виде. Так, например, сочетание ИБС+АГ+ХСН составило 70% (n=14) случаев с ХСН, АГ+ХСН – 15% (n=3). И только 15% (n=3) пациентов с ХСН не имели других ССЗ (рис. 2).
В группе Село было обнаружено относительно меньшее (24/39%) число ССП, чем в группе Город (рис. 3). Также была выявлена коморбидность ССЗ. Все (n=24) больные ССП имели АГ. Соответственно, все 4 пациента имевших ИБС, также страдали АГ. Один пациент имел сочетанную патологию в виде АГ+ИБС+ХСН. Сочетание АГ+ХСН встретилось у я 2 пациентов, 17 пациентов имели только АГ.
В половом разрезе существенной разницы в структуре ССП не наблюдалось. Если у пациентов с АГ в группе Город (n=55) незначительно преобладали женщины (28), то в группе Село это были мужчины (14 человек из 24). ИБС чаще страдали мужчины группы Село, в то время как в группе Город этот показатель был равным между обоими полами. В обеих группах мужчины также незначительно чаще страдали ХСН: в группе Город – 12 мужчин, 8 женщин, в группе Село – 2 и 1 соответственно.
Так как на сегодняшний день СД рассматривают как эквивалент наличия у пациента клинически выраженного ССЗ и независимый фактор риска ССЗ [18], интересным моментом стало выявление СД у пациентов с ССП. Необходимо отметить высокую встречаемость СД в сочетании с ССП у пациентов группы Город, находившихся на ПГД. Так, почти у 26 (42%) пациентов с ССП был диагностирован СД. В группе Село только у 5 (21%) пациентов с ССП был выявлен СД.
Как известно, длительно существующая анемия может сопровождаться расширением левых отделов сердца и развитием ССЗ [19]. Исходя из этого, необходимо отметить, что в обеих группах анемией страдали 77% обследованных пациентов (Город – 80, Село – 47 пациентов), которая была представлена ренальной анемией, что характерно для пациентов с ХБП 5-й стадии [20].
Заключение
На основании анализа данных 165 пациентов с ХБП на ПГД можно предположить, что основными ССП у больных являются АГ, ИБС и ХСН.
Согласно результатам нашего исследования, городские пациенты с ХБП 5-й стадии ССП страдают чаще, чем сельское население. Коморбидная патология сердечно-сосудистой системы занимает ведущее место в структуре ССП среди пациентов с ХБП 5-й стадии как в городе, так и в сельской местности. В половом разрезе структура ССП в группах существенно не различается.



