Введение
Кардиоренальные взаимоотношения привлекают в последние годы все большее внимание, что обусловлено значительным ростом распространенности сердечно-сосудистой и почечной патологии, сахарного диабета (СД), ожирения, увеличением продолжительности жизни больных при этих заболеваниях и частым применением интервенционных методов обследования и лечения, прежде всего в кардиологии [1–5].
Острый кардиоренальный синдром (ОКРС) – это патофизиологическое расстройство сердца и почек, при котором острая дисфункция сердца приводит к острой дисфункции почек [6]. Острое почечное повреждение (ОПП) осложняет острую декомпенсацию хронической сердечной недостаточности (ОДХСН) в 25–70 % случаев [7–10]. Развитие ОПП значительно ухудшает прогноз больных ОДХСН и ассоциируется с более высоким риском общей и сердечно-сосудистой смертности, более продолжительной госпитализацией, большей частотой повторных госпитализаций и прогрессированием хронической болезни почек (ХБП) при ее наличии до более высоких стадий [9–13].
До недавнего времени острое нарушение функции почек обозначалось термином «острая почечная недостаточность», диагностические критерии которой не были четко установлены, и оценка ее реальной распространенности представлялась затрудненной [14]. Впоследствии была предложена концепция ОПП, для диагностики которого предлагалось использовать критерии RIFLE (Risk, Injury, Failure, Loss, End-stage renal failure) и AKIN (Acute Kidney Injury Network) [14–15], а в 2012 г. были опубликованы первые рекомендации KDIGO по диагностике и лечению ОПП. Согласно рекомендациям, ОПП диагностируют на основании объединенных критериев RIFLE и AKIN с учетом уровня и динамики уровня креатинина сыворотки (СКр) и/или скорости диуреза (табл. 1) [16].
Данные о распространенности и прогностическом значении различных клинических вариантов ОПП в Российской Федерации практически отсутствуют. В связи с этим представляет существенный интерес изучение ОПП в зависимости от времени развития (до или во время госпитализации, раннее или позднее), наличия или отсутствия в анамнезе ХБП, транзиторного или персистирующего течения.
Целью исследования было изучение частоты, тяжести, клинических вариантов и исходов ОПП в популяции пациентов, госпитализированных с ОДХСН.
Материал и методы
 В исследование были включены 183 человека (125 мужчин), экстренно госпитализированных с клиническими проявлениями ОДХСН. ОДХСН диагностировано на основании общепринятых критериев: быстрое внезапное нарастание симптомов СН у пациентов с ранее диагностированной ХСН при наличии объективных признаков поражения сердца (систолическая и/или диастолическая дисфункция по данным ЭхоКГ) [17].
В исследование были включены 183 человека (125 мужчин), экстренно госпитализированных с клиническими проявлениями ОДХСН. ОДХСН диагностировано на основании общепринятых критериев: быстрое внезапное нарастание симптомов СН у пациентов с ранее диагностированной ХСН при наличии объективных признаков поражения сердца (систолическая и/или диастолическая дисфункция по данным ЭхоКГ) [17].
В исследование не включали больных с острым коронарным синдромом, терминальной стадией хронической почечной недостаточности, тяжелыми нарушениями функции печени, аутоиммунными и онкологическими заболеваниями.
В анализ включены пациенты в возрасте от 45 до 84 лет (в среднем 68,9 ± 9,4 года). Длительность ХСН составила от месяца до 18 лет (в среднем 3,6 ± 3,0 года). Артериальной гипертонией (АГ) в анамнезе страдали 86,9 %, ишемической болезнью сердца (ИБС) – 55,7 %, перенесенным инфарктом миокарда – 53,0 % и инсультом – 13,7 %. Из сопутствующих заболеваний ХБП выявлена у половины пациентов, у каждого третьего пациента – сахарный диабет (СД) 2 типа, у каждого пятого – анемия. Клинико-демографическая характеристика включенных в исследование пациентов приведена в табл. 2.
Клинический статус больных оценивали с использованием общепринятых методов (опрос, осмотр, физическое обследование). Для оценки динамики симптомов сердечной недостаточности использован опросник Борг для самостоятельной оценки одышки пациентом.
Оценка тяжести ХСН проведена по критериям Нью-Йоркской ассоциации сердца (NYHA) [17]. В исследование включены пациенты только с III–IV ФК (NYHA).
Клиническая характеристика пациентов с ОДХСН представлена в табл. 3.
Для оценки функционального состояния почек на основании уровня СКр рассчитана СКФ по формуле CKD-EPI [18].
В качестве дополнительных параметров помимо уровня креатинина ежедневно мониторировали уровень мочевины, электролитов (калий, натрий, хлор), мочевой кислоты, оценивали уровень гемоглобина. Анемией считали снижение уровня гемоглобина < 130 г/л для мужчин и < 120 г/л для женщин (ВОЗ, 1997).
ОПП диагностировано при нарастании уровня СКр ≥ 26,5 мкмоль/л (0,3 мг/дл) в течение 48 часов или нарастании СКр ≥ 1,5 раза от исходного в течение 7 дней [16]. В качестве исходного уровня СКр считали наименьший из зарегистрированных при госпитализации уровень СКр [19]. При снижении СКр в ходе госпитализации по сравнению с СКр при поступлении диагностировано раннее ОПП (имевшееся при поступлении). При развитии ОПП в стационаре диагностировано позднее ОПП. Тяжесть ОПП определена на основании объединенных критериев RIFLE и AKIN [16]. ОПП считали транзиторным при снижении уровня креатинина до исходных значений и при восстановлении СКФ в пределах 10 % от исходного к моменту выписки из стационара. В отсутствие этих критериев ОПП определено как персистирующее [16].
 В зависимости от наличия анамнеза ХБП выделены ОПП de novo (у пациентов без анамнеза ХБП) и ОПП на фоне ХБП. При этом ХБП определена только как снижение СКФCKD-EPI < 60 мл/мин/1,73 м2 на протяжении не менее 3 месяцев, предшествующих госпитализации.
В зависимости от наличия анамнеза ХБП выделены ОПП de novo (у пациентов без анамнеза ХБП) и ОПП на фоне ХБП. При этом ХБП определена только как снижение СКФCKD-EPI < 60 мл/мин/1,73 м2 на протяжении не менее 3 месяцев, предшествующих госпитализации.
Пациентов с ОДХСН и ОПП рассматривали как больных ОКРС.
Всем пациентам проведены ЭКГ- и ЭхоКГ-исследования по стандартной методике. Систолической дисфункцией левого желудочка считали уровень ФВ < 40 %.
Пациенты выписаны из стационара с подробными письменными рекомендациями по медикаментозной терапии и изменению образа жизни (диета, уровень физической активности). Через 1 и 6 месяцев (телефонный контакт) после госпитализации оценивали нежелательные явления (повторные госпитализации по поводу ХСН, смерть).
Статистический анализ результатов исследования
Статистический анализ проведен с использованием пакета прикладных статистических программ Statistica 8.0 для Windows с применением стандартных алгоритмов вариационной статистики. Для количественных показателей рассчитывалось среднее арифметическое значение и стандартное отклонение. Данные представлены в виде M ± D, где M – среднее значение, SD – cтандартное отклонение среднего значения. При сравнении средних значений использован двусторонний t-критерий Стьюдента. Качественные переменные описаны абсолютными (n) и относительными (%) значениями. Для сравнения частот признаков и качественных переменных пользовались критерием хи-квадрат (χ2). Оценка достоверности различий между группами проведена при помощи непараметрического критерия Манна–Уитни. При непараметрическом распределении данных рассчитан коэффициент ранговой корреляции Спирмена. Различия средних величин и корреляционные связи считались достоверными при уровне значимости р < 0,05.
Результаты исследования
Распространенность острого почечного повреждения в популяции пациентов с декомпенсацией хронической сердечной недостаточности ОПП диагностировано у 41 % (n = 75) пациентов, госпитализированных с декомпенсацией ХСН в среднем на 3,9 ± 3,6 дня (от 0 до 10 дней) пребывания в стационаре, при этом 63 % – в первые 4 дня госпитализации, 75 % – в первые 7 дней. При оценке тяжести ОПП, согласно объединенным критериям RIFLE и AKIN. установлено, что ОПП было представлено преимущественно I и III стадиями (рис. 1).
Среди 55 % пациентов наблюдалось преходящее нарушение функции почек.
Группы пациентов с и без ОПП были сопоставимыми по полу и возрасту (мужчин 53 [71 %] в группе с ОПП и 72 [67 %] в группе без ОПП; средний возраст группы с ОПП – 65,8 ± 8,6 и средний возраст группы без ОПП – 69,3 ± 10,7 года).
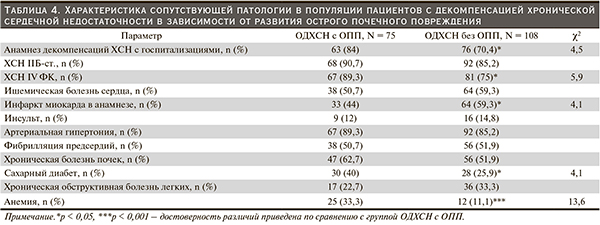
У пациентов с ОПП по сравнению с пациентами без ОПП отмечена более высокая частота СД 2 типа, анемии, большая частота госпитализаций по поводу декомпенсации ХСН в течение предшествующих 12 месяцев. Не выявлены достоверные различия между группами по частоте ХБП. Характеристика сопутствующей патологии представлена в табл. 4.
Группа пациентов с развитием ОПП по сравнению с таковой без ухудшения функции почек в ходе госпитализации исходно клинически была тяжелее и характеризовалась более выраженными проявлениями системного застоя: большая частота ортопноэ, акроцианоза, набухших шейных вен, гепатомегалии, асцита, большая ЧДД при поступлении (24,7 ± 3,2 и 23,4 ± 2,8 в минуту; p < 0,01) с более высокой оценкой по шкале Борга (8,4 ± 2,0 и 7,6 ± 1,6 балла, p < 0,01) (рис. 2).
При изучении эхокардиографических параметров в группах пациентов с развитием ОПП и без ухудшения функции почек в ходе госпитализации не выявлено различий в величине ФВ левого желудочка (46 ± 17 и 43 ± 13 %; p > 0,05), а также частоте выявления сохраненной ФВ левого желудочка (51 и 41 %, p > 0,05).

Пациенты в группе ОДХСН без ОПП по сравнению с пациентами группы ОДХСН с развитием ОПП достоверно чаще получали регулярную терапию ХСН на амбулаторном этапе (74 и 56 %, χ2 = 6,5; p < 0,05), характеризовались значимо более высокой частотой применения петлевых диуретиков (81 и 76 %, χ2 = 8,5; p < 0,01) и сердечных гликозидов (40 и 19 %, χ2 = 5,5; p < 0,05). Также в группе пациентов без ОПП выявлена большая частота терапии статинами (20 и 0 %; χ2 = 9, 7, p < 0,01). В группе пациентов с ОПП по сравнению с пациентами без ОПП отмечена большая частота антитромбоцитарной терапии (76 и 54 %; χ2 = 5,9, p < 0,05).
Анализ терапии ХСН в стационаре продемонстрировал, что пациенты с развитием ОКРС по сравнению с таковыми без ухудшения функции почек в ходе госпитализации характеризовались меньшей частотой назначения всех основных классов лекарственных препаратов для лечения ХСН (рис. 3).
Важно отметить, что пациенты с ОКРС по сравнению с пациентами без ухудшения функции почек в ходе госпитализации характеризовались более низкими стартовыми дозами петлевых диуретиков (65,8 ± 28,2 [от 20 до 120] и 85,6 ± 23,8 мг/сут [от 80 до 120], p < 0,05).

Проанализирована частота назначения других классов лекарственных препаратов, потенциально оказывающих влияние на развитие ухудшения функции почек при ОДХСН. Не выявлено различий в частоте назначения метформина и нестероидных противовоспалительных средств в группах в зависимости от развития ОПП. Пациенты с ОПП по сравнению с таковыми без ОПП характеризовались достоверно меньшей частотой антибактериальной терапии в неадекватной дозе (без поправки на СКФ) (21 и 41 %; χ2= 7,6, p < 0,01), большей частотой назначения инотропных препаратов (11 и 0 %; χ2 = 12,1, p < 0,001). Однако во всех случаях начало инотропной терапии отмечено уже на фоне развившегося ОПП, поэтому терапия инотропными препаратами в данном исследовании не является предиктором развития ОПП, а скорее отражает тяжесть состояния больного.
Клинические варианты острого почечного повреждения: ОПП на фоне ХБП и ОПП de novo
На основании использованных в настоящей работе критериев ХБП диагностирована у 56 % обследованных (n = 103). Пациенты с развитием ОПП по сравнению с таковыми без ухудшения функции почек исходно характеризовались более значимым нарушением функции почек (более высоким уровнем СКр (189 ± 94 и 115 ± 50 мкмоль/л, p < 0,001), более низкой СКФCKD-EPI (36 ± 18 и 56,8 ± 15,6 мл/мин/1,73 м2; p < 0,001), более высоким уровнем мочевины (18,1 ± 10,6 и 8,8 ± 3,0 ммоль/л; p < 0,001)), что было ассоциировано с тенденцией к более высокой частоте ХБП в группе пациентов с ОПП (63 и 52 %; p > 0,05).
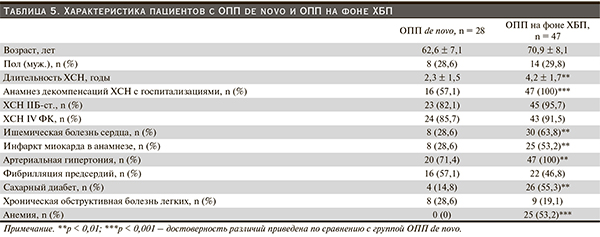
 ОПП на фоне ХБП развилось в 63 % случаев (n = 47). Пациенты с ОПП на фоне ХБП и таковые без анамнеза ХБП (ОПП de novo) были сопоставимыми по возрасту, полу и частоте табакокурения (48 и 52 %; p > 0,05), однако характеризовались большей длительностью ХСН, большей частотой ИБС, инфаркта миокарда, АГ, СД, анемии, госпитализаций по поводу сердечной недостаточности в течение предшествующих 12 месяцев (табл. 5).
ОПП на фоне ХБП развилось в 63 % случаев (n = 47). Пациенты с ОПП на фоне ХБП и таковые без анамнеза ХБП (ОПП de novo) были сопоставимыми по возрасту, полу и частоте табакокурения (48 и 52 %; p > 0,05), однако характеризовались большей длительностью ХСН, большей частотой ИБС, инфаркта миокарда, АГ, СД, анемии, госпитализаций по поводу сердечной недостаточности в течение предшествующих 12 месяцев (табл. 5).
Пациенты с ОПП de novo имели тенденцию к преобладанию проявлений недостаточности кровообращения по малому кругу, и по сравнению с пациентами с ОПП на фоне ХБП достоверно чаще выявлялось ортопноэ (100 и 75 %; p < 0,01), реже – периферические отеки (71 и 100 %; p < 0,001) и дополнительный III тон (14 и 45 %; p < 0,01). Не выявлено различий между группами по величине ФВ левого желудочка (48 ± 16 и 45 ± 18 %; p > 0,05), а также частоте сниженной ФВ левого желудочка (43 и 53 %; p > 0,05).
Пациенты с ОПП на фоне ХБП по сравнению с таковыми с ОПП de novo характеризовались более значимым нарушением функции почек (более высоким уровнем СКр (208 ± 96 и 131 ± 59 мкмоль/л; p < 0,01) с более низкой СКФCKD-EPI (29 ± 11 и 56 ± 21 мл/мин/1,73 м2; p < 0,001) и более низким уровнем гемоглобина при поступлении (113 ± 20 и 147 ± 13 г/л; p < 0,001).
Пациенты c ОПП на фоне ХБП по сравнению с таковыми с ОПП de novo были сопоставимыми по частоте назначения ИАПФ (53 и 57 %; p > 0,05), нитратов внутривенно (53 и 43 %; p > 0,05), однако характеризовались большей частотой терапии бета-блокаторами (70 и 43 %; χ2 = 7,5, p < 0,05), петлевых диуретиков (70 и 43 %; p < 0,05), антагонистов альдостерона (53 и 14 %; χ2 = 11,4, p < 0,01). Развитие ОПП на фоне ХБП в 12 % случаев ассоциировалось с антибактериальной терапией в неадекватных дозах без поправки на СКФ. Развитие ОПП de novo в 14 % случаев ассоциировалось с терапией метформином.
Клинические варианты острого почечного повреждения: раннее и позднее ОПП
У 56 % пациентов ОПП было диагностировано ретроспективно на основании снижения СКр при поступлении в течение госпитализации (раннее ОПП). Пациенты с поздним ОПП (развившимся в стационаре) были старше (71,1 ± 8,3 и 64,9 ± 8,1 года; p < 0,01) пациентов с ранним ОПП и характеризовались большей частотой госпитализаций по поводу сердечной недостаточности в течение предшествующих 12 месяцев (100 и 71 %; p < 0,001) при сопоставимой длительности ХСН (3,3 ± 1,7 и 3,7 ± 2,0 года; p > 0,05). Не выявлено различий в профиле сопутствующих заболевания у пациентов с поздним ОПП по сравнению с таковыми с ранним ОПП. Однако обращает на себя внимание тенденция к большей частоте АГ (91 и 79 %; p > 0,05), ИБС (50 и 43 %; p > 0,05), СД (41 и 30 %; p > 0,05), ХБП (61 и 55 %; p > 0,05) и анемии (41 и 24 %; p > 0,05) при сопоставимом уровне гемоглобина при поступлении (122 ± 29 и 121 ± 14 г/л; р > 0,05) в группе пациентов с ранним ОПП.
Пациенты с поздним ОПП были сопоставимы с пациентами с ранним ОПП по выраженности проявлений системного застоя, не выявлено различий в величине ФВ левого желудочка (44 ± 16 и 47 ± 19 %; р > 0,05), а также частоте выявления сниженной ФВ левого желудочка (49 и 50 %; р > 0,05).
Пациенты с поздним ОПП были сопоставимыми с пациентами с ранним ОПП по уровню СКр (184 ± 77 и 192 ± 105 мкмоль/л; p > 0,05) и калия (4,7 ± 0,5 4,5 ± 0,9 ммоль/л; p > 0,05), но различались более высокими значениями других электролитов (натрий [143,0 ± 3,7 и 141,0 ± 3,8 ммоль/л; p < 0,05] и хлор [108,0 ± 4,1 и 102,0 ± 4,7 ммоль/л; р < 0,001]).
Изучение прогноза острого кардиоренального синдрома в зависимости от тяжести острого почечного повреждения и его вариантов Проанализированы исходы ОПП в популяции пациентов с ОДХСН: 30-дневная смертность и повторные госпитализации по поводу ХСН в течение 6 месяцев. Пациенты с развитием ОПП по сравнению с таковыми без ухудшения функции почек характеризуются худшим краткосрочным прогнозом: более высокой смертностью в течение 30 дней (χ2 = 20,2, p < 0,001) и более частыми повторными госпитализациями по поводу сердечной недостаточности в течение 6 месяцев (χ2 = 4,1; p < 0,05) (рис. 4).
ОПП на фоне ХБП по сравнению с ОПП de novo имело тенденцию к развитию в более поздние сроки госпитализации (4,2 ± 3,8 и 3,0 ± 2,3 дня; p > 0,05), реже отмечался его транзиторный характер, ассоциировалось с меньшей 30-дневной летальностью и большей частотой повторных госпитализаций (рис. 5).
Развитие раннего ОПП по сравнению с поздним ОПП было ассоциировано с более высоким уровнем 30-дневной смертности (рис. 6).
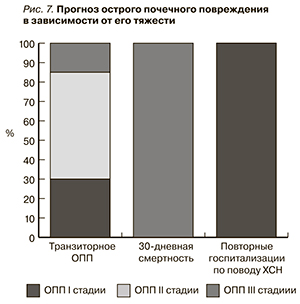
Развитие ОПП III стадии ассоциировалось с таковым неблагоприятного исхода в течение 30 дней – 72 % умерли в течение 30 дней (рис. 7).
Обсуждение результатов
В представленной работе проведено исследование распространенности ОКРС в популяции пациентов с ОДХСН, изучены варианты ОПП и проанализированы его исходы.
ОКРС – частое осложнение декомпенсации ХСН, и в последнее время распространенность его неуклонно растет, варьируясь от 25 до 70 % [20–23]. Такой большой разброс в частоте развития ОКРС в популяции пациентов с ОДХСН обусловлен разными критериями включения пациентов в исследования, а также применением разных диагностических критериев ОПП (в регистрах по сердечной недостаточности под ухудшением функции почек обычно подразумевали повышение уровня СКр в диапазоне от 0,3 до 0,5 мг/дл).

Острая почечная дисфункция обычно развивается в начальные сроки госпитализации: в 50 % случаев – в первые 4 дня, в 70–90 % – в первые 7, что сопоставимо с данными, полученными в представленной работе: у 62,5 % пациентов ОПП развилось в первые 4, у 75 % – в первые 7 дней госпитализации [11–12]. Более значимое нарастание СКр ассоциируется с более высокой смертностью, что и было продемонстрировано в данном исследовании: 72,2 % с ОПП III стадии умерли в течение 30 дней.
У пациентов с ОДХСН в анамнезе часто присутствуют хронические нарушения функции почек, предрасполагающие к развитию ОПП и наблюдающиеся приблизительно в 60 % случаев [6–8]. Представленная работа – одна из первых, в которой проанализированы исходы ОПП de novo и ОПП на фоне ХБП. Установлено, что ОПП у пациентов с ОДХСН гораздо чаще (62,7 %) развивается на фоне ХБП. Пациенты с ОПП на фоне ХБП по сравнению с пациентами с ОПП de novo характеризуются большей длительностью ХСН, большей частотой важной сопутствующей патологии (АГ, ИБС, СД, анемия). Развитие ОПП на фоне ХБП ассоциируется с персистирующим характером и большей частотой повторных госпитализаций по поводу ХСН в течение 6 месяцев, что согласуется с данными литературы [10].
 ОПП реже развивается на догоспитальном этапе и чаще манифестирует после начала лечения в стационаре [6]. Однако в представленной работе частота развития раннего ОПП была выше, чем позднего (56 и 44 %), что может быть связано с применением в качестве критерия «исходного креатинина» наименьшего из зарегистрированных в ходе госпитализации. В настоящем исследовании продемонстрировано, что развитие раннего ОПП ассоциировано с более высоким уровнем 30-дневной смертности (21,4 и 12,1 %). Таким образом, раннее ОПП, т. е. наличие ОПП при поступлении, можно рассматривать в качестве маркера неблагоприятного прогноза пациентов с ОДХСН.
ОПП реже развивается на догоспитальном этапе и чаще манифестирует после начала лечения в стационаре [6]. Однако в представленной работе частота развития раннего ОПП была выше, чем позднего (56 и 44 %), что может быть связано с применением в качестве критерия «исходного креатинина» наименьшего из зарегистрированных в ходе госпитализации. В настоящем исследовании продемонстрировано, что развитие раннего ОПП ассоциировано с более высоким уровнем 30-дневной смертности (21,4 и 12,1 %). Таким образом, раннее ОПП, т. е. наличие ОПП при поступлении, можно рассматривать в качестве маркера неблагоприятного прогноза пациентов с ОДХСН.
ОПП – независимый предиктор годичной смертности в указанной популяции пациентов [6, 24]. Важно как можно раньше идентифицировать популяцию пациентов с высоким риском ухудшения функции почек. В наблюдательных исследованиях продемонстрировано, что в популяции госпитальных пациентов развитие ОПП ассоциируется с более продолжительной госпитализацией и большей частотой повторных госпитализаций по поводу ХСН, прогрессированием ХБП, повышением риска сердечно-сосудистой и общей смертности [25]. Риск неблагоприятных исходов увеличивается независимо от транзиторности или устойчивости ОПП [20, 26]. Даже незначительное нарастание уровня креатинина на 0,3 мг/дл (26,5 мкмоль/л) ассоциируется с повышением смертности [13, 20, 27, 28]. В представленной работе пациенты с развитием ОПП по сравнению с пациентами без ухудшения функции почек в ходе госпитализации характеризуются худшим прогнозом: более высоким уровнем 30-дневной смертности, более высокой частотой повторных госпитализаций по поводу ХСН в течение 6 месяцев, что согласуется с результатами крупных исследований в области СН [11, 27, 29].
Заключение
У 41 % пациентов с ОДХСН на основании действующих критериев диагностировано ОПП. В 63 % случаев оно развивалось на фоне ХБП, ассоциировалось с его персистирующим характером и большей частотой повторных госпитализаций по поводу ХСН в течение 6 месяцев наблюдения. У 56 % пациентов ОПП было диагностировано ретроспективно на основании снижения СКр при поступлении в ходе госпитализации (раннее ОПП) и ассоциировалось с более высоким уровнем 30-дневной смертности.
Таким образом, развитие ОПП при ОДХСН можно рассматривать в качестве предиктора неблагоприятных исходов (кратко- и долгосрочных). Необходимо тщательное мониторирование функционального состояния почек в указанной популяции пациентов с целью своевременной диагностики ОПП и реализации адекватных терапевтических стратегий.