Инцидент гемоперитонеума после имплантации перитонеального катетера, по данным разных авторов колеблется, от 1 до 23 %.
Наиболее частые причины развития гемоперитонеума у больных на программном перитонеальном диализе могут быть самые различные и включать ретроградную менструацию, овуляцию и разрыв кисты фолопиевых труб, эндометриоз, внематочную беременность, ранение и травмы кровеносного сосуда имплантированным перитонеальным катетером, травмы a. epigastrica во время имплантации перитонеального катететра, коагулопатию [1]. Менее частые и более опасные случаи гемоперитонеума связаны с распадом опухоли или метастазов, раком кишечника или внутриполостной травмой брюшной полости. Более редкие случаи включают панкреатит, перитонеальный склероз, разрыв печеночной капсулы, селезенки или почки, перфорацию толстого кишечника после колоноскопии, перфорацию после облучения опухоли кишки, аневризму внутрибрюшных сосудов [2].
Значительные по объему крови в брюшной полости могут быть при ранении эпигастральной артерии. Эта артерия проходит в прямой мышце живота и не визуализируется при перкутарной технике. При этом методе предлагается использовать ультразвуковое исследование для предотвращения повреждения эпигастральной артерии [3].
При имплантации перитонеального катетера лапароскопическим способом инцидент внутрибрюшного кровотечения составляет до 6 % [4]. Однако эти данные не характеризуют инциденты кровотечения вообще. Анализ, проведенный на 292 больных, которым выполнена открытая хирургическая имплантация перитонеального катетера, показал, что гемоперитонеума в раннем послеоперационном периоде чаще всего возникает среди больных низким гематокритом – ниже 18. Имеет также значение прием антикоагулянтов перед операцией и наличие коагулопатии [5]. Уровень кровотечений может быть ниже при использовании менее агрессивных методик имплантации перитонеального катетера. Из существующих различных методик имплантации перитонеального катетера: открытый хирургический способ, перинеоскопии, лапароскопии, флюороскопический, перкутанная методика по Seldinger; флюороскопический и перкутанный методы считаются наименее травматичными [6]. В двух рандомизированных исследованиях было сравнение открытого хирургического метода и перинеоскопического.
 В обоих методах проанализирована склонность к кровоточивости в послеоперационном периоде. За 10-летний опыт при перинеоскопической имплантации не было эпизодов кровотечения в брюшную полость, а при хирургическом методе отмечено 16 % случаев гемоперитонеума [7]. M.F. Gadallah в своем анализе на 362 больных показал, что лапароскопическая техника менее агрессивна по сравнению с открытым хирургическим. При лапароскопической технике имплантации отмечено 6 % случаев гемоперитонеума, а при хирургическом – 18,7 % [8].
В обоих методах проанализирована склонность к кровоточивости в послеоперационном периоде. За 10-летний опыт при перинеоскопической имплантации не было эпизодов кровотечения в брюшную полость, а при хирургическом методе отмечено 16 % случаев гемоперитонеума [7]. M.F. Gadallah в своем анализе на 362 больных показал, что лапароскопическая техника менее агрессивна по сравнению с открытым хирургическим. При лапароскопической технике имплантации отмечено 6 % случаев гемоперитонеума, а при хирургическом – 18,7 % [8].
Как правило, гемоперитонеум после имплантации перитонеального катетера возникает в раннем послеоперационном периоде. В позднем послеоперационном периоде гемоперитонеум возникает в 1–3 % случаев в связи с развившейся патологией внутренних органов. Случаев массивного кровотечения и образования обширной гематомы у больного на лечении постоянным амбулаторным перитонеальным диализом в литературе мы не встретили. Приводим собственное наблюдение.
Клиническое наблюдение. Больной Б. 71 года, № 17910, пост. 20.09.2010 с диагнозом: хронический диффузный гломерулонефрит, нефрогенная гипертензия, ХБП-V, состояние на лечении перитонеальным диализом с 10.2009. ИБС, стенокардия напряжения II ФК, постинфарктный кардиосклероз, атеросклероз аорты и коронарных артерий.
Впервые изменения в моче – протеинурия, изогипостенурия зафиксированы в 2001 г. С 2004 г. отмечен подъем креатинина крови до 385, мочевины крови до 18,7 ммоль/л. Гипертензия до 180/95 мм рт. ст. Диагностирован хронический диффузный гломерулонефрит. Тогда же у больного диагностирован инфаркт миокарда. С 2009 г. существенное ухудшение состояния больного. Отмечают значительное снижение работоспособности, периодически тошнота, рвота, снижение аппетита. Ухудшение работы почек: Cr крови повысился до 839,5 ммоль/л; Ur крови – до 34,5; К крови – до 5,8; Na крови – до 139 ммоль/л. Fкл – 5,3 мл/мин. По данным эхокардиографии, ФВ составил 57,3 %.
В связи с тем что у больного отягощенный кардиологический анамнез, а именно: ишемическая болезнь сердца, стенокардия напряжения, постинфарктный кардиосклероз, решено лечение терминальной стадии почечной недостаточности начать с перитонеального диализа.
Имплантация перитонеального катетера была выполнена эндоскопическим способом с клепированием 20.09.09.
С 03.10.09 больному проводится лечение перитонеальным диализом по программе 8 литров в сутки, низко- и среднеосмолярные растворы Physioneal (Baxter Healthcare Corp., USA), Nutrineal-содержащий основные незаменимые и ряд заменимых аминокислот (Baxter Healthcare Corp., USA), Extraneal-содержащий высокомолекулярный полимер глюкозы (Baxter Healthcare Corp., USA). Через 10 суток после начала лечения перитонеальным диализом KT/V составил 1,8. Cr крови – 387,3 ммоль/л, Ur крови – 16,2 ммоль/л. Гиперкалиемии нет. Мочи за сутки – до 1200,0 мл.
01.06.2010 со слов жены пациента во время проведения работ на земельном участке больной упал, при этом сильно ударился животом о камень. Кратковременно потерял сознание. Однако при этом к врачам не обращался, т.к. состояние больного полностью нормализовалось. Первые трое суток и в последующем в течение месяца пациент периодически отмечал примесь крови в диализной жидкости. В связи с наличием фибриновых сгустков в перфузате больному внутрибрюшинно вводилось 2500 ЕД раствора гепарина. Со слов больного отмечены периодические боли в брюшной полости, подъем температуры тела. При этом симптомов диализного перитонита не наблюдалось. Периодически отмечено затруднение слива и залива диализной жидкости.
10.10.2010 больной госпитализирован в клинику с явлениями затруднения слива диализной жидкости, умеренными болями в правой половине живота, особенно во время залива диализной жидкости в брюшную полость. Умеренное вздутие брюшной полости. Kt/V при этом составил 1,3. Отмечается повышение Cr крови до 1100 ммоль/л; Ur крови – 34,7; K крови – 5,3 ммоль/л; общий белок – 53 г/л. Заподозрена дислокация перитонеального катетера.
Hb – 63 г/л, L – 14 x 10,9, Ht – 21, СОЭ – 25 мм/ч, CRP – 6 мг/л. Прокальцитонин > 1. Палочкоядерный сдвиг до 14, метамиелоциты – 2, лимфоциты – 11,5, моноциты – 5,5.
Время свертывания – 4,5 минут, время кровотечения – 6,8 минуты.
Коагулограмма от 11.10.10: АЧТВ – 30,06 с, протромбиновая активность по Квику – 112,0 %, МНО – 1,1. тромбиновое время – 25,8 с, фибриноген – 2,61 г/л, Д-димер – 0,71 мкг/мл.
Прокальцитонин крови отр. СРБ – 96.
При рентгенографии брюшной полости перитонеальный катете находится в малом тазу.
Больному имплантирован двухпросветный диализный катетер в v. jagularis и начато лечение гемодиализом.
14.10.10 УЗИ брюшной полости: жидкостной коллектор в правом поддиафрагмальном пространстве, в правом боковом канале и мезогастрии.
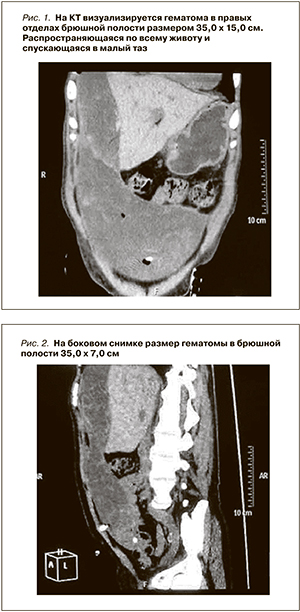
14.10.10 КТ брюшной полости: гематома брюшной полости вдоль наружных отделов печени с распространением вдоль передней брюшной стенки на всем протяжении и спускается в малый таз по правому латеральному каналу. Образование гипоэхогенное, неоднородное. В толще образования к малому тазу определяется завиток перитонеального катетера (рис. 1, 2).
В связи с тем что у больного при обследовании обнаружено жидкостное образование V до 3650 см3 и нарушение работы перитонеального катетера, решено выполнить лапаротомию.
15.10.10 лапаротомия. Ревизия брюшной полости. Удаление гематомы из брюшной полости. В брюшной полости выраженный спаечный процесс, в который вовлечены все петли кишечника. Гематома расположена в правых отделах живота – под передней брюшной стенкой, распространяется от правого поддиафрагмального пространства до малого таза. Возможного источника кровотечения найдено не было. Диффузной кровоточивости не отмечено. Удалено до 2,5 литров старой гематомы и лизированой крови. Учитывая выраженный спаечный процесс в брюшной полости, продолжение ПД признано нецелесообразным. Перитонеальный катетер удален.
Больному перелито 300 мл эритроцитарной массы, 450 мл свежезамороженной плазмы.
С 17.10.10 пациент переведен на лечение гемодиализом. Больному сформирована дистальная артериовенозная фистула. Постепенно состояние больного нормализовалось, и больной выписан на амбулаторное лечение систематическим гемодиализом. Cr крови снизился до 452 ммоль/л, Ur крови – 13,8 ммоль/л. Гиперкалиемии нет.
Коагулограмма: от 15.10.2012. АЧТВ – 33,9 с, протромбиновая активность по Квику – 93 %, МНО – 1,04, тромбиновое время – 23,30 с, Фибриноген плазмы – 7,57 г/л, Активность фактора ХII – 85 %.
Время свертывания крови – 4,4 минуты.
Динамика уровня гемоглобина: Hb – 59 г/л; 61; 64; 74; 92 г/л.
Гематокрит Ht: 18,6 – 29,2; эритроциты – 2,79 х 10,12.
Лейкоцитоз снизился с 15,8 х 10,9 до 10,2 х 10,9; тромбоциты – 257 х 10,9.
Биохимия крови: общий белок – 63 г/л. Альбумин – 34 г/л. Билирубин (общий) – 13,6 ммоль/л. Холестерин общий – 4,2 ммоль/л. АЛТ – 18 ЕД/л. АСТ – 19 ЕД/л. Щелочная фосфатаза – 64 ЕД/л.
В настоящее время состояние больного удовлетворительное, проводится лечение систематическим гемодиализом.
При подозрении на гемоперитонеум необходимо в максимально короткие сроки обследовать больного, т.к. затягивание процесса обследования может приводить к смерти больного от кровотечения. Хотя в нашем случае даже длительное кровотечение в брюшную полость с образованием обширной гематомы не привело к фатальному исходу. Во многих случаях единственным признаком гемоперитонеума является наличие окрашивания кровью диализной жидкости. Возможно даже осветление диализной жидкости, что может быть связано с временным вазоспазмом [9]. Перед имплантацией перитонеального катетера ряд авторов рекомендуют прекратить любую антикоагулянтную терапию – гепарин, варфарин. Использование аспирина может увеличивать риск гемоперитонеума. Тем не менее нет разницы в приеме аспирина для констатации факта кровотечения после имплантации перитонеального катетера [10].
Любой поврежденный кровеносный сосуд может явиться причиной гематомы в брюшной полости как в раннем, так и в позднем послеоперационном периоде. Однако незначительную кровоточивость можно попытаться остановить. После имплантации катетера и при признаках наличия крови в брюшной полости надо ввести в брюшную полость 0,5–1,0 литр холодного раствора. Это может предотвратить незначительную кровоточивость, удалить образующуюся гематому. Обычно 2–3 литров диализного раствора достаточно для ликвидации гематомы. При продолжающемся кровотечении необходимо больного госпитализировать и мониторировать 24 часа. При наличии нестабильной гемодинамики необходимо решение о хирургическом вмешательстве. Переливание крови, криопреципитата может быть использовано, особенно при снижении гематокрита на 30 % от исходного уровня [11]. Кровоточивость из выходного отверстия перитонеального катетера или кожного разреза можно остановить простым наложением давящей повязки.
Наличие крови в брюшной полости представляет опасность для образования тромба кровяными или фибриновыми сгустками в перитонеальном катетере. В связи с чем для продолжения проведения перитонеального диализа предполагается введение через катетер интраперитонеально низких доз гепарина для предотвращения обструкции перитонеального катетера фибриновыми сгустками. Если после операции нет возможности трансфера на гемодиализ, проводить перитонеальный диализ необходимо более часто и малыми объемами диализной жидкости – до 1000 мл [9].
По-видимому, после травмы брюшной полости периодическая незначительная кровоточивость в брюшную полость стабилизировала больного. Тромбы, образующиеся в брюшной полости, периодически закрывали кровоточащие сосуды. Однако наличие гепарина в брюшной полости, который вводился для предотвращения образования фибриновых сгустков, умеренная коагулопатия, которая при этом присутствовала у больного, способствовали продолжению кровоточивости и в конце концов привели к образованию огромной гематомы и нарушению дренажной функции перитонеального катетера в связи с образованием фибриновых тромбов в просвете последнего. Состояние больного оставалось удовлетворительным. Сыграло положительную роль и отсутствие профузного кровотечения. При наличии последнего больной мог бы погибнуть.
Наличие спаечного процесса в брюшной полости есть результат длительного (в течение четырех месяцев) наличия гематомы. Образование фибринозных спаек между кишечником делает проблематичным дальнейшее проведение перитонеального диализа. При ранней эвакуации гематомы из брюшной полости возникновение спаечного процесса маловероятно и продолжение перитонеального диализа возможно, несмотря на лапаротомию. Тем более что и у самого больного был положительный настрой на продолжение перитонеального диализа.



