Введение
На сегодняшний день значительное количество работ посвящено натрийурезу и тубулоинтерстициальной ткани (ТИТ) почек. В структуре поражения почек при артериальной гипертонии (АГ) на сегодняшний день наибольший интерес представляет ТИТ почек, т.к. она наиболее чувствительна к повреждению при повышении артериального давления (АД). Также известно, что у пациентов с измененной ТИТ почек высокий риск развития неблагоприятного профиля АД, таких как «non-dipper» и «night-peaker». В связи с этим представляет интерес поиск новых маркеров почечной дисфункции, например маркеров, связанных с изменением функции ТИТ почек, поскольку у больных гипертонией это сопряжено с нарушениями процесса реабсорбции электролитов, в первую очередь с изменением натрийуреза, и следовательно, профиля артериального давления. Однако рутинное проведение суточного мониторирования АД всем пациентам, имеющим факторы риска, на сегодняшний момент не предоставляется возможным. Также на данный момент не существует общепринятого и доступного скринингового маркера поражения ТИТ почек по сравнению с другими частями нефрона, например с клубочковым аппаратом почки. Одним из наиболее перспективных маркеров для определения неблагоприятного суточного профиля АД и поражения ТИТ почек на сегодняшний день является натрийурез, определенный с помощью кондуктивности (удельной электропроводности) мочи. Включение скринингового метода исследования натрийуреза в план обследования в центрах здоровья позволит на ранних этапах выявлять пациентов с неблагоприятными профилями АД и назначать лечение, направленное на нормализацию натрийуреза, что в свою очередь приведет к замедлению прогрессирования тубулоинтерстициального фиброза и снижению общего сердечно-сосудистого риска.
Цель исследования: установить взаимосвязь изменения натрийуреза, кондуктивности мочи и суточного профиля АД у пациентов с гипертонической болезнью I стадии.
Структура исследования
В исследование включены пациенты, обратившиеся в центр здоровья (база ГБУЗ Москвы ГП № 170 ДЗМ, филиал № 2) для проведения комплексного обследования.
Все пациенты, обратившиеся в центр здоровья, прошли комплексное обследование, в ходе которого выявлены различные факторы риска. Нас интересовали абдоминальное ожирение, гиперхолестериемия, табакокурение. Дополнительно всем пациентам был определен уровень потребления соли. Всем включенным в исследование пациентам (n=375) определен уровень кондуктивности мочи и натрийуреза в однократной порции мочи, собранной в утренние (08.00–10.00), дневные (12.00–14.00) и вечерние (18.00–20.00) часы с целью определения временного интервала «пиков» уровня натрийуреза и кондуктивности мочи.
Критерии включения:
- мужчины и женщины в возрасте от 18 до 60 лет;
- наличие гипертонической болезни 1-й стадии;
- наличие гипертонического анамнеза не более 5 лет;
- наличие факторов риска: абдоминальное ожирение и/или гиперхолестеринемия, и/или табакокурение;
- пациенты, ранее не получавшие медикаментозной терапии;
- потребление соли более 6 г/сут;
- наличие СМАД в течение месяца до включения в исследование.
Критерии невключения:
- мужчины и женщины младше 18 лет и старше 60 лет;
- наличие гипертонического анамнеза более 5 лет;
- наличие 2–3-й стадий гипертонической болезни;
- наличие в анамнезе ХОБЛ, бронхиальной астмы, сахарного диабета, любых заболеваний почек, онкологических заболеваний;
- пациенты, перенесшие инфаркт миокарда, нестабильную стенокардию, чрескожное коронарное вмешательство, сердечную недостаточность, ОНМК или ТИА;
- злоупотребление алкоголем или лекарственными средствами;
- беременность, период лактации.
За период времени с сентября 2013 по сентябрь 2014 г. в центр здоровья обратились 13 805 человек. Из них выявлено здоровых 3724 человека, с функциональными отклонениями – 10 081. Соответствовали критериям включения 568 человек. Всем пациентам, соответствующим критериям включения, была рассчитана СКФ по формуле CKD-EPI. Оказалось, что трое пациентов имели СКФ≤60 мл/мин/1,73 м2. Согласились участвовать в исследовании 375 человек, остальные отказались по различным причинам.

Все пациенты, включенные в исследование, были сопоставимыми по основным клиническим характеристикам (табл. 1). Ни один из пациентов до включения в исследование не получал гипотензивную терапию. Средний возраст пациентов составил 46±8 лет. Женщин, включенных в исследование, было почти в 2,5 больше, чем мужчин. Почти все пациенты имели избыточную массу тела, из них 56% имели абдоминальное ожирение. В рамках комплексного обследования в центре здоровья всем пациентам с помощью экспресс-анализатора определены общий холестерин и глюкоза крови. Обращает на себя внимание довольно высокий уровень холестерина – 6,1±2,1 ммоль/л, учитывая достаточно молодой возраст пациентов, включенных в исследование. «Офисное» АД при амбулаторном измерении в исследуемой группе в среднем составило: систолическое АД (САД) – 144±12,8 мм рт.ст., диастолическое АД (ДАД) – 89±7 мм рт.ст. Анализ результатов СМАД позволил распределить всех включенных пациентов в зависимости от суточного профиля АД на «non-dipper» – 36%, «night-peaker» – 19,2%, «dipper» – 42,4%, «over-dippers» 2,4%.
У включенных в исследование пациентов (n=375) креатинин крови в среднем составил 78±12,2 мкмоль/л, а расчетная СКФ по формуле CKD-EPI – 102±7,2 мл/мин/1,73 м2, таким образом фильтрационная функция почек ни у одного из пациентов не была нарушена.
Методы обследования
Опросник «Charlton: SaltScreener»
Уровень потребления соли определен с помощью опросника «Charlton: SaltScreener» [1]. Опросник предназначен для быстрого определения уровня потребляемой соли: выше или ниже 6 г соли в сутки потребляет пациент. Пациенты отмечали употребляемые ими продукты в течение последней недели, оценка результатов проводилась по балльной системе. При наборе 17 баллов и более считалось, что пациент употребляет более 6 г соли в сутки.
Кондуктометрия мочи
Уровень кондуктивности мочи определен с помощью портативного кондуктометра EC-3. Кондуктометрия – метод физико-химического анализа, основанный на измерении электропроводности растворов и позволяющий определять содержание индивидуального вещества (например, натрия) в растворе простым измерением его электропроводности. Достоинства кондуктометрии: высокая чувствительность (нижняя граница определяемых концентраций ~10–4–10–5 М), достаточно высокая точность (относительная погрешность определения – 0,1–2%), простота методики, доступность аппаратуры.
Используемый прибор калиброван в заводских условиях и не требует калибровки после каждого измерения. Собранную пациентом мочу перемешивали, погружали в нее электрод (нижнюю часть) кондуктометра. Измерения проводили в течение 30 секунд, затем фиксировали результат измерения на дисплее прибора. После каждого измерения электрод промывали дистиллированной водой согласно инструкции. Результат оценивался по таблице соответствия (100 ммоль/л натрия соответствует 12,7 мСм/см кондуктивности мочи).
Натрийурез
Уровень натрийуреза определен с помощью анализатора электролитов EASYLYTE Na/K. EASYLYTE Na/K – полностью автоматизированный ионоселективный анализатор с автокалибровкой и высокоселективными электродами. Достоинства анализатора: точность измерения, простота эксплуатации.
Собранную пациентом мочу перемешивали. Зонд пробы погружали в мочу. Измерения проводились автоматически. Результат измерения отображался на дисплее прибора. После серии измерений прибор промывали согласно инструкции.
Абдоминальное ожирение
Абдоминальное ожирение определено путем измерения окружности талии. Измерения проводили в положении стоя, посередине между краями реберной дуги и гребнями подвздошных костей. Измерительную ленту располагали горизонтально не натягивая. Показания считывали на выдохе. Абдоминальным ожирением считали, если окружность талии более 88 см для женщин и более 102 см – для мужчин [2].

Комплексное обследование центра здоровья
Комплексное обследование в центрах здоровья Москвы включает:
- биоимпедансметр для анализа внутренних сред организма (процентное соотношение воды, мышечной и жировой ткани) с программным обеспечением ABC – 01 «Медасс»;
- комплекс «Здоровье экспресс» – комплекс для оценки уровней психофизиологического и соматического здоровья, резервов организма, параметров физического развития (в основе компьютерный пульт психофизиологической диагностики, компьютерный ростомер, компьютерные весы, компьютерный динамометр);
- система скрининга сердца компьютеризированная (экспресс-оценка состояния сердца по ЭКГ-сигналам от конечностей) «Кардиовизор – 6С» МКС. КС 000001-02;
- аппарат для комплексной детальной оценки функций дыхательной системы (спирометр компьютеризированный) – «Спиро-Спектр»;
- система ангиологического скрининга с автоматическим измерением САД и расчета плече-лодыжечного индекса – Smartdop 30 EX;
- экспресс-анализатор для определения общего холестерина и глюкозы в крови – Ассutrend GC;
- оборудование для определения токсических веществ в биологических средах организма, анализатор окиси углерода выдыхаемого воздуха с определением карбоксигемоглобина, анализатор котинина и других биологических маркеров в крови и моче, пульсоксиметр (оксиметр пульсовой).
Методы статистической обработки материала
Для статистической обработки использовалось программное обеспечение Statistica 10.0. Нормальность распределения проверялась с помошью критерия Шапиро–Уилка и Колмогорова–Смирнова. При изложении результатов пользовались описательными статистиками в зависимости от вида распределения данных. Для количественных переменных использовалось среднее (M) стандартное отклонение (SD) или медиана и 25-я и 75-я процентили. С целью выявления связи факторов между собой были использованы однофакторная и многомерная регрессионная модель, для бинарных данных – логит-регрессионная модель, непараметрический метод ранговой коэффициент-конкордантности Кендалла, непараметрический метод ранговой корреляции Спирмена. Для изучения влияния одного или нескольких факторов на рассматриваемый признак применялся однофакторный и многофакторный дисперсионные анализы. Для решения задач классификации и кластеризации данных использовался модуль Data Mining методом к-средних, k-ближайших соседей (модуль MARSplines). При проверке статистических гипотез нулевую гипотезу отвергали при уровне значимости менее 0,05.

Результаты
Изучение взаимосвязи уровня натрийуреза и кондуктивности мочи
Изучение уровня натрийуреза и кондуктивности мочи показало, что среднее значение у включенных пациентов (n=375) в утренние часы составило 209±103 ммоль/л и 27,06±13,38 мСм/см соответственно; в дневные часы – 230±64,6 ммоль/л и 29,7±8,77 мСм/см соответственно; в вечерние часы – 314±135,2 ммоль/л и 40,4±17,42 мСм/см.
Установлена взаимосвязь уровня кондуктивности мочи и натрийуреза в разовой порции мочи у включенных пациентов (n=375) в различные временные интервалы. Так, в утренней порции мочи корреляция натрийуреза и кондуктивности мочи составила r=0,987, p<0,0001, в дневной порции мочи – r=0,982, p<0,0001, в вечерние часы – r=0,989, p<0,0001. Проверка корреляционной связи между другими порциями дала следующие результаты: натрий утренней порции мочи и кондуктивность дневной продемонстрировали слабую, но достоверную коррекцию (r=0,304 p<0,0001). Другие возможные сочетания не дали каких-либо достоверных зависимостей.
Изучение взаимосвязи суточного профиля АД, уровня натрийуреза и кондуктивности мочи
С целью предполагаемого наличия тесной взаимосвязи суточного профиля АД и уровня экскреции натрия с помощью многомерной статистики была проведена классификация суточного профиля АД в зависимости от уровня кондуктивности
мочи и натрийуреза в разовых порциях мочи. Кластерный анализ с помощью модуля Data Mining выделил 3 кластера, соответствующих трем профилям суточного АД: «non-dipper», «dipper», «night-peaker», выделение в отдельный кластер пациентов с профилем АД «over-dipper» не удалось ввиду их малого числа.
Средние значения уровня натрийуреза и кондуктивности мочи с учетом профиля АД представлены в табл. 2.
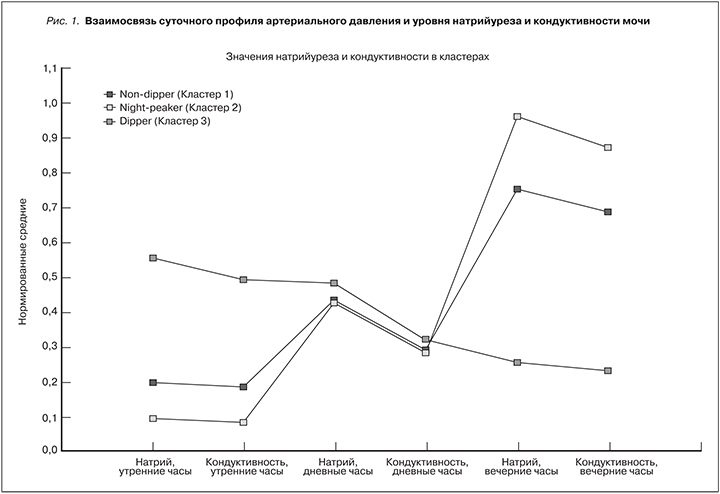
Было показано, что для суточного профиля АД «non-dipper» и «night-peaker» в утренние часы характерны более низкие значения уровня кондуктивности мочи и уровня натрийуреза, затем отмечен их плавный рост в дневные часы, в вечерние часы обращает на себя внимание резкий подъем уровня натрийуреза и кондуктивности мочи («пик»), причем наиболее высокий «пик» выражен в кластере «night-peaker» (рис. 1, табл. 2). Для кластера «dipper» характерна противоположная картина: более высокие значения уровня натрийуреза и кондуктивности мочи определены в утренние часы, «пик» в вечерние часы не наблюдается.
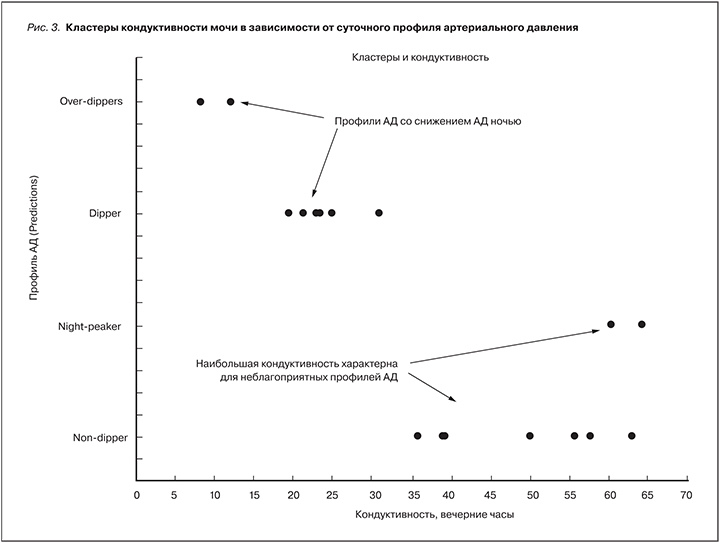
Рис. 2 показывает плотности вероятности возникновения суточного профиля АД «dipper», «non-dipper» и «night-peaker» в зависимости от «пика» уровня натрийуреза и кондуктивности мочи в различных временных интервалах: в утренние и дневные часы «пики» пересекаются и невозможно выделить значимые различия в отличие от вечерних часов, где нет пересечений вероятностей возникновения «пика» экскреции натрия и кондуктивности мочи, что позволяет судить о наибольшей информативности значений уровня кондуктивности мочи и натрийуреза именно вечерней порции мочи. Проверка вероятности возникновения неблагоприятного суточного профиля АД (рис. 2) в зависимости от «пика» экскреции натрия и кондуктивности мочи показала, что при появлении «пика» уровня натрийуреза и кондуктивности мочи в вечерние часы повышается вероятность возникновения суточного профиля АД «night-peaker» (в большей степени) и «non-dipper».
Графическое изображение кластеров, выделенных с помощью метода к-ближайших соседей (рис. 3), также демонстрирует, что для неблагоприятных профилей суточного АД характерно повышение уровня кондуктивности мочи в вечерние часы, тогда как для суточного профиля АД с падением АД ночью, напротив, характерны более низкие значения уровня кондуктивности мочи.
Обсуждение
Работы последних лет подтверждают особую важность нарушения экскреции натрия в формировании неблагоприятного суточного профиля АД. Еще в 1987 г. Dyer в своей работе [3] изучал соотношение дневного к ночному натрийурезу у гипертоников, пациентов с высоким нормальным АД и нормотоников и показал, что экскреция натрия в ночные часы выше у гипертоников, кроме того, этот феномен более значим для пациентов пожилого возраста. В работе Fukuda [4] была показана связь ночного повышения АД с увеличением ночного натрийуреза, который преобладал над дневным у больных, имевших гломерулопатии, кроме того, было показано увеличение экскреции белка в ночные часы. В аспекте почечной патологии представляет интерес работа Lurbe [5], в которой было показано, что неблагоприятный ночной профиль АД приводит к возникновению микроальбуминурии. Похожие данные были получены Perri [6], где в результате 6-летнего наблюдения за пациентами с диабетической нефропатией наиболее значимым предиктором оказалось именно ночное повышение АД. Кроме того, в ряде работ была показана связь формирования неблагоприятного профиля АД с задержкой натрия в дневные часы у пациентов с хронической сердечной недостаточностью (ХСН) [7, 8]. Нарушения натрийуреза, приводящие к изменению суточного профиля АД на более неблагоприятный, предшествуют формированию общепринятых маркеров поражения почек (микроальбуминурия), что может способствовать прогрессированию нефропатии. По-видимому, именно натрийурез, который отражает функциональное состояние ТИТ почек и его циркадное нарушение, наиболее полно может отразить риск возникновения неблагоприятного профиля АД. Существует ряд маркеров, отражающих состояние ТИТ почек, например β2-микроглобулин, ретинол-связывающий белок, белок Тамма–Хорсфалла [9], однако данные маркеры дороги и трудоемки в применении, поэтому в настоящий момент необходим простой маркер, позволяющий скринингово оценить функцию ТИТ почек. Наиболее подходящим является оценка натрийуреза у пациентов с подозрением на поражение ТИТ почек, но это также трудоемкая методика в связи с необходимостью суточного сбора мочи [10]. В исследовании K. Yamamoto [11] оценивал связь между неблагоприятным профилем АД и суточным натрийурезом. Было показано, что для пациентов с профилем АД «non-dipper» и «night-peaker» характерен вечерний «пик» экскреции натрия, наиболее выраженный «пик» был характерен для пациентов, имевших снижение СКФ. В работах, проведенных Fukuda [12, 13], было показано, что изменение «пика» натрийуреза с вечерних часов на более ранние приводит к нормализации суточного профиля АД. В наших ранних работах было показано, что нормализация натрийуреза в целом обладает протективным в отношении ТИТ почек эффектом [14, 15]. В связи с этим актуальным становится выявление натрийуретических «пиков» в вечерние часы как скрининговых маркеров измененного суточного профиля АД. Так, наиболее простым способом выявления изменения натрийуреза является определение кондуктивности мочи, т.е. изменения ее электропроводных свойств, напрямую зависящих от количества электролитов (в основном Na) в растворе. В нашей работе показана высокая корреляция между кондуктивностью и натрийурезом у пациентов с гипертонической болезнью I стадии в утренние, дневные и вечерние часы: r=0,987, r=0,982, r=0,987 соответственно (р<0,0001). Проведенное нами исследование демонстрирует, что определение кондуктивности мочи является скрининговым способом оценки натрийуреза и диагностики суточного профиля АД: повышение уровня кондуктивности мочи и натрийуреза в вечерние часы является маркером неблагоприятного суточного профиля АД «non-dipper», «night-peaker» (кондуктивность в вечерние часы в среднем для «non-dipper» и «night-peaker» составила 50,8 и 62,04 мСм/см соответственно vs 22,8 мСм/см для профиля АД «dipper»).
Таким образом, наше исследование позволяет говорить о следующем: повышение уровня кондуктивности мочи в «вечерние» часы является предиктором возникновения неблагоприятного профиля АД. В связи с эти пациентам с гипертонической болезнью I стадии и повышенным уровнем «вечерней» кондуктивности мочи (более 40 мСм/см) необходимо проведение СМАД с целью выявления неблагоприятных суточных профилей АД («non-dipper», «night-peaker»).



