Введение
Причиной высокой смертности больных хронической болезнью почек (ХБП) сявляются сердечно-сосудистые осложнения, в т.ч. острый инфаркт миокарда (ОИМ), связанные с минеральными и костными нарушениями (МКН-ХБП). МКН-ХБП способствуют развитию кальцификации сосудов, в т.ч. коронарных, гипертрофии и кальцинозу миокарда [1–4]. Гиперфосфатемия, гиперпаратиреоз и снижение уровня кальция – основные факторы развития сердечно-сосудистой кальцификации (ССК). Их значение в летальности от сердечнососудистых осложнений у пациентов с ХБП продемонстрировано во многих исследованиях [4–11). Матриксным белкам, моделирующим кальцификацию, принадлежит важная роль в МКН и развитии ССК. Установлено, что повышение уровня фосфатурического гормона (FGF-23) приводит к повышению риска развития ССК у больных ХБП-5Д, частоты госпитализаций и смерти от сердечно-сосудистых осложнений. А-Клото (А-Klotho), являясь трансмембранным белком, участвует в активации рецептора FGF-23 в органах-мишенях [4, 12–14]. Изучение роли FGF-23 в развитии МКН-ХБП и его влияния на риск развития ОИМ весьма актуально.
Цель исследования: изучить участие FGF-23 во взаимосвязи с показателями минерального обмена, в механизмах развития ОИМ у больных ХБП, получающих заместительную почечную терапию, оценить риск фатальных и нефатальных случаев.
Материал и методы
В течение 3 лет проводилось проспективное когортное исследование 85 больных ХБП 5Д-стадии, получавших лечение программным гемодиализом. Средний возраст составил 56,8±14,8 года. Продолжительность ХБП – 23,2±10,1 года. Лечение гемодиализом проводилось в течение 11,7±6,9 года. Kt/V составил в группе в среднем 1,4±0,08 [15]. Обследование проведено по предварительно утвержденному протоколу, всем больным выполнены рутинные лабораторные и инструментальные исследования, определены показатели, характеризующие МКН: уровни фосфата, кальция крови, паратиреоидного гормона (ПТГ), кальцитириола (1,25(ОН)D), FGF-23 и A-Klotho. Второй этап исследования проведен через 3,1±0,1 года с регистрацией конечных точек, в качестве которых были определены случаи фатального и нефатального ОИМ [15]. Гиперпаратиреоз диагностирован в случае превышения уровня ПТГ>300 пг/мл (исключены первичные формы), гиперфосфатемия – при повышении уровня фосфата >1,49 ммоль/л [16]. Недостаточностью (1,25(ОН)D) считалось снижение его уровня <30 нг/мл. Проведено разделение группы по медиане A-Klotho, составившей 444 пг/мл, и по медиане FGF-23, составившей 63 пг/мл [15]. Статистическая обработка полученных данных проводилась с применением аппарата программы Statistica, 12.6. Использованы стандартные методы описательной статистики, проведен логит-регрессионный анализ с определением χ2-критерия, и при значении р<0,05 результат считался статистически значимым.
Результаты
Средние значения показателей минерально-костного обмена составили: ПТГ – 345±331 пг/мл, FGF-23 – 69,9±24,4 пг/мл, A-Klotho – 443±145 пг/мл, 1,25(ОН)D – 27±8,0 нг/мл, Р – 1,6±0,36 ммоль/л, Са – 2,3±0,32 ммоль/л, Р*Са – 3,8±1,32 ммоль2/л2 [17]. Зарегистрировано 10 случаев ОИМ, из них нефатальных – 6, фатальных – 4. Для выявления связи FGF-23 и других показателей минерально-костного обмена с риском развития ОИМ (все случаи) проведен логит-регрессионный анализ (табл. 1).
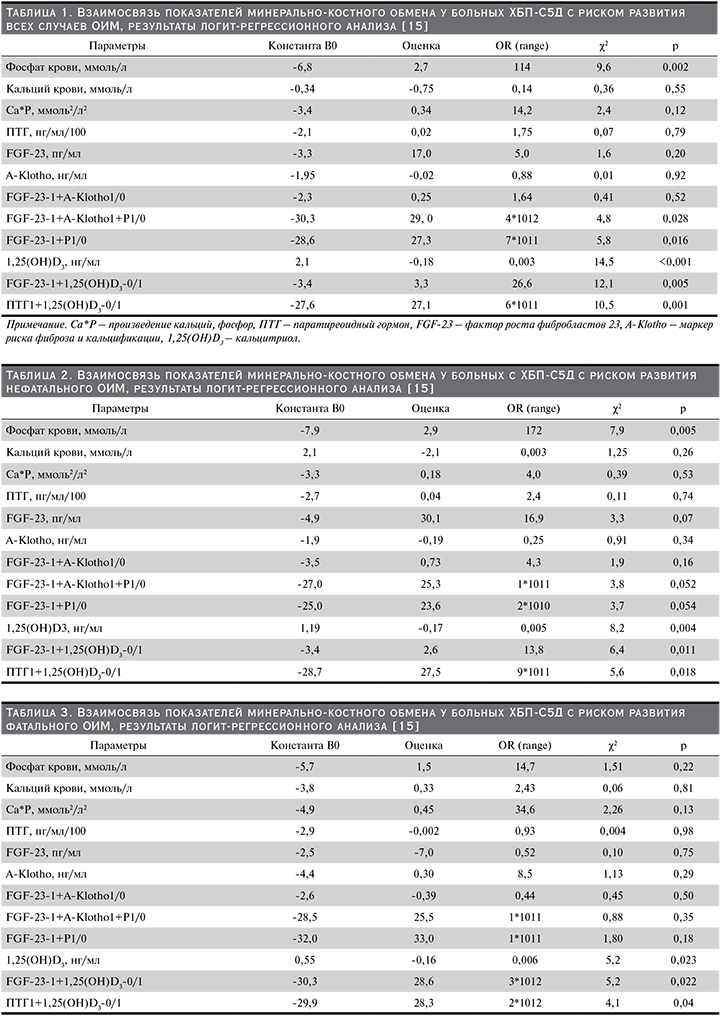
Выявлена достоверная корреляционная связь риска развития ОИМ с уровнем фосфатов крови и 1,25(ОН)D. Статистически значимое влияние на риск ОИМ оказывает как изолированный дефицит 1,25(ОН)D3, так и его сочетание с гиперпаратиреозом (ПТГ1+1,25(ОН)D3-0/1) [15] (табл. 1). Высокие значения FGF-23 и низкие А-Klotho не обладают самостоятельной рисковой активностью в отношении ОИМ. Однако проведенный анализ сочетанного влияния повышенного уровня FGF-23 и низких значений А-Klotho с гиперфосфатемией и дефицитом 1,25(ОН)D3 продемонстрировал достоверно значимое повышение риска развития ОИМ [15] (табл. 1).
Далее был проведен анализ взаимосвязи показателей минерально-костного обмена и случаев нефатального ОИМ (табл. 2). Из табл. 2 следует, что у пациентов с нефатальными случаями ОИМ повышение уровня FGF-23 также демонстрирует прогностическую значимость риска, но только в сочетании с дефицитом 1,25(ОН)D3 (FGF-23-1+1,25(ОН)D3-0/1) [15].
Установлена достоверная статистическая связь риска развития ОИМ в случае изолированной гиперфосфатемии и дефицита витамина D. Гиперпаратиреоз имеет диагностическую значимость только в сочетании с дефицитом витамина D (ПТГ1+1,25(ОН)D3-0/1).
Далее был проведен анализ в отношении фатальных случаев ОИМ (табл. 3). Несмотря на то что их было немного и продолжительность проспективного наблюдения была 3-летней, данный анализ послужил важным инструментом прогнозирования смертельных исходов у больных ОИМ [15].
Из табл. 3 следует, что в отношении фатальных случаев ОИМ приобретает значение дефицит 1,25(ОН)D3, как изолированный, так и в сочетании с повышением уровня FGF-23 (FGF-23-1+1,25(ОН)D3-0/1) [15]. Гиперпаратиреоз также имеет диагностичеcкую значимость в случае фатальных вариантов ОИМ, но только в сочетании с дефицитом витамина D (ПТГ1+1,25(ОН)D3-0/1).
Обсуждение
FGF-23 принадлежит ключевая роль в регуляции фосфорно-кальциевого обмена [4, 12, 14, 18]. В проведенном исследовании высокие значения FGF-23 и низкие А-Klotho не показали самостоятельной рисковой активности в отношении ОИМ [15]. Выявлен повышенный риск развития ОИМ, связанный с гиперфосфатемией, гиперпаратиреозом и дефицитом витамина D. Вместе с тем анализ сочетанного влияния повышенного уровня FGF-23 и /или низких значений А-Klotho с гиперфосфатемией и дефицитом 1,25(ОН)D3 демонстрирует важную роль FGF-23 в механизмах развития ОИМ, достоверно повышая риск развития ОИМ, и подтверждает сложные патофизиологические механизмы МКН-ХБП. Функции FGF-23 многогранны, он не только оказывает фосфатурическое действие через натрий-фосфорный транспортер почечного канальца, но и угнетает 1α-гидроксилазу, приводя к снижению продукции 1,25-дигидроксивитамина D, стимулирует 24-гидроксилазу, приводя к ускоренной деградации активной формы витамина D [19]. FGF-23 напрямую ингибирует секрецию ПТГ [4, 18].
Таким образом, полученные данные подтверждают не только участие FGF-23 в регуляции фосфорно-кальциевого обмена, но и его тесную взаимосвязь с показателями минерально-костного обмена, демонстрируют влияние на риск развития фатального и нефатального ОИМ.
Заключение
FGF-23 – один из ключевых маркеров развития как фатальных, так и нефатальных случаев ОИМ, прогнозирования сердечнососудистого риска у больных ХБП. Заслуживают внимания данные о содружественном влиянии нескольких факторов из числа МКН на риск ОИМ [15].



