Введение
В настоящее время целью лечения пациентов с аксиальными спондилоартритами (СпА) стало достижение ремиссии заболевания или его низкой активности, увеличение продолжительности жизни больных до сопоставимой с общепопуляционным уровнем [1, 2]. Для этого необходимо раннее и длительное применение препаратов. С учетом персистирующего характера воспаления при СпА рекомендовано назначать нестероидные противовоспалительные средства (НПВС) в постоянном режиме и максимально возможных дозах, т.к. постоянный контроль низкой активности заболевания может предотвращать прогрессирование структурных изменений позвоночника [3, 4]. Вместе с тем наряду с высокой активностью заболевания, персистирующим воспалением и дисфункцией эндотелия длительная лекарственная терапия может быть фактором риска поражения почек. В этих условиях все бóльшую актуальность приобретает безопасность лечения пациентов. В последние годы активно изучается безопасность краткосрочного приема лекарств, в то время как информация о длительном применении НПВС малочисленна и разноречива. Поскольку подходы к ведению пациентов с СпА изменились относительно недавно, сведений о безопасности длительного применения НПВС недостаточно.
Таким образом, проблема повреждения почек на фоне длительной лекарственной терапии актуальна в связи с ее малой изученностью и важностью в оценке прогноза жизни пациентов.
Цель настоящего исследования – провести анализ состояния почек у пациентов с СпА, принимающих НПВС постоянно в течение 24 месяцев.
Материал и методы
В исследование были включены 36 пациентов с СпА, ответивших критериям аксиального спондилоартрита Assessment of SpondyloArthritis international Society (2009). Все включенные в исследование пациенты принимали назначенные врачом по месту жительства НПВС в течение 24 месяцев. При этом 11 (30,6%) пациентов принимали нимесулид, 6 (16,7%) – мелоксикам, 10 (27,7%) – диклофенак натрия, 9 (25%) пациентов принимали эторикоксиб. В отношении всех пациентов с СпА собирали биологический материал (сыворотка крови и моча). Выполняли следующие исследования: биохимическое исследование крови с определением креатинина сыворотки крови, биохимическое исследование мочи с определением уровня креатинина мочи по методу Яффе на биохимическом анализаторе «Hitachi 912» с использованием реагентов фирмы «DiaSys»; рассчитывали скорость клубочковой фильтрации (СКФ) по формуле CKD-EPI (Chronic Kidney Disease Epidemiology Collaboration) [5]. На момент вступления в исследование и через 12, 24 месяца постоянного приема НПВС у всех пациентов с СпА определен уровень α1-микроглобулина в моче (аппарат Hitachi 912) с расчетом отношения α1-микроглобулин/креатинин мочи (мг/г); а также уровень альбумина в утренней порции мочи (аппарат Hitachi 912) с расчетом отношения альбумин/креатинин мочи (мг/г). Всем пациентам рассчитывали индекс приема НПВС (индекс ASAS) за последний год.
Из исследования исключили пациентов с заболеваниями мочевыделительной системы (острые и хронические воспалительные заболевания, мочекаменная болезнь, аномалии развития, опухоли, гломерулонефриты, острая и хроническая почечная недостаточность, амилоидоз и др.), с болью в спине травматического, онкогематологического характера, с другими хроническими заболеваниями в стадии обострения (язвенная болезнь, хронический холецистит и др.), пациентов с декомпенсацией хронической сердечной недостаточности (III–IV классы по NYHA) и печеночной недостаточностью, больных онкогематологическими заболеваниями, с инфекциями (в т.ч. лиц, инфицированных вирусами иммунодефицита человека и вирусными гепатитами), беременных.
Статистическая обработка материала проведена с использованием программ Microsoft Office Exсel 2007 (Microsoft Corp., США) и Statistica 8.0 (StatSoft Inc, США). Характер распределения данных оценивали графическим методом и с использованием критерия Шапиро–Уилка. Описание признаков, отличных от нормального распределения, представлено в виде Ме [Q1; Q3], где Me – медиана, Q1 и Q3 – первый и третий квартили. При характере распределения данных, отличном от нормального, применяли непараметрические методы: критерий Манна–Уитни, критерий Вальда–Вольфовица, χ2-критерий, критерий Вилкоксона. Все пациенты подписывали форму информированного согласия на вступление в исследование.
Протокол исследования был одобрен этическим комитетом ФГБОУ ВО «Саратовский ГМУ им. В.И. Разумовского» Минздрава России.
Результаты исследования
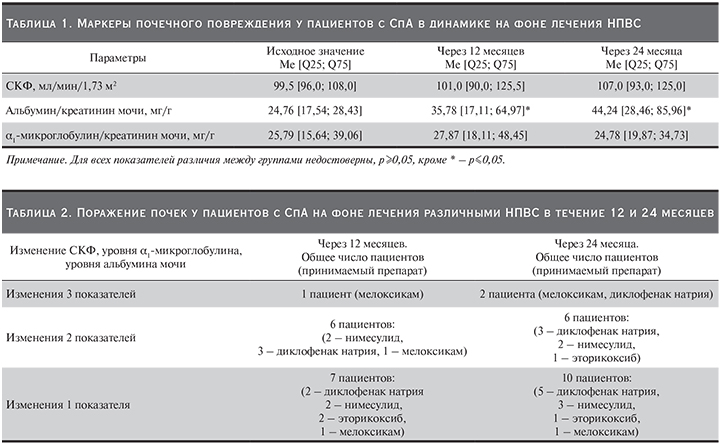
Средний возраст пациентов составил 30 (22–39) лет, длительность заболевания – 8 (5–18), длительность приема НПВС – 7±4,2 года. Пациенты, принимавшие разные НПВС, имели сопоставимую исходную активность СпА и сопоставимый сердечно-сосудистый риск. У пациентов с СпА, включенных в исследование, индекс приема НПВС ASAS составил 75±25,0%. Средняя СКФ у пациентов на момент включения в исследование составила 99,5 (96,0–108,0) мл/мин/1,73 м2, уровень альбуминурии – 24,76 (17,54–28,43) мг/г, уровень α1-микроглобулинурии – 25,79 (15,64–39,06) мг/г.
Через 12 месяцев на фоне терапии НПВС средняя СКФ составила 101,0 (90,0–125,5) мл/мин/1,73 м2 (p≥0,05 по сравнению с исходной), уровень α1-микроглобулина мочи – 27,87 (18,11–48,45) (p≥0,05 относительно исходного), несколько повысился уровень альбумина мочи – 35,78 (17,11–64,97) мг/г (р=0,04 относительно исходного).
Через 12 месяцев терапии НПВС повышение уровня альбумина мочи установлено у 10 (27,8%) пациентов: альбуминурия более 30 мг/г выявлена у 9 (25%), более 300 мг/г – у 1 (2,8%) пациента. Через 12 месяцев терапии снижение СКФ менее 90 мл/мин/1,73 м2 выявлено у 6 (16,7%) пациентов, повышение уровня α1-микроглобулина мочи у 6 (16,7%).
Через 24 месяца терапии на фоне постоянного приема НПВС средняя СКФ составила 107,0 (93,0–125,0) мл/мин/1,73 м2, уровень α1-микроглобулина мочи – 24,78 (19,87–34,73) мг/г (p≥0,05). Отмечено повышение уровня альбумина мочи до 44,24 (28,46–85,96) мг/г (р=0,035 по сравнению со значением альбумина мочи через 12 месяцев лечения). Изменения маркеров почечного повреждения представлены в табл. 1.
Снижение СКФ менее 90 мл/мин/1,73 м2 через 24 месяца терапии выявлено у 8 (22,2%) пациентов. Повышение уровня альбумина мочи установлено у 16 (44,4%) пациентов, у 9 (25%) больных впервые зафиксировано повышение уровня альбумина мочи более 30 мг/г. При этом у 3 (8,3%) пациентов отмечена нормализация уровня альбуминурии. При контрольном исследовании в динамике через 24 месяца лечения уровень α1-микроглобулина мочи оставался повышенным у 4 (11,1%) пациентов.
Через 12 месяцев наблюдения повышение уровней альбумина, α1-микроглобулина мочи, снижение СКФ менее 90 мл/мин/1,73 м2 выявлено у 1 (2,8%) пациента с СпА. Поражение почек по двум любым показателям обнаружено у 6 (16,7%) больных. Повышение уровня альбумина или α1-микроглобулина мочи или снижение СКФ менее 90 мл/мин/1,73 м2 выявлено у 7 (19,4%) пациентов.
Через 24 месяца наблюдения отклонение по всем трем параметрам уставлено у 2 (5,6%) пациентов с СпА. Повышение уровня альбумина или α1-микроглобулина мочи или снижение СКФ менее 90 мл/мин/1,73 м2 выявлено у 10 (27,8%) пациентов. У 7 (19,4%) пациентов определены отклонения по двум параметрам. В целом изменение того или иного параметра зафиксировано у 18 (50%) пациентов. У всех пациентов СКФ соответствовала 1–2 стадиям ХБП.
 Нами проведен анализ маркеров почечного повреждения у пациентов с СпА на фоне приема разных препаратов группы НПВС. В табл. 2 представлена динамика изменения маркеров почечного повреждения в зависимости от принимаемого препарата.
Нами проведен анализ маркеров почечного повреждения у пациентов с СпА на фоне приема разных препаратов группы НПВС. В табл. 2 представлена динамика изменения маркеров почечного повреждения в зависимости от принимаемого препарата.
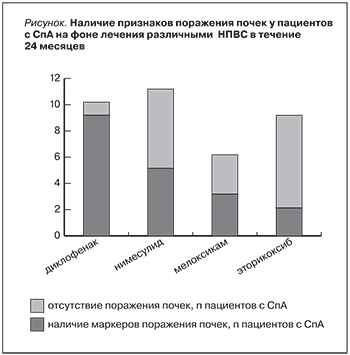
Поражение почек через 24 месяца терапии выявлено у 9 из 10 пациентов с СпА, принимавших диклофенак натрия (р=,01; χ2=6,79; см. рисунок).
В целом изменения изучаемых параметров выявлены у 5 из 11 пациентов на фоне приема нимесулида, у 3 пациентов из 6 – на фоне приема мелоксикама. Наименьшее число пациентов с СпА, у которых зарегистрировано отклонение хотя бы одного параметра, отмечено на фоне приема эторикоксиба у 2 из 9 пациентов (р=0,12; χ2=2,37, для сравнения с нимесулидом и мелоксикамом).
Обсуждение
Сведения о частоте и характере поражения почек у пациентов, получавших НПВС по поводу боли в спине, немногочисленны и не всегда однозначны [6]. Это обусловлено тем, что НПВС-нефропатия в большинстве случаев протекает доброкачественно, тяжелая хроническая почечная недостаточность отмечается редко [7, 8]. В ходе настоящего исследования мы установили, что уровень альбумина мочи является более ранним маркером почечного повреждения. Высокая встречаемость повышения альбуминурии отмечена и в работах других авторов.
Мы оценили состояние почек у пациентов с СпА на фоне приема различных НПВС, т.к. известно, что разные препараты обладают разной нефротоксичностью [9]. В нашем исследовании чаще изменения состояния почек зафиксированы у пациентов, принимавших диклофенак натрия, что согласуется с данными других исследователей [9].
В свете того, что даже субклиническое поражение почек служит фактором сердечно-сосудистого риска, интересны данные Тайского регистра [10]. В этом исследовании, включившем 10 тыс. пациентов с анкилозирующим спондилитом, наблюдавшихся с 1999 г., представлен подробный анализ сердечно-сосудистого риска при лечении НПВС больных анкилозирующим спондилитом [10]. Достоинством исследования стал подробный анализ сердечно-сосудистых событий у больных, получавших НПВС, селективные и неселективные ингибиторы ЦОГ2, анализ вероятности наступления событий при применении высоких и низких доз НПВС, постоянном и редком приеме лекарственных средств. Было показано повышение риска сердечно-сосудистых событий в первые месяцы от начала приема неселективных НПВС. Интересно, что для пациентов, получавших селективные ЦОГ2-ингибиторы, установлено снижение кардиоваскулярного риска в долгосрочной перспективе, что хорошо согласуется с нашими данными о наименьшей нефротоксичности эторикоксиба [10].
Ограничением проведенной работы служит малая численность выборки. Несмотря на это, полученные данные представляют большой клинический интерес, т.к. исследования по изучению состояния почек, в т.ч. ранних маркеров повреждения, у пациентов одной нозологической формы, принимавших в постоянном режиме НПВС в течение 24 месяцев, отсутствуют.
Выводы
На фоне постоянного приема НПВС в течение 24 месяцев у 50% пациентов с СпА выявлены те или иные изменения параметров состояния почек. Наиболее ранним маркером поражения почек является альбуминурия. Поражение почек из всех установленных случаев чаще встречалось у пациентов, принимавших диклофенак натрия.
Заключение
При планировании и проведении длительной терапии НПВС необходим регулярный контроль функции почек, при этом целесообразно оценивать не только СКФ, но и уровень альбуминурии как маркера раннего поражения почек.



