Введение
Множественная миелома (ММ) – многоликое заболевание, поражающее преимущественно людей старшей возрастной группы. Средний возраст вновь заболевших составляет около 70 лет, распространенность заболевания среди населения моложе 40 лет не превышает 2% [1]. Наличие значительного числа различных генетических нарушений обусловливает высокую вариабельность течения болезни. Многие специалисты, включая гематологов, нефрологов, иммунологов, неврологов, ортопедов-травматологов, химиотерапевтов, вовлечены в процесс диагностики и лечения данной патологии [2].
ММ – В-клеточная злокачественная опухоль, морфологическим субстратом которой являются плазматические клетки, продуцирующие моноклональный иммуноглобулин (Ig).
В результате длительной серии генетических событий формируется патологический клон В-клеток, способных к дифференцировке до плазматических, но продуцирующих нефункциональный Ig. Заболеваемость ММ составляет приблизительно 1% среди всех злокачественных опухолей и до 10−15% всех опухолей кроветворной и лимфоидной тканей [1].
Поражение почек при ММ может быть первым или единственным проявлением этого заболевания и служит важнейшим негативным прогностическим фактором, уменьшающим выживаемость пациентов [3]. Основная причина поражения почек при ММ – поражение структур нефрона моноклональными легкими цепями. Наиболее часто (33–57% от всех причин почечной недостаточности) развивается миеломная, или цилиндровая, нефропатия, реже (21%) AL-амилоидоз и болезнь отложения легких цепей (22%) [1]. Иными причинами поражения почек могут также стать острое повреждение почек (ОПП), инфекционные осложнения по причине самой ММ или ее лечения, гиперкальциемия, гиповолемия, сопутствующие заболевания, такие как сахарный диабет (СД) и сердечно-сосудистые заболевания, дегидратация, лекарственное поражение почек [2, 3].
Миеломная, или цилиндровая, нефропатия характеризуется выраженной протеинурией, представленной патологическим белком – свободными легкими цепями (СЛЦ) без развития нефротического синдрома. Она отличается быстропрогрессирующим течением и быстрым (в течение нескольких месяцев) развитием тубулоинтерстициального фиброза [4].
Почечная недостаточность занимает 2-е место среди причин смерти при ММ. Согласно анализу, представленному R.J. Haynes и соавт. [5], в странах Северо-Западной Европы на момент установления диагноза ММ у 29% из наблюдаемых 775 пациентов определялась хроническая болезнь почек (ХБП), 23,4% пациентов начинали лечение у нефролога, т.к. на момент обращения отмечалось повышение уровня сывороточного креатинина [6].
Цель исследования: сравнительный анализ факторов, влияющих на течение и прогноз при ММ в зависимости от вовлеченности почек.
Материал и методы
Ретроспективному анализу были подвергнуты клинико-лабораторные показатели 100 пациентов, прошедших стационарное лечение в гематологическом отделении ГБУЗ СК СККОД за 2020–2022 гг. Исследуемые параметры оценивали на момент постановки диагноза и через 6–12 месяцев проводимой химио-терапии (ХТ).
Пациенты были распределены в две группы: I группа – 50 пациентов с ММ, осложненной поражением почек, II группа – 50 пациентов с ММ без поражения почек.
Согласно классификации B. Durie, S. Salmon, стадийность ММ в I и II группах распределялась следующим образом (табл. 1):
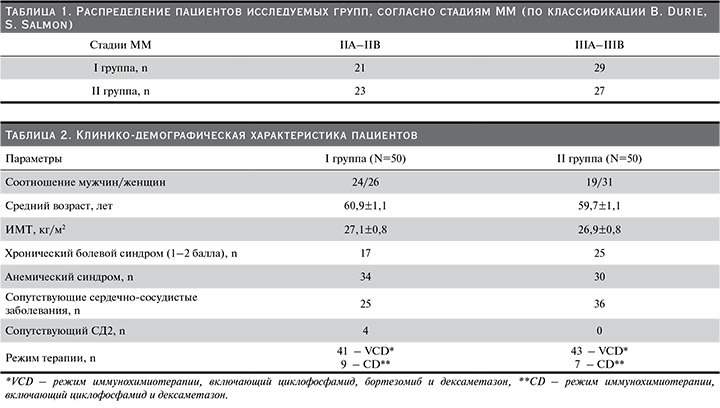
В обеих группах были сопоставимыми средний возраст, соотношение мужчин/женщин, ИМТ тела, схемы лечения ММ (табл. 2).
Следовательно, демографические и конституциональные показатели, схемы лечения не влияли на результаты проведенного исследования. Изучались следующие параметры: продолжительность периода от времени появления жалоб до постановки диагноза; специалист, поставивший предварительный диагноз; результаты инструментальных методов исследования: компьютерной томографии (КТ), рентген-исследования, магнитно-резонансной томографии (МРТ); процент плазматических клеток, тип обнаруживаемых СЛЦ, тип обнаруживаемых Ig, уровень Hb, кальция, общего белка, мочевины, мочевой кислоты, лактатдегидрогеназы (ЛДГ), креатинина в сыворотке крови, расчетной скорости клубочковой фильтрации (рСКФ) в динамике.
Статистическая обработка полученных данных выполнена при помощи программы для персональных компьютеров Statistica for Windows (версия 10,0). Количественные признаки представлены в виде среднеарифметического значения и стандартной ошибки средней (М±m). Достоверность выявленных различий между группами оценивались по t-критерию Стьюдента (в связи с нормальным распределением показателей в выборках). Результаты оценивались как статистически достоверные при t≥2 с вероятностью безошибочного прогноза в 95% (р<0,05), при t≥3 вероятность безошибочного прогноза составляла 99% (р<0,01).
Результаты
В I группе от момента появления жалоб до постановки диагноза прошло в среднем 12,8±2,9 месяца, во II группе – 7,9±1,2 месяца (t=1,5; р>0,05). В основном пациенты попадали на консультацию к гематологу после получения результатов рентген/КТ/МРТ-диагностики, проведенной в связи с болевым синдромом. Также пациентов консультировали терапевты (I группа – 24%, II группа – 20%), нефрологи (10 и 0% соответственно) и неврологи (по 4% в обеих группах).
При первичной постановке диагноза ММ у пациентов обеих групп наблюдались дегенеративно-деструктивные изменения, патологические переломы в одном или более отделах костной системы. Чаще всего подобные изменения выявлялись в грудном (у 35 пациентов I группы и у 30 пациентов II группы) и пояснично-крестцовом отделах позвоночника (у 30 и 29 пациентов соответственно). В целом суммарное поражение различных отделов костной системы у пациентов I группы оказалось несколько выше, чем у пациентов II группы (125 и 107 соответственно, t=1,6; р>0,05).
При изучении миелограмм средний процент плазматических клеток составил 39,9±2,7% в I группе и 27,6±3,1% – во II (t=3; р<0,01).
Полученные нами данные выявленных СЛЦ в двух группах представлены в табл. 3.

Согласно полученным данным, процент пациентов с СЛЦ k в обеих группах был одинаковым. В группе пациентов с поражением почек СЛЦ λ встречались несколько чаще. Кроме того, в нашем исследовании почти у каждого седьмого пациента с ММ без признаков поражения почек СЛЦ вообще не выявлялись.
Тринадцати (26%) пациентам с тяжелой почечной недостаточностью была начата заместительная почечная терапия (ЗПТ) методом гемодиализа. Их средний возраст составил 59,0±1,3 года, мужчины превалировали (м:ж – 9:4). У пациентов данной когорты выявлялись только IgG, частота выявления СЛЦ k или λ составила 61,5 и 30,8% соответственно (р<0,01).
У 68% пациентов I группы и у 60% пациентов II группы на момент постановки диагноза была анемия (Hb – 94,9±3,2 г/л и Hb – 106,2±2,7 г/л соответственно). При динамическом наблюдении выявлено, что у пациентов II группы в ходе терапии уровень Hb повысился и через год составил 125,5±2,6 г/л. В I же группе данный показатель в динамике изменился в меньшей степени: Hb – 109,3±3,3 г/л (t=2,8; р<0,05).
Показатели биохимического анализа крови в двух группах на момент постановки диагноза и через 6–12 месяцев проводимой ХТ, представлены в табл. 4.
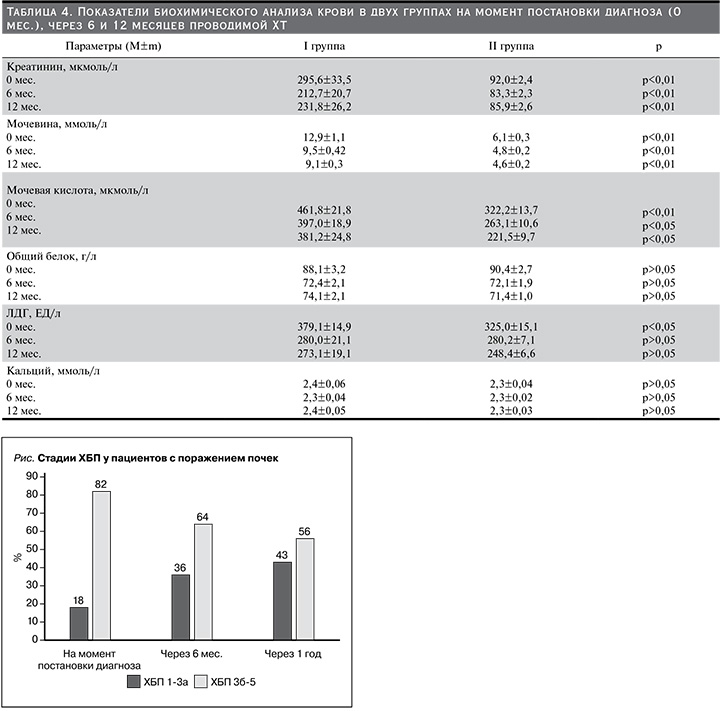
Таким образом, биохимические показатели, характеризующие ММ, такие как общий белок, кальций, были сопоставимыми в обеих группах. Биохимические показатели, характеризующие азотистый обмен, были закономерно выше в I группе и сохранялись таковыми через 6 и 12 месяцев на фоне лечения.
На момент постановки диагноза ХБП С-3б–5 была диагностирована у 82% пациентов I группы, через 6 месяцев – у 64% и через 1 год – у 56% (см. рисунок). рСКФ у пациентов I группы с нарушением функции почек составляла в дебюте заболевания 28,1±2,5 мл/мин/1,73 м2, во II группе – 69,1±2,3 мл/мин/1,73 м2 (t=6,1; р<0,01). В ходе проведенного лечения через 12 месяцев в I группе был получен частичный почечный ответ с повышением рСКФ до 36,0±2,7 мл/мин/1,73 м2. Во II группе через 1 год рСКФ составила 75,6±1,9 мл/мин/1,73 м2. У 37 пациентов I группы наступило улучшение функции почек на фоне проводимой ХТ. Однако 13 (26%) пациентам I группы потребовалось проведение сеансов гемодиализа. Причем 9 (70%) из них диализное лечение начато на момент постановки диагноза. И только у 2 пациентов функция почек улучшилась на фоне лечения, и стало возможным прекращение гемодиализа.
Обсуждение
Проведенное нами исследование направлено на сравнение двух популяций пациентов, одна из которых при прочих равных условиях продемонстрировала поражение почек при ММ, другая – нет.
Известным является факт, что 20–40% пациентов с ММ имеют различную степень поражения почек на момент постановки диагноза и это ассоциируется с высоким риском смерти. Ранняя летальность (в первые 3 месяца) у пациентов с ММ, осложненной почечной недостаточностью, составляет около 30% [7].
Согласно исследованию L.M. Knudsen и соавт., опубликованному в 1994 г., среди 1353 пациентов с впервые выявленной ММ почечная недостаточность присутствовала у 24% пациентов с М-компонентом IgG, у 31% – IgA и у 100% IgD-типа. Частота почечной недостаточности была одинаковой при заболеваниях λ- и k-легких цепей. Кроме того, авторы отметили, что доля пациентов с почечной недостаточностью увеличивается с возрастом [8].
Согласно исследованию О.Н. Писаревской и соавт., в группе пациентов с парапротеинемическими гемобластозами в сочетании с ХБП абсолютное большинство составляли пациенты с наличием IgG k и IgG λ, значительно реже встречались пациенты с секрецией парапротеинов IgD λ, IgA λ, IgA k, IgM k [9].
Судить о степени отрицательного воздействия на почки тех или иных СЛЦ или Ig в нашем исследовании не представилось возможным ввиду недостаточного числа наблюдений. СЛЦ k встречались в двух исследуемых группах с одинаковой частотой, в группе пациентов с поражением почек несколько чаще, чем в группе без поражения почек, встречались СЛЦ λ.
В целом в группе пациентов с поражением почек почти в равном соотношении встречались IgG k, IgG λ, IgA k (38%, 26 и 23% соответственно), значительно меньше IgA λ – 13%. Среди пациентов, которым была начата ЗПТ, выявлялись только IgG, причем СЛЦ k достоверно определялись в 2 раза чаще.
В группе же пациентов без поражения почек значительно превалировали IgG k (57%), а IgG λ, IgA k и IgA λ встречались существенно реже (19%, 12 и 7% соответственно). В группе пациентов с поражением почек несекретирующая миелома встречалась крайне редко.
Согласно полученным данным, уровень плазматических клеток у пациентов с поражением почек был достоверно выше, чем у пациентов без поражения почек. В доступной литературе мы не обнаружили работ по изучению значимости процента плазматических клеток как фактора, указывающего на поражение почек при ММ, однако предполагаем, что это может быть связано с более длительным периодом от дебюта заболевания до постановки диагноза, что, соответственно, с одной стороны, приводит к увеличению объема опухолевой массы, с другой – повышает вероятность поражения почек.
Согласно данным С.С. Бессмельцева, при рентгенологических исследованиях больных ММ костная ткань поражается в 80% случаев [10]. Согласно нашему анализу, у 100% пациентов наблюдались дегенеративно-деструктивные явления в одном или нескольких отделах позвоночника, но у пациентов с поражением почек объем деструктивного поражения позвоночника был больше, что свидетельствовало о более тяжелом течении заболевания.
В нашем исследовании у пациентов с ММ и поражением почек уровень Hb был достоверно ниже. Как известно, наиболее частыми звеньями патогенеза анемии при ММ являются неадекватная продукция эритропоэтина и супрессия эритроидных предшественников. У пациентов с поражением почек в связи с уменьшением массы действующих нефронов прежде всего развивается дефицит эритропоэтина [11].
Cогласно данным F. Rainone и соавт. [12], пациентами с ММ и поражением почек чаще всего являются лица пожилого возраста и мужского пола. Наиболее распространенной формой нарушения функции почек было ОПП. Авторы показали, что ММ с ОПП является более агрессивным заболеванием, связанным с худшими гематологическими показателями и повышенным риском ранней смертности. Из числа пациентов с ОПП, которые нуждались в ЗПТ, 80% она потребовалась в дебюте заболевания. Не было выявлено повышенного риска смерти в когорте, требующей ЗПТ, по сравнению с когортой, не требующей ЗПТ. Согласно выводам, сделанным авторами, почечная недостаточность, ассоциированная с ММ, является неотложным состоянием, требующим быстрой диагностики, начала лечения диализом и специфической терапии.
Согласно данным других авторов, диализное лечение требуется 5% пациентов с патологией почек при ММ, однако восстановление функции почек происходит не более чем в 15% наблюдений [13, 14].
В нашем исследовании диализное лечение потребовалось 13 (26%) пациентам из I группы, причем 9 (~70%) из них на момент постановки диагноза. Преобладали лица мужского пола (9 чел.) ММ с ОПП выявлена у 3 (6%) пациентов.
На фоне проводимой химиотерапии у 78% пациентов I группы был достигнут частичный почечный ответ, что привело к повышению рСКФ, у 22% почечный ответ не получен, и пациенты продолжали ЗПТ методом гемодиализа и только двум пациентам впоследствии удалось прекратить лечение гемодиализом. В то же время, по некоторым данным литературы, у 64% больных удавалось прекратить ЗПТ [4].
Проблема обратимости поражения почек при ММ при использовании стандартных схем лечения широко обсуждается. Так, по данным ряда авторов [4, 15–17], почечный ответ с возможностью прекращения лечения гемодиализом достигается в 38–48% случаев. Почти у половины таких пациентов почечный ответ неполный, а функция почек не восстанавливается в должной степени и соответствует ХБП 4-й стадии [18, 19].
Интересными являются выводы корейских ученых, опубликованные в 2022 г., после ретроспективного изучения ассоциации между функцией почек, протеинурией и риском развития ММ [20]. Согласно их выводам, снижение рСКФ и альбуминурия часто могут быть ранним проявлением моноклональной гаммапатии, что может остаться незамеченным, не получить должной оценки в диагностике ММ на ранних стадиях, что способствовало бы уменьшению поражения органов-мишеней и улучшило бы выживаемость.
В нашем исследовании пациентам, которые развернули поражение почек при ММ, потребовалось больше времени для постановки первичного диагноза (12,8±2,9 месяца) по сравнению с пациентами без патологии почек (7,9±1,2 месяца), р>0,05.
Тот же вывод сделан в исследовании И.Г. Рехтиной и соавт. [21]: «Фактор времени имеет первостепенное значение и во многом определяет успех терапии… От момента диагностики 3-й стадии ОПП с потребностью в диализе до подтверждения диагноза ММ и начала ХТ проходит еще в среднем 43 дня, в течение которых продолжаются повреждения почек».
Выводы
Репрезентативными факторами поражения почек при ММ в проведенном нами исследовании стали продолжительность времени от дебюта заболевания до постановки диагноза, рСКФ на момент постановки диагноза и процент плазматических клеток, полученных в ходе изучения миелограммы.
Пациенты с ММ и поражением почек имели достоверно ниже уровень Hb и чаще деструктивное поражение скелета.
На фоне проводимой ХТ у 78% пациентов был достигнут частичный почечный ответ. Чаще всего почечный ответ не достигался у пациентов мужского пола, уже начавших ЗПТ к моменту постановки диагноза.
Своевременная постановка диагноза ММ позволит избежать тяжелого поражения почек, будет способствовать лучшему почечному ответу и позволит улучшить прогноз заболевания.



