Введение
В настоящее время проблеме взаимосвязи сердечно-сосуди-стой и почечной патологий уделяется все большее внимание. Это неудивительно, т.к. острое или хроническое нарушение функции в одном органе приводит к острой или хронической дисфункции другого, что определяется как кардиоренальный синдром [1]. С учетом роли почек в патогенезе данного синдрома появляются данные о прогностической роли различных маркеров повреждения почек (Cys-C, KIM-1, NGAL и др.), которые используют как изолированно, так и совместно с другими прогностическими шкалами для оценки риска осложненного течения сердечно-сосудистых заболеваний, в т.ч. острого коронарного синдрома (ОКС) [2, 3].
Одним из таких биомаркеров является KIM-1 (kidney injury molecule-1, молекула почечного повреждения-1). KIM-1 отражает преимущественно повреждение проксимальных почечных канальцев, вызванное ишемическими, токсическими, в т.ч. лекарственными, факторами [4]. Ранее в исследованиях доказана возможность применения данного биомаркера для ранней диагностики и прогнозирования острого повреждения почек (ОПП), в т.ч. контраст-индуцированного ОПП (КИ-ОПП). При этом KIM-1 может быть полезен в диагностике субклинического ОПП, подтвержденного гистологическим исследованием, тогда как концентрация сывороточного креатинина (сКр) может оставаться неизменной [3, 5]. В последнее время появляются данные о возможности применения KIM-1 для ранней диагностики и прогнозирования как развития, так и течения не только ОПП, но и хронической болезни почек (ХБП) [6, 7].
В ряде работ была изучена прогностическая роль KIM-1 для выявления пациентов с высоким риском неблагоприятных исходов [3, 8]. В исследовании M.T. Wybraniec и соавт. было показано, что увеличение концентрации данного маркера после селективной коронароангиографии у пациентов со стабильной и нестабильной стенокардией было предиктором наступления комбинированной конечной точки (сердечно-сосудистая смерть, инфаркт миокарда [ИМ], повторная реваскуляризация миокарда или инсульт) в течение 12 месяцев [8].
По данным литературы, KIM-1 выполняет в почках двоякую функцию: с одной стороны, участвует в процессах регенерации и дифференцировки клеток после воздействия повреждающего фактора, с другой – приводит к неконтролируемому ангиогенезу и пролиферации, играя роль фактора канцерогенеза, кроме того, может способствовать метастазированию при онкологических заболеваниях (ОЗ). Повышенная экспрессия данного биомаркера может быть связана с плохим прогнозом у пациентов с ОЗ [9].
По данным литературы, у 3–17% больных ОКС в стационаре выявляют ОЗ [10]. Пациенты с ОКС, имеющие ОЗ, подвержены более высокому риску кардиоваскулярных осложнений (КВО), сердечно-сосудистой смерти и смерти от всех причин по сравнению с больными ОКС без ОЗ [11]. Особый вклад в ухудшение прогноза вносит развитие почечного повреждения [12].
В связи с этим важной задачей является стратификация риска жизнеугрожающих осложнений, что необходимо для выбора дальнейшей тактики ведения этих пациентов, разработки программ реабилитации и вторичной профилактики [13].
В настоящее время у больных ОКС наиболее часто применяемой в клинической практике является шкала GRACE, в т.ч. ее усовершенствованный вариант – GRACE 2.0, которая позволяет прогнозировать риск смерти и/или ИМ в течение первого года, а также вероятность летального исхода (ЛИ) на госпитальном этапе и через 6 месяцев, 1 и 3 года после выписки из стационара [14]. Широкое применение шкалы GRACE у пациентов с ОКС, подвергшихся чрескожному коронарному вмешательству (ЧКВ), остается спорным в связи с тем, что только 26,6% больных, вошедших в когорту регистра «GRACE», было проведено интервенционное лечение. Несмотря на то что данная прогностическая шкала учитывает концентрацию креатинина крови, она остается мало исследованной у пациентов с нарушенной функцией почек, что значимо влияет на прогноз больных после ЧКВ, а также на безопасность и эффективность многих лекарственных препаратов [13]. Кроме того, шкала GRACE не позволяет прогнозировать развитие других ургентных КВО. В связи с этим в последние годы ведутся исследования по улучшению клинической эффективности данной шкалы путем добавления различных предикторов, включая биомаркеры почечного повреждения [2].
В настоящее время сведения о стратификации риска у больных ОКС, имеющих ОЗ, ограниченны, т.к. злокачественное новообразование часто является критерием исключения из многих исследований [15]. В ряде работ показана невысокая прогностическая ценность шкалы GRACE у пациентов этой категории [16, 17]. В связи с этим продолжается создание новых и совершенствование уже существующих прогностических шкал с целью улучшения эффективности прогнозирования неблагоприятных сердечно-сосудистых осложнений [15].
Цель исследования
Разработать эффективный способ прогнозирования ургентных КВО у пациентов с ОКС в сочетании с ОЗ.
Материал и методы
Исследование выполнено на базе регионального сосудистого центра № 2 (Нижний Новгород). В исследование были включены 40 больных ОКС в сочетании с ОЗ (65% мужчин, средний возраст – 69±9 лет). Критерием включения стали ОКС с подъемом или без подъема сегмента ST электрокардиограммы, ОЗ (активное и/или в анамнезе давностью не более 10 лет). Критерии исключения: возраст старше 90 лет, тяжелая печеночная и/или дыхательная недостаточность, раковая кахексия, гипертермия (>38˚С), острое инфекционное заболевание; беременность и/или лактация, психическое расстройство, отказ пациента от включения в исследование (отказ подписать добровольное информированное согласие). Диагностику и лечение пациентов с ОКС проводили согласно действующим клиническим рекомендациям [14, 18].
В нашем исследовании проанализированы данные анамнеза больных ОКС в сочетании с ОЗ. Медиана индекса коморбидности Charlson составила 8 (6; 10) баллов. Все пациенты в анамнезе имели артериальную гипертензию и хроническую сердечную недостаточность I–IV ФК (по результатам теста шестиминутной ходьбы). ИМ ранее был выявлен у 37,5% больных, стабильная стенокардия (II–IV ФК) у 85%, фибрилляция предсердий у 15%, сахарный диабет у 47,5%, анемия у 27,5%. Хроническая болезнь почек (ХБП) при поступлении была у 87,5% пациентов, среди которых 45,7% имели С1–С2-стадии, остальные – С3а–С5-стадии. У 30% пациентов в анамнезе были диагностированы кисты почек, хронический пиелонефрит у 27,5%, диабетическая нефропатия (III–V стадии) у 27,5%, мочекаменная болезнь у 15%; нефрэктомия по поводу рака почки проведена 7,5% больных.
Активное ОЗ имели 37,5% пациентов. Наиболее частыми локализациями опухолевого процесса у больных были молочные железы, предстательная железа, легкие, толстая кишка, мочевой пузырь (70,0%). У 61,5% больных выявили ранние (Т1–2), у 38,5% поздние (Т3–4) стадии опухолевого процесса по системе TNM (tumor, nodus, metastasis). Поражение лимфатических узлов было у 42,5% пациентов, отдаленные метастазы у 17,5%. Ранее было проведено противоопухолевое лечение
92,5% больных. Три пациента не получили специфического лечения вследствие впервые выявленного опухолевого процесса во время индексной госпитализации. При оценке общего
состояния онкологических больных по шкале ECOG 90% пациентов имели 0–1, 10% – 2–3 балла. В нашем исследовании
62,5% пациентов были отнесены к III клинической группе диспансерного наблюдения, 30% к II, 5% к IIa, 2,5% к IV.
Диагноз ХБП и ОПП устанавливали согласно действующим клиническим рекомендациям [19, 20].
При поступлении у 52,5% пациентов был выявлен диагноз ОКС с подъемом сегмента ST электрокардиограммы. После верификации диагноза у 40,0% больных диагностирован ИМ с формированием зубца Q, у 37,5% – ИМ без формирования зубца Q, у 22,5% – нестабильная стенокардия. При поступлении всем исследуемым проводили подсчет числа баллов по шкале GRACE 2.0 с целью стратификации риска развития ИМ и/или летального исхода.
В стационаре 87,5% пациентов проведена селективная коронароангиография. Реперфузионное лечение выполнили 75,0% больных: первичное ЧКВ – 60,0%, фармакоинвазивный подход –
12,5%, тромболитическую терапию без ЧКВ – 2,5% больных.
У 37,5% пациентов при текущей госпитализации развились следующие ургентные КВО: острая сердечная недостаточность (ОСН) (Killip II–IV классы) – 22,5%, рецидив ИМ – 5%, фибрилляция желудочков – 5%, атриовентрикулярная блокада III степени – 5%, тромбоз стента – 2,5%, острая аневризма левого желудочка – 2,5%, острая недостаточность мозгового кровообращения – 2,5%. При этом у 12,5% больных наступил ЛИ. Основным осложнением, приведшим к данному исходу, стала ОСН.
Пациенты с ОКС и ОЗ были разделены на 2 группы: ургентные КВО (n=15) и без ургентных КВО (n=25). Пациенты с ургентными КВО и без данных осложнений были сопоставимыми по полу, возрасту и данным анамнеза. Однако пациенты с ургентными КВО чаще имели ИМ в анамнезе (60 и 20%; p=0,024). Кроме того, у них был выше индекс коморбидности Charlson (9 [7; 13] и 7 [6; 8] баллы; p=0,013). У больных, имевших ургентные КВО, была выше частота активного ОЗ (60 и 24% соответственно; p=0,042). При этом у пациентов с данными осложнениями наиболее частыми локализациями ОЗ были молочные железы, легкие, толстая кишка и матка (суммарно 60%).
В первые сутки госпитализации всем больным проведен забор 10 мл средней порции утренней мочи в пробирки «BD Vacutainer». Пробирки с содержимым доставляли в лабораторию «АВК-Мед» (Нижний Новгород). В лаборатории пробы мочи центрифугировали при 2000 оборотах/мин в течение 5 минут, после чего исследуемые образцы замораживали и хранили при температуре -20◦С не более 10 месяцев. Затем образцы мочи подвергали разморозке и единовременному анализу для определения содержания биомаркера KIM-1 (пг/мл) с помощью тест-системы «ENZoLife Scientifiс КIM-1 ELISA» (США) методом иммуноферментного анализа.
Статистический анализ проведен с использованием специализированных программ: «IBM SPSS Statistics 23», «MedCalc 18.9.1». Правильность распределения количественного признака оценивали при помощи критериев Шапиро–Уилка (n<50). При нормальном распределении количественного признака данные представляли в виде среднего значения и стандартного отклонения (М±SD), при распределении признака, отличного от нормального, – в виде медианы (Ме) и квартилей (Q25; Q75). С целью создания прогностической модели применяли бинарную логистическую регрессию с пошаговым включением количественных и качественных признаков и дальнейшим построением регрессионного уравнения. Для определения диагностической и прогностической значимости, а также выявления оптимального соотношения показателей чувствительности и специфичности применяли ROC-анализ (Receiver Operating Characteristic) с построением ROC-кривой и указанием площади под кривой (AUC). Значимость различий считали при р<0,05 [21].
Результаты
В нашем исследовании была изучена частота и структура ОПП (см. таблицу). У 45% больных ОКС и ОЗ диагностировали ОПП – преимущественно 1-й стадии. У 30% пациентов ОПП было индуцировано применением рентгеноконтрастного препарата (КИ-ОПП). В случае отсутствия информации об уровне сКр за последние 7 дней за исходный сКр принимали «базальный», соответствующий рСКФ 75 мл/мин/1,73 м2 (ОПП по исходному креатинину). Данный вариант ОПП диагностировали у 20% больных, при этом в стационаре у 62,5% из них наблюдали динамику уровня креатинина, соответствовавшую критериям ОПП (ОПП по динамике креатинина) [19].
В нашей работе определено содержание KIM-1 в моче у всех исследуемых. Медиана данного биомаркера составила 921,0 (425,1; 1314,8) пг/мл, что было выше референсных значений, полученных К.Ю. Канукоевым и соавт. при обследовании здоровых лиц [22]. Возможность применения KIM-1 для ранней диагностики ОПП, в т.ч. КИ-ОПП, была исследована нами ранее [23].
В стационаре 12,5% пациентов умерли (у всех высокий риск по шкале GRACE 2.0), у 5% больных диагностировали повторный ИМ (у одного – высокий риск по шкале GRACE 2.0, у другого – средний).
Шкала GRACE 2.0 показала хорошую эффективность в отношении прогнозирования летального исхода и/или ИМ: AUC=0,898 (95% ДИ: 0,761–0,971; p<0,001, >144 б.) В то же время данная шкала продемонстрировала удовлетворительную прогностическую значимость при выявлении пациентов, имевших высокий риск ургентных КВО: AUC=0,775 (95% ДИ: 0,615–0,891; p<0,001, >144 б.). С целью улучшения эффективности прогнозирования ургентных КВО проведена комплексная оценка возможности использования шкалы GRACE 2.0 в сочетании с другими показателями.
Проведен логистический регрессионный анализ с пошаговым включением анамнестических, клинических и лабораторно-инструментальных показателей (n=39) с целью выявления факторов риска развития ургентных КВО в госпитальном периоде у пациентов с ОКС в сочетании с ОЗ.
Выявили две статистически значимые переменные (баллы по шкале GRACE 2.0, величина KIM-1 (пг/мл)
в моче. Построили уравнение логистической регрессии: Y=-14,04813+(0,080005×баллы по шкале GRACE 2.0)+(0,0035426×величина KIM-1 в моче). Переменной «Y» дали название «GRACE 2.0 – KIM-1» (патент № 2751808 от 19.07.2021) [24].
По данным ROC-анализа выявили, что при значении показателя «GRACE 2.0 – KIM-1» >-0,668390598 выше вероятность развития ургентных КВО, а при значении показателя ≤-0,668390598 – ниже. Прогностическая чувствительность модели составила 86,67% (95% ДИ: 59,5–98,3), специфичность – 76,0% (95% ДИ: 54,9–90,6), диагностическая эффективность – 81,34%, отношение правдоподобия для отрицательного результата теста – 0,18 (95% ДИ: 0,05–0,6), для положительного – 3,61 (95% ДИ: 1,7–7,5) AUC=0,872 (95% ДИ: 0,728–0,956; p<0,001).
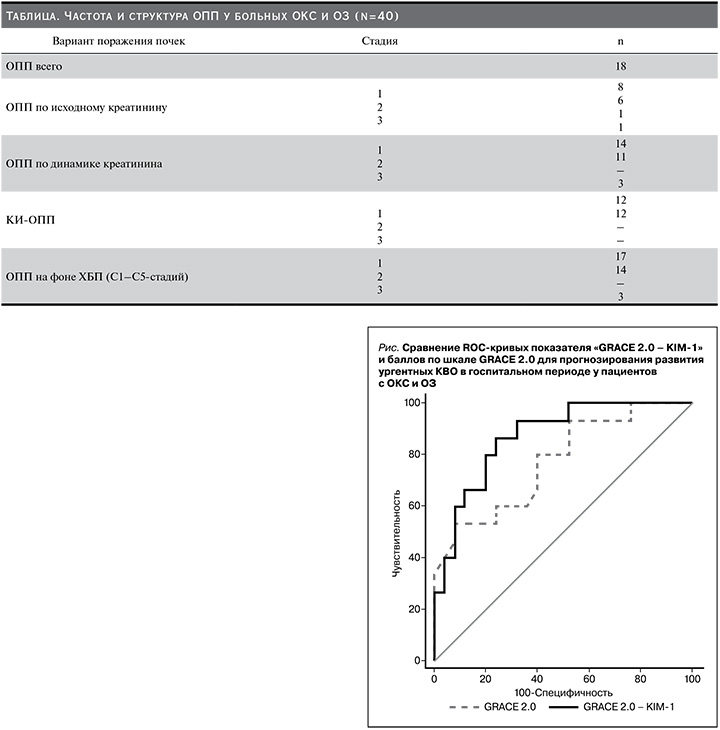
Проведено сравнение ROC-кривых полученного показателя «GRACE 2.0 – KIM-1» и баллов по шкале GRACE 2.0. При этом установили статистически значимые различия между ROC-кривыми (р=0,048) (см. рисунок). Важно отметить, что при совместном использовании уровня KIM-1 дополнительно к баллам по шкале GRACE 2.0 прогностическая значимость полученного показателя «GRACE 2.0 – KIM-1»
в отношении развития ургентных КВО в госпитальном периоде увеличилась на 12,5% по сравнению с применением только баллов по шкале GRACE 2.0. При этом качество модели с использованием общепринятой шкалы GRACE 2.0 было удовлетворительным (интервал AUC – 0,7–0,8), а полученного показателя «GRACE 2.0 – KIM-1» – хорошим (интервал AUC – 0,8–0,9).
Обсуждение
На сегодняшний день, несмотря на улучшение качества оказания медицинской помощи больным ОКС, летальность в России остается высокой – в большей степени при сочетании с ОЗ [25]. В связи с этим становится актуальным вопрос о стратификации риска развития осложнений, в т.ч. ургентных, для улучшения тактики ведения этих пациентов. Как в нашей стране, так и за рубежом имеется достаточное число прогностических шкал, применяемых в отношении больных ОКС. В то же время ни одна из них не обладает высокой эффективностью и не позволяет прогнозировать большинство жизнеугрожающих осложнений, в т.ч. у пациентов с ОЗ [15, 16, 25]. По этой причине в настоящее время продолжаются научные исследования по созданию эффективных прогностических инструментов.
В нашей работе доказано, что прогностическая модель «GRACE 2.0 – KIM-1» у больных ОКС в сочетании с ОЗ может быть использована для оценки вероятности развития ургентных КВО в госпитальном периоде. Добавление значений биомаркера KIM-1 дополнительно к баллам по шкале GRACE 2.0 позволяет повысить эффективность модели на 12,5%. Следует отметить, что данная модель по времени получения результата почти не уступает шкале GRACE 2.0, т.к. для расчета баллов необходимо определить содержание сКр и тропонина, что наряду с оценкой величины KIM-1 может быть выполнено в первые часы госпитализации. По нашему мнению, прогностическая роль KIM-1 в отношении ургентных КВО совместно с другими предикторами, включенными в шкалу GRACE 2.0, связана с формированием кардиоренального континуума у пациентов с ОКС, когда острое сердечно-сосудистое событие ведет к развитию почечного повреждения. В то же время развитие почечной патологии еще в большей степени приводит к повреждению сердечно-сосудистой системы, тем самым замыкая порочный круг [1, 3].
Выводы
В ходе нашей работы показана возможность применения новой шкалы «GRACE 2.0 – KIM-1», которая в совокупности с общеизвестными способами стратификации риска позволяет повышать эффективность прогнозирования ургентных КВО в госпитальном периоде у больных ОКС в сочетании с ОЗ. Не вызывает сомнений, что раннее выявление пациентов, имеющих высокий риск неблагоприятных сердечно-сосудистых событий, позволит своевременно корректировать лечебно-диагностическую тактику и улучшать ближайший и отдаленный прогноз. При этом необходимо проведение дальнейших исследований по изучению данной проблемы.



