Обоснование
Несмотря на очевидные достижения в диагностике и лечении заболеваний и состояний, связанных с хронической болезнью почек (ХБП), ее распространенность продолжает расти и, по последним данным, достигает 13,4% [1, 2]. В среднем ежегодный прирост пациентов, имеющих ХБП, во всем мире составляет 7%, в Российской Федерации – 10% [3]. При этом значимое влияние на инвалидность и смертность таких пациентов оказывает спектр системных осложнений, ассоциированный с неуклонным угасанием почечной функции. Артериальная гипертензия и связанные с ней сердечно-сосудистые заболевания (ССЗ), гипоальбуминемия, анемия, гиперкалиемия, метаболический ацидоз, дефицит 25(OH)D и минерально-костные нарушений (МКН) напрямую влияют не только на качество, но и на продолжительность жизни пациентов с ХБП [4]. Одним из широко распространенных осложнений, ярких, с точки зрения, клинических проявлений и наиболее тяжелым по течению является вторичный гиперпаратиреоз (ВГПТ). Биохимические отклонения, характеризующиеся избыточной секрецией паратиреоидного гормона (ПТГ) и развивающейся в ответ на хроническую гипокальциемию, представляют собой неотъемлемую часть ВГПТ при ХБП [5, 6]. При этом уже при начальных стадиях ХБП продукция ПТГ повышается, в то время как уровни кальция и фосфора остаются в пределах референсных значений. Мониторинг показателей кальций-фосфорного гомеостаза рекомендован в клинических практических рекомендациях KDIGO (2017), начиная со стадии ХБП С3a [7]. При этом некоторые обсервационные исследования [8–10] у пациентов с недиализной стадией ХБП предполагают, что наличие ВГПТ напрямую связано не только с патологией минерального и костного обменов, но и с повышенным риском прогрессирования ХБП, ССЗ и смертностью.
Целью настоящего исследования является оценка клинико-лабораторных особенностей ВГПТ на фоне ХБП на территории Тюменской области.
Материал и методы
В исследование были включены 416 историй болезни пациентов с ХБП С3–С5 (до начала проведения заместительной почечной терапии) и ВГПТ, которые находились на обследовании и лечении в нефрологическом отделении ГБУЗ ТО «Областная клиническая больница №1» г. Тюмени в период с 01.01.2018 по 31.12.2022, исключая период перепрофилирования отделения в моноинфекционный госпиталь по оказанию помощи больным новой коронавирусной инфекцией COVID-19 (с 03.2020 по 05.2022)
Критериями включения в исследование были: возраст не менее 18 лет, ХБП С3–С5 и ВГПТ на момент поступления в стационар, отсутствие приема витамина D по данным истории болезни. Стадия ХБП, альбуминурии и ВГПТ выставлена в соответствии с утвержденными клиническими рекомендациями по ХБП (2023) [1].
Критерии исключения: возраст до 18 лет, пациенты с диагнозами ХБП С1–С2, первичный и третичный гиперпаратиреоз.
Проведено одноцентровое сплошное ретроспективное неконтролируемое неинтервенционное поперечное исследование с использованием данных из историй болезни.
Сбор данных историй болезни осуществлялся согласно единому протоколу (сбор жалоб, анамнеза основного заболевания и сопутствующей патологии, анамнеза жизни, данных физикального обследования с измерением роста, массы тела и расчетом индекса массы тела – ИМТ). Лабораторные исследования проводили по стандартным методикам в центральной лаборатории ГБУЗ ТО «Областная клиническая больница №1» г. Тюмени на биохимическом анализаторе (Roshe HITACHI cobas 6000). Из лабораторных методов оценивали уровень общего кальция (референсные значения 2,25–2,75 ммоль/л), общего белка (референсные значения 65–85 г/л), альбумина (референсные значения 35–53 г/л), паратиреоидного гормона – ПТГ (референсные значения 15–65 пг/мл), ионизированного кальция (референсные значения 1,16–1,32 ммоль/л), фосфора (референсные значения0,8–1,45 ммоль/л), 25(OH)D (референсные значения 75–250 нмоль/л), креатинина (референсные значения 44–80 мкмоль/л для женщин, 74–110 мкмоль/л для мужчин), щелочная фосфатаза – ЩФ (референсные значения 44–147 Ед/л). Инструментальные методы диагностики включали в себя: эхокардиографию – Эхо-КГ (Philips EPIQ 5), ультразвуковое исследование (УЗИ) почек и забрюшинного пространства (General electric Logiq P9). При проведении Эхо-КГ определяли массу миокарда левого желудочка (ЛЖ), индекс массы миокарда ЛЖ, толщину задней стенки ЛЖ и межжелудочковой перегородки, конечный диастолический размер, конечный систолический размер. Рассчитывали систолическое давление в легочной артерии (СДЛА). При УЗИ почек оценивали форму, размеры, подвижность и положение органа, а также структуру паренхимы и чашечно-лоханочной системы.
Статистическую обработку полученных данных проводили с использованием пакета статистической программы Microsoft Office Excel 2010, версия: 14.0.4760.1000 (64-разрядная). Оценку нормальности распределения количественных признаков проводили с использованием теста Колмогорова–Смирнова. Среднее значение обозначалось с указанием стандартного отклонения (M±SD). Для сравнения двух независимых групп использовали параметрический t-критерий Стьюдента. Статистически значимым считался критерий при р<0,05.
В соответствии с приказом Департамента здравоохранения Тюменской области от 16 августа 2018 г. №20/15 маршрутизация пациентов с ХБП (код по МКБ-10: N18.3–N18.5) для обследования и лечения осуществлялся в нефрологическом отделении ГБУЗ ТО «Областная клиническая больница №1» г. Тюмени. Для настоящего исследования были отобраны 416 пациентов с установленным диагнозом ХБП С3–С5 и имеющие МКН, классифицируемые, как вторичный гиперпаратиреоз (код по МКБ-10: Е21.1). Пациенты, поступившие в экстренном порядке с урологической патологией и переведенные в профильный стационар, в исследование не включались: один пациент с раком мочевого пузыря, один пациент с раком предстательной железы, а также трое пациентов с уретерогидронефрозом.
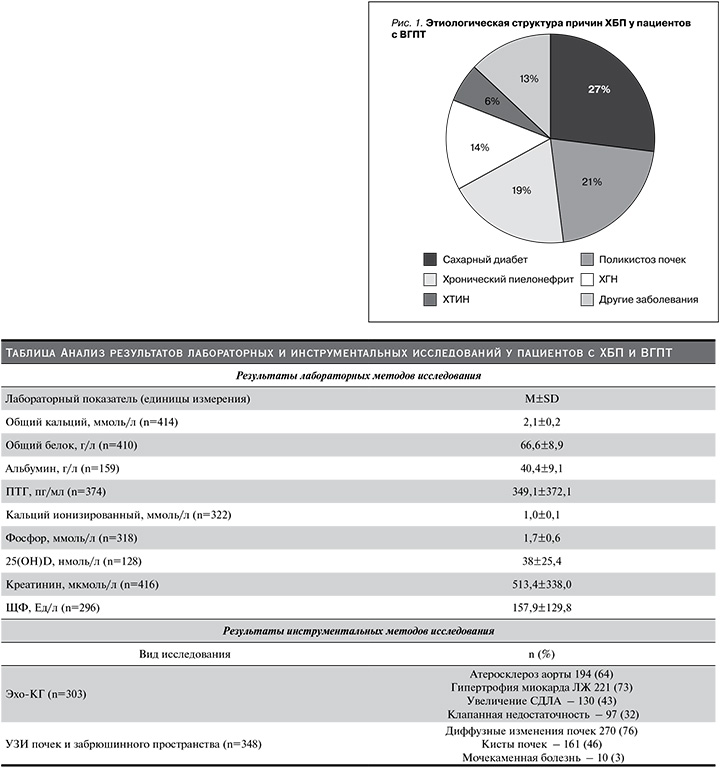
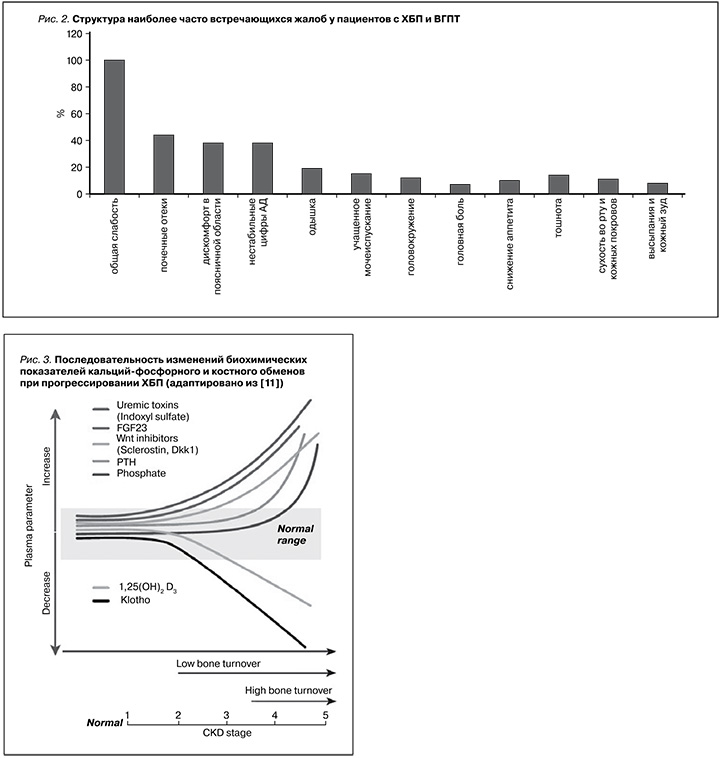
Из общего числа отобранных пациентов 184 (44,2%) составили мужчины и 232 (55,8%) женщины. Средний возраст обследуемых составил 56,7±14,02 года. Длительность ХБП в среднем составила 3,5±4,3 года. У 123 обследуемых пациентов было проведено исследование росто-весовых показателей с расчетом ИМТ. Нормальную массу тела имели 20% пациентов, 2% – дефицит массы тела, 18,7% – избыточную массу тела, у 30,1% ИМТ соответствовал ожирению I степени, у 15,4% регистрировалось ожирение II степени, 13,8% – ожирение III степени. Средний ИМТ составил 31,7 кг/м2, что соответствует ожирению I степени. По этиологической структуре ХБП среди всех пациентов лидирующую позицию занимали первичные заболевания почек, в т.ч.: поликистоз почек – 21%, хронический гломерулонефрит – 14%, хронический пиелонефрит – 19%, хронические тубулоинтерстициальные нефриты – 6%. Второе место приходилось на больных сахарным диабетом – 27%. Остальные 13% составили такие заболевания, как системный васкулит, ишемическая болезнь почек, злокачественные новообразования почек, подагрическая нефропатия, системная красная волчанка, ВИЧ-инфекция (рис. 1). Жалобы пациентов при поступлении с ХБП и ВГПТ представлены на рис. 2. Из сопутствующей патологии чаще всего встречались заболевания сердечно-сосудистой системы (ССС) в виде артериальной гипертензии – 387 (93%) и ишемической болезни сердца – 110 (27%), в меньшем проценте случаев инфекции мочевыводящих путей – 31 (10%), нарушения ритма сердца – 26 (9%), мочекаменная болезнь – 14 (7%), последствия острого нарушения мозгового кровообращения – 13 (4%). Наиболее часто встречающимися осложнениями у исследуемых являлись анемия – 322 (77%), гиперурикемия – 119 (29%).
Результаты
Анализ лабораторных показателей обследуемых пациентов подтвердил наличие классического течения ВГТП у пациентов с ХБП: выявлено повышение среднего уровня ПТГ в 5,3 раза, сывороточного креатинина в 6,5 раза, а также незначительное увеличение показателей фосфора и ЩФ по сравнению с референсными показателями. Средние значения ПТГ составили 349,1±372,1 пг/мл (15–65 пг/мл), общего кальция 2,1±0,2 ммоль/л (2,25–2,75 ммоль/л), кальция ионизированного 1,0±0,1 ммоль/л (1,16–1,32 ммоль/л), фосфора 1,7±0,6 ммоль/л (0,8–1,45 ммоль/л), креатинина 513,4±338,0 мкмоль/л (44–80 мкмоль/л для женщин, 74–110 мкмоль/л для мужчин), ЩФ 157,9±129,8 Ед/л (44–147 Ед/л). Из общего числа обследуемых уровень 25(OH)D определяли у 128 пациентов, который в среднем составил 38±25,4 нмоль/л (75–250 нмоль/л), что соответствует дефициту витамина D. При проведении Эхо-КГ наиболее часто встречались атеросклероз аорты и гипертрофия миокарда ЛЖ. При выполнении УЗИ почек и забрюшинного пространства – диффузные изменения почек (см. таблицу).
Обсуждение
ХБП тесно ассоциирована с патологией минерального и костного обменов. Согласно этой концепции, МКН при ХБП проявляются либо ВГПТ в виде комбинации нескольких биохимических отклонений (кальция, фосфора, ПТГ и витамина D), либо костными аномалиями (аномальный обмен костной ткани, минерализация, объем или линейный рост), либо кальцификацией сосудов и других мягких тканей или сочетанием нескольких патологических состояний [7]. В структуре осложнений ХБП ВГПТ занимает одну из ведущих позиций и напрямую связан с прогрессированием ренальной дисфункции [11] (рис. 3). По данным крупнейшего обсервационного исследования DOPPS (Dialysis Outcomes and Practice Pattern Study), в котором проанализированы данные более чем 35 000 пациентов с ХБП, практически во всех странах мира с 1996 г. до настоящего времени число пациентов, имеющих повышенный уровень ПТГ, неуклонно растет [12]. Кроме этого, по результатам когортного исследования продемонстрировано, что нарушения минерального обмена зачастую развиваются за 5 лет до терминальной почечной недостаточности, начиная со стадии ХБП C3а [13], что нашло отражение и в проведенном исследовании. Гиперпаратиреоз связан с повышенным риском повреждений ССС, в особенности у пациентов с ХБП [14]. Гипертрофия миокарда ЛЖ является наиболее частой патологией сердца у пациентов с ХБП [15]. По оценкам экспертов ее распространенность составляет от 16 до 31% у лиц со скоростью клубочковой фильтрации >30 мл/мин, с возрастанием до 60–75% до начала заместительной почечной терапии и до 90% после начала диализа [16]. Это связано с хронической перегрузкой объемом и давлением, нейрогормональной активацией и накоплением уремических токсинов [17]. Кроме этого исследования показали наличие рецепторов к ПТГ в ССС, например в кардиомиоцитах, гладко-мышечных и эндотелиальных клетках [14], что подтверждает тот факт, что прогрессивная секреция ПТГ может влиять на состояние ССС, включая индукцию апоптоза в кардиомиоцитах, активацию сердечных фибробластов, вызывающую интерстициальный фиброз, утолщение артериол миокарда и повышение эндотелиальной экспрессии молекулярных маркеров атеросклероза [18], таких как интерлейкин-6. Однако более убедительные доказательства причинной роли ПТГ в патогенезе ССЗ до сих пор отсутствуют. Фактически, снижение уровня ПТГ может параллельно вызывать снижение других факторов (например, фактора роста фибробластов 23 типа – FGF-23), которые сами по себе способствуют увеличению ССЗ и смертности [19].
Заключение
Таким образом, проведенное исследование показало, что ВГПТ у наблюдаемых пациентов с ХБП характеризуется значительным увеличением уровня ПТГ (более чем в 5 раз), активности ЩФ (более чем в 3,5 раза), а также низким содержанием витамина D (почти в 2 раза) на фоне изменений со стороны ССС (гипертрофия миокарда ЛЖ и атеросклероз аорты), что необходимо учитывать при диагностическом обследовании и определении тактики лечебных и профилактических мероприятий у таких пациентов.



