Введение
В настоящее время наблюдается неуклонный рост числа операций по трансплантации почки, что связано с увеличением числа больных терминальной хронической почечной недостаточностью (ТХПН) и развитием технических возможностей выполнения подобных операций [1–4]. Очевидно, что трансплантация почки служит наиболее эффективным методом лечения (ТХПН) [3, 5]. Заместительная почечная терапия (гемодиализ, перитонеальный диализ и трансплантация почки) существенно продлевает жизнь пациентов с ТХПН [2, 6]. Функциональное состояние и адаптационные резервы пациентов с ТПХН зависят как от особенностей течения самой болезни, так и от типа заместительной терапии. Пациенты вынуждены длительное время находиться на диализе до трансплантации, а нередко и пожизненно. Трансплантация почки является главным методом лечения ТХПН при условии выживания трансплантата, а также обеспечивает лучший реабилитационный прогноз [5]. Анализ функционального состояния и адаптационных резервов организма подтверждает необходимость трансплантации, количественно определяет реабилитационный потенциал и позволяет объективно оценивать эффективность предложенной программы физической реабилитации [7].
После трансплантации органа можно вести активный образ жизни, заниматься физической культурой и спортом [8–10]. Об этом свидетельствуют Всемирные игры людей с трансплантированными органами, которые проводятся с 1978 г. по настоящее время [11, 12].
Физические нагрузки широко используются при реабилитации пациентов с заболеваниями сердечно-сосудистой, дыхательной, нервной систем, при метаболическом синдроме. Реципиенты с донорской почкой относятся к группе риска многих из этих состояний, что диктует необходимость развития в трансплантологии реабилитационных технологий на основе ЛФК [11, 13]. Однако в настоящее время нет единой точки зрения на программу реабилитации таких больных, не разработана система индивидуальных занятий ЛФК, не выработаны критерии допуска к занятиям физкультурой и спортом, не установлены объем и интенсивность физических нагрузок в различные сроки после трансплантации.
 Разработка комплексной программы обследования на основании оценки функционального состояния и адаптационных резервов организма, по результатам которой формируется индивидуальная программа реабилитации реципиентов с донорской почкой, актуальна и пока не вполне решенная проблема.
Разработка комплексной программы обследования на основании оценки функционального состояния и адаптационных резервов организма, по результатам которой формируется индивидуальная программа реабилитации реципиентов с донорской почкой, актуальна и пока не вполне решенная проблема.
В работе была поставлена цель изучить влияние физической активности на функциональное состояние и адаптационные резервы организма пациентов после трансплантации почки в разные периоды лечения (до трансплантации, через 1, 3, 6 месяцев и через год после трансплантации).
Материал и методы исследования
Проведен анализ результатов обследования и лечения 57 пациентов от 20 до 57 лет (в среднем 35 ± 9,65 года; 25 женщин, 32 мужчины), перенесших трансплантацию почки в 2011–2013 гг. с удовлетворительной функцией трансплантата. Из них на гемодиализе находились 75,5 %, на перитонеальном диализе – 24,5 % больных; сроки диализа составили от 2 месяцев до 5,5 лет, в среднем 24 ± 1,5 месяца до операции. Причиной трансплантации почки во всех случаях стала ТХПН в исходе следующих заболеваний: хронический гломерулонефрит – 65,5 %, хронический пиелонефрит – 19,6 %, другие причины – 14,9 %.
Характер трансплантата: от трупного донора – 59,6 %, от родственного донора – 40,4 %. В зависимости от программ физической реабилитации выделено 2 группы больных. Группу I составили 30 человек (13 женщин и 17 мужчин) в возрасте 21–55 (35,6 ± 9,9) лет, которые проходили все 3 этапа физической реабилитации. Группа II – 27 пациентов (12 женщин и 15 мужчин) в возрасте 20–57 (34,4 ± 9,4) лет, которым реализовывали только программу медицинской реабилитации 1-го этапа.
В III группу объединили 30 относительно здоровых человек (15 женщин и 15 мужчин), не нуждающихся в трансплантации органа, в возрасте 19–56 (33,7 ± 8,7) лет, ведущих обычный образ жизни, не занимающихся спортом и фитнессом. Группы I и II были сопоставимыми по полу, возрасту, причинам ТХПН, длительности нахождения на заместительной почечной терапии до операции и функции трансплантата.
Разработанный алгоритм физической реабилитации после операции включал два этапа.
I этап – ранний послеоперационный. На этом этапе реабилитации мы выделили два подпериода: 1-е сутки после операции, в отделении реанимации, и первые 3 месяца после операции. Цели ЛФК на этом этапе: профилактика ранних и поздних послеоперационных осложнений (пневмония, ателектаз легкого, атония кишечника, тромбоэмболические осложнения и т. д.); улучшение деятельности сердечно-сосудистой и дыхательной систем, психоэмоционального состояния больного; профилактика спаечного процесса; формирование эластичного подвижного рубца. Первый подпериод: 1-е сутки реабилитации прошли в отделении интенсивной терапии и включали дыхательную гимнастику, постуральный дренаж, раннюю активацию больного. Второй подпериод: в палате в течение первой недели пациент занимался ЛФК под контролем врача по специально разработанной программе, которая включала различные упражнения для мышц конечностей с чередованием дыхательной гимнастики в положении лежа. Затем по мере готовности пациента со второй недели добавляли упражнения в положении сидя на стуле с дозированной ходьбой. В течение следующих недель увеличивали интенсивность нагрузки в соответствии с самочувствием пациента. После выписки пациенту рекомендовали комплекс общеукрепляющих упражнений для самостоятельного выполнения дома и рекомендации по дозированной ходьбе.
II этап – поздний послеоперационный период. Сроки – от 3 месяцев до года. Цели ЛФК в этом периоде: улучшение жизненно важных функций организма (кровообращения, дыхания, пищеварения); ослабление побочных эффектов иммуносупрессивной терапии; профилактика остеопороза; укрепление мышц брюшного пресса, профилактика нарушений осанки; адаптация всех систем организма к возрастающей физической нагрузке; повышение психического компонента здоровья и качества жизни. На этом этапе применены упражнения, способствующие укреплению мышц спины и живота, суставная гимнастика, общеукрепляющие упражнения для мышц рук и ног, дозированная ходьба – 30 минут ежедневно или 1 час через день в среднем темпе.
Во всех периодах физическую нагрузку дозировали с помощью шкалы индивидуального восприятия нагрузки Борга, основанной на собственном восприятии физических ощущений человека во время нагрузки. В шкале Борга 20 баллов: 0 и 1 – полное отсутствие нагрузки, а 19–20 – максимальное, практически запредельное напряжение. Пациентам в первые 2 подпериода рекомендованы начальные нагрузки от 6 до 12 баллов, а на II этапе в соответствии с тренированностью больного можно было увеличивать нагрузки до среднего уровня (12–16 баллов).
До операции, через 1, 3, 6 и 12 месяцев после трансплантации оценивали функциональное состояние и адаптационные резервы организма пациентов I и II групп с помощью аппаратно-программного комплекса (АПК) «Истоки здоровья» (Св. РОСПАТЕНТ № 2004610012 от 05.01.2004). Для сравнения была также протестирована III группа.
АПК «Истоки здоровья» представляет собой комплексную программу тестирования для оценки функциональных и адаптационных резервов организма [14]. Входящие в состав АПК диагностические тесты общепризнанны и широко применяются в функциональной диагностике: проба PWC-170 позволяет оценивать физическую работоспособность, определять фактическое и должное максимальное потребление кислорода, характеризующее аэробную производительность и функциональные резервы кислородтранспортной системы организма; тест вариационной пульсометрии – высокоэффективный метод исследования системы нейрогуморальной регуляции, оценки на этой основе текущего функционального состояния и адаптационных резервов организма; тест зрительно-моторной реакции, позволяющий оценивать функциональное состояние центральной нервной системы по показателям возбудимости, реактивности и устойчивости реагирования; тест физических возможностей, по Г.Л. Апанасенко, является известным экспресс-методом количественной оценки физического здоровья; тест общей реактивности (по Л.Х. Гаркави и соавт.), основанный на тесной связи психофизиологического состояния человека с общей неспецифической адаптационной реакцией, которая позволяет определять тип и уровень адаптивных реакций организма; блок тестов для оценки психоэмоционального состояния человека используется для характеристики уровня тревожности, эмоциональной стабильности и стрессоустойчивости. Результатом тестирования служит комплексная оценка резервов здоровья – «интегральный показатель здоровья» (ИПЗ), который вычисляется как производная величина от значений соматического, психологического и гомеостатического компонентов, исходя из принципа выявления и учета «слабых» звеньев в функциональном состоянии организма [7, 14]. Составляющие шкалы оценки ИПЗ: общие резервы (ОР), физические резервы (ФР), психические резервы (ПР), адаптационные резервы (АР).
 Использован следующий порядок вычисления ИПЗ: результаты каждого теста соотносили с нормой и рекомендациями авторов конкретной методики (результатами их исследований достаточной выборки испытуемых) и переведены по линейным шкалам в проценты от максимума функционального резерва для здорового организма. На последнем этапе оценки соматической, психоэмоциональной и гомеостатической составляющих суммированы в ИПЗ [7, 15].
Использован следующий порядок вычисления ИПЗ: результаты каждого теста соотносили с нормой и рекомендациями авторов конкретной методики (результатами их исследований достаточной выборки испытуемых) и переведены по линейным шкалам в проценты от максимума функционального резерва для здорового организма. На последнем этапе оценки соматической, психоэмоциональной и гомеостатической составляющих суммированы в ИПЗ [7, 15].
Одной из целей обобщения результатов тестирования в виде интегральной оценки служит реализация современного подхода к показателю здоровья не как к усредненной сумме показателей резервов разных органов и систем, а как к отсутствию «провалов» показателей резервов по отдельным органам и системам [7]. Поэтому использованный алгоритм оценки подчеркивает наличие слабых звеньев организма. Это позволяет и врачу, и обследуемому не акцентироваться на отдельных хороших показателях, а сосредоточить свое внимание на слабом звене и принять необходимые меры по его укреплению.
Динамика ИПЗ, выраженного в процентах от максимально возможного значения, позволяет объективно оценивать эффективность лечебно-реабилитационных и оздоровительно-тренировочных мероприятий. При этом эффект проведенного оздоровления или лечения ставится в зависимость от прироста «количества здоровья», а не от уменьшения «количества болезни» [7, 15].
Статистическая обработка данных
Статистическая обработка производилась с помощью программы SPSS Statistics 17.0 и MS Excel. Поскольку на данном объеме выборки не получено нормального распределения признаков, были использованы методы непараметрической статистики: для выявления значимости различий между тремя группами применен критерий U Манна–Уитни при достоверном уровне вероятности различий р < 0,05. В статье представлены среднее арифметическое и стандартное отклонения.
Результаты исследования и их обсуждение
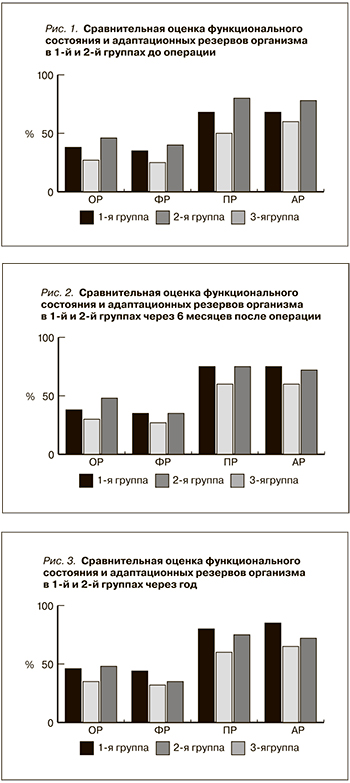
Во всех группах обследуемых нежелательных реакций на физическую нагрузку не отмечено. По результатам исследования с помощью АПК «Истоки здоровья» до операции значимых различий по всем шкалам в I и II группах не было (рис. 1).
В раннем послеоперационном периоде значимых различий величины ИПЗ в I и II группах не выявлено, однако в позднем послеоперационном периоде отмечен рост значений показателей здоровья в I группе по сравнению со II, что связано с проведением физической реабилитации в этой группе.
Сравнительная оценка функционального состояния и адаптационных резервов организма в двух группах больных через месяц после операции показала (р < 0,05): в I группе по сравнению со II отмечается увеличение ОР на 6 %, ФР – на 6,1, ПР – на 2,6, АР – на 3,2 %. Однако относительно данных до операции имело место снижение ОР, ФР, АР, что связано с ограничением двигательного режима в связи с особенностями раннего послеоперационного периода у пациентов после трансплантации почки. Обнаружено увеличение ПР, что, по-видимому, связано с положительными эмоциями от долгожданной операции.
Через 6 месяцев после операции в I группе по сравнению со II достоверно увеличились (р < 0,05) ОР на 10,1 %, ФР – на 5,3, ПР – на 8,1, АР – на 7,8 %, что связано с проведением физической реабилитации в этой группе, однако по сравнению с III группой наблюдается отставание по всем шкалам (рис. 2). Следует отметить растущую разницу между группами в шкалах ОР, ФР, ПР и АР в пользу группы I, установленную статистически (р < 0,05), что подтверждает пользу выполнения физических упражнений. Таким образом, пациенты занимающиеся физкультурой, имеют больший показатель общих резервов здоровья.
Через год после операции в I группе по сравнению со II отмечается значительное улучшение по всем компонентам здоровья (р < 0,05): ОР возросли на 13,6 %, ФР – на 9,8, ПР – на 12,4 и АР – на 15,5 % (рис. 3).
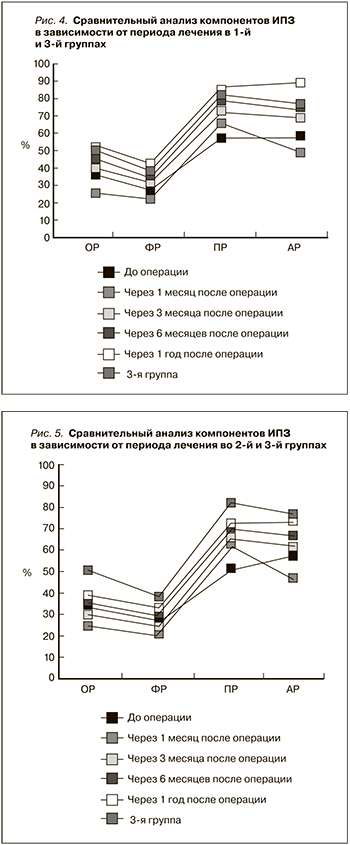
Сравнительная оценка I группы на различных сроках после операции по сравнению с группой здоровых людей показала: через год после операции показатели компонентов ИПЗ в I группе оказались выше: ОР – на 0,7 %, ФР – на 4,0 и АР – на 12,8 %, что связано с полезными эффектами физических нагрузок и нормальной функции почки после трансплантации, а увеличение ПР на 2,2 % можно связать с появлением физических сил и способностью ощущать себя полноценным работоспособным человеком в связи с контрастом ощущений до операции. В группе здоровых людей не происходило существенных изменений в повседневной жизни, которые бы стимулировали их вести здоровый образ жизни, заниматься физкультурой, что связано с отсутствием болезней, операции, риска смерти, ощущения беспомощности, бессилия и т.д., именно поэтому показатели I группы оказались значимо выше (р < 0,05; рис. 4).
На различных сроках после операции во II группе показано улучшение компонентов ИПЗ по сравнению с дооперационным периодом, однако через год показатели оказались ниже (р < 0,05), чем в III группе: ОР – на 12,9 %, ФР – на 5,8, ПР – на 10,2 и АР – на 2,7 % (рис. 5).
Заключение
Сравнительная оценка функциональных и адаптационных резервов организма в двух группах больных через 1, 3, 6 и 12 месяцев после операции показала, что через месяц после операции в I группе по сравнению со II отмечено увеличение ОР на 1,2 %, ФР – на 2,1, ПР – на 2,6, АР – на 1,2 %, что статистически недостоверно, однако через год после операции в I группе по сравнению со II отмечено значительное улучшение по всем компонентам ИПЗ: увеличение ОР –на 13,6 %, ФР – на 9,8, ПР – на 12,4 и АР – на 15,5 %. Результаты обследования с помощью АПК «Истоки здоровья» позволили не только количественно оценить общие резервы здоровья в выделенных группах, но и изучить особенности адаптации к физическим нагрузкам пациентов после трансплантации. Так, снижение общих, физических и адаптационных резервов здоровья на первом месяце после операции происходило за счет самой операции и особенностей послеоперационного этапа при трансплантации. Однако мы наблюдаем рост всех показателей в течение года в I группе по сравнению со II за счет проведения физической реабилитации в течение года. Более того, пациенты с трансплантированной почкой при регулярных занятиях оздоровительной физической культурой могут демонстрировать более высокие показатели отдельных компонентов здоровья относительно общей популяции.
Все полученные данные подтверждают известный факт: регулярные физические нагрузки, выбранные в соответствии с функциональным состоянием организма, полезны для здоровья и повышают его резервы. Таким образом, разработанные индивидуальные программы физической реабилитации для раннего и позднего послеоперационного периодов, учитывающие результаты комплексного обследования, служат важным компонентом лечебно-реабилитационных мероприятий на различных этапах реабилитации после трансплантации почки.



