Введение
Анемия – одно из самых частых осложнений хронической болезни почек (ХБП). Популяционные исследования показывают однозначный тренд нарастания частоты выявления нефрогенной анемии (НА) с прогрессией ХБП [1–3]. Статистически достоверное возрастание частоты развития анемии при ХБП отмечается при снижении скорости клубочковой фильтрации (СКФ) до 60–70 мл/мин [1]. Появление анемии у пациентов на начальных стадиях ХБП в основном обусловлено особенностями течения заболевания почек и сопутствующим коморбидным фоном, и причины ее развитие, чаще всего выходят за рамки патогенеза истинной НА. Точно так же следует расценивать развитие у пациентов ХБП 4–5-й ст. анемии, резистентной к терапии стимулирующими эритропоэз агентами.
Лечение НА основано на понимании ее патогенеза. Оно сводится к устранению ведущих патогенетических факторов, начиная с адекватной коррекции уремии, минимизации воспаления, обеспечения достаточных запасов железа, завершаясь назначением стимуляторов эритропоэза. Базисные принципы лечения НА отработаны в течение последних трех десятилетий. Они научно обоснованы, изложены в литературе и национальных практических рекомендациях.
Появление нового направления патогенетической терапии НА связано с воздействием на систему стабилизации гипоксией индуцируемого фактора (ГИФ). Обоснование нового подхода к терапии НА также базируется на патогенезе ее развития, а именно активации синтеза эндогенного эпоэтина (ЭПО) ренальной и экстраренальной природы, обусловленной снижением доставки кислорода тканям и уменьшения функционального блока доставки железа в ядерные клетки эритропоэза, необходимого для синтеза гемоглобина (Hb). Применение ингибиторов пролилгидроксилаз в качестве альтернативы препаратам рекомбинантного человеческого ЭПО (рчЭПО) позволяет воздействовать на оба направления патогенетической терапии НА. При использовании ингибиторов пролилгидроксилаз для лечения НА на первый план выступают вопросы доказательства их эффективности и безо-пасности, отмены применяемых стимуляторов эритропоэза, а также подтверждения преимущества их использования у определенной категории пациентов. Несмотря на большой объем клинических исследований, обзоров и мета-анализов, относящихся к препаратам группы ингибиторов пролилгидроксилаз, по всем этим вопросам консенсус не достигнут.
Цель настоящей работы – представить обзор причин развития резистентности к стимулирующим эритропоэз препаратам при НА с учетом ее патогенеза, что поможет клиницисту обосновать подходы к лечению.
Патогенез НА
НА относится к гипорегенеративным анемиям, обусловленным неэффективным эритропоэзом. Причины ее развития – это факторы, связанные с ХБП, которые приводят к нарушению функционирования эритрона, начиная с родоначальных, пролиферирующих и созревающих клеток и заканчивая зрелыми эритроцитами, циркулирующими в крови.
Последовательность вовлечения различных факторов, принимающих участие в патогенезе НА, дебютирует с развития нефросклероза, ретенции уремических токсинов и активации воспалительных цитокинов (см. рисунок). Дальнейшие механизмы развития НА следует рассматривать как вторичные. К ним можно отнести модификацию механизмов регуляции эритропоэза, присущих здоровым лицам на уровне генома, дефицит синтеза эндогенного ЭПО, развитие функционального дефицита железа, активацию апоптоза и программированной клеточной смерти.
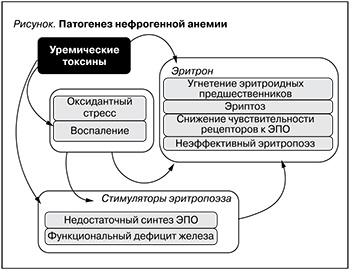
Уремические токсины
С целью систематизации представлений о роли уремических токсинов в развитии НА следует выделить их непосредственное влияние на кроветворную систему, воспаление, оксидативный стресс и эриптоз.
По сравнению с клетками других органов и систем для эритрона описано гораздо меньше токсинов, обладающих прямым действием. Было показано, что накопление в клетках эритропоэза АДМА ассоциируется с повышением резистентности к ЭПО, что авторы связывают со снижением продукции оксида азота, стимулирующего эритропоэз [4]. Такие полиамины, как спермин, спермидин, путресцин и кадаверин («трупные яды»), снижают пролиферацию и созревание ядерных эритроидных предшественников независимо от величины ЭПО [5]. Блокирующий эффект на ядерные эритроидные клетки можно ожидать от β-2 микроглобулина, моноцитарного колонии стимулирующего фактора, токсинов, связанных с белками (например, хинолиновая кислота) и токсинов средней молекулярной массы [6]. Особое место среди уремических токсинов занимает индоксилсульфат. Его роль в развитии НА прослеживается на многих критических для эритропоэза этапах [7]. Он ингибирует пути активации рецептора ЭПО, подавляет продукцию HIF, блокирует транскрипции гена ЭПО при гипоксии, а также снижает темп эритроидой продукции посредством активации Са2+-зависимого НАДФ оксидазного и глутатионового механизмов [5].
Количество продуктов ретенции при уремии, потенциально оказывающих прямое и косвенное влияние на эритрон, вероятно, гораздо больше. Включение в список токсинов и доказательство их токсического действия на эритрон требуют методически сложной работы, одной из проблем которой является отделение эффекта одного токсина от другого. Вероятно, в этот список можно включить FGF‐23, обладающий широким спектром независимых взаимосвязей с продукцией эритроцитов, ЭПО, регуляции воспаления и обмена железа [8], а также адипонектин, являющийся продуктом и регулятором роста массы жировой ткани, в т.ч. и в костном мозге, что оказывает негативное влияние на активность гемопоэза в целом [9]. Описан ряд маркеров, присутствие которых сопутствует снижению СКФ и развитию резистентности эритропоэза к ЭПО. Например, белок Fas (CD95/APO-1), относящийся к суперсемейству TNF-рецепторов, принимает участие в регуляции клеточной смерти, в т.ч. лейкоцитов и стволовых клеток гемопоэза [10].
Роль уремических токсинов в развитии НА нельзя рассматривать исключительно с позиции их влияния на те или иные отделы эритрона в отрыве от других глобальных механизмов их влияния на организм человека. Среди уремических токсинов выявлено 35 веществ, являющихся активаторами воспалительных каскадов. В развитии НА принимает участие и ряд других составляющих общей уремической токсичности, например фиброз костной ткани под воздействием паратгормона и уменьшение числа костных полостей, заселяющихся мезенхимальными стволовыми клетками, развитие белково-энергетической недостаточности и т.д. [11, 12].
Воспаление
Воспаление рассматривается как неотделимый фактор развития НА. Изучение при ХБП изменений синтеза и экспрессии рецепторов, представленных в базах данных метаболом/генов, показало, что уремические токсины, которые представляют 1/80 часть низкомолекулярного метаболома сыворотки крови, способны индуцировать либо подавлять экспрессию воспалительных молекул. Экспрессия генов, причастных к продукции уремических токсинов, у пациентов с ХБП модулируется и регулируется путями каспазы-1 и TNF-a и подавляется регуляторными Т-клетками. Увеличение продукции уремических токсинов происходит избирательно и выступает в качестве молекулярных паттернов, связанных с молекулами повреждения DAMP, и молекулярных паттернов, связанных с гомеостазом, которые модулируют воспаление. Показано, что возрастание уремических токсинов не всегда является пассивным процессом накопления. Некоторые гены, принимающие участие в синтезе веществ, отнесенных к уремическим токсинам, активируются при ХБП через каспаза-1/воспалительные цитокиновые пути [13].
Для ХБП характерно хроническое воспаление низкой степени активности. оно характеризуется относительно низкими проявлениями системной иммунной реакции, что связано с недостаточным тканевым стрессом для развития классического или системного воспаления [14]. Для этого варианта воспаления характерны следующие признаки:
- содержание С-реактивного белка (СРБ) в сыворотке крови находится в пределах 3–10 мг/л;
- концентрация ключевых провоспалительных цитокинов в 2–4 раза превышает верхнюю границу нормальных значений;
- атипичные системные коагулопатии;
- медленное развитие признаков дисфункции органов и систем;
- ускоренное развитие атеросклероза сосудов;
- артериальная гипертензия;
- активация процессов старения;
- отсутствие связи органных изменений с системными проявлениями инфекционных или аутоиммунных заболеваний с признаками классического воспаления.
Даже при субклинических проявлениях воспаление как системный процесс патогенетически связано со многими звеньями развития НА (табл. 1).
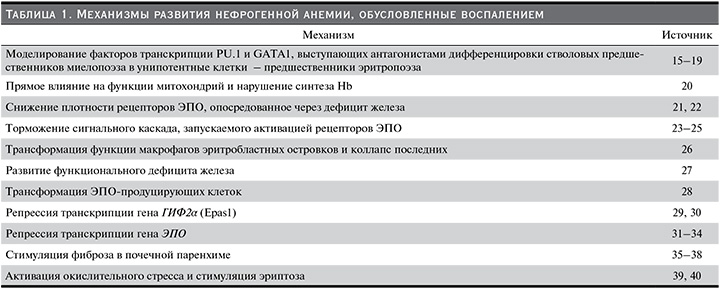
Как видно из таблицы, воспаление оказывает существенное влияние на все звенья функционирующего эритрона, начиная с ранних стадий развития эритропоэза и заканчивая функционированием зрелых эритроцитов, а также на синтез ЭПО и инкорпорацию железа.
Помимо воспаления низкой степени активности пациенты с ХБП регулярно сталкиваются с интеркуррентными заболеваниями, приводящими к появлению признаков воспаления классического типа. Это приводит к виражам маркеров воспаления с последующим снижением уровня Hb и повышением потребности в рчЭПО, что можно характеризовать как наслоение хронического воспаления на классическое течение НА.
Дефицит железа
Дефицит железа – это один из важных факторов, определяющих риск развития анемии при ХБП. На ранних стадиях развития ХБП он проявляется в виде абсолютного дефицита железа, выступая как общепопуляционный фактор риска и дополняется потерей железа на фоне массивной протеинурии. По мере прогрессирования ХБП и нарастания признаков воспаления добавляются факторы, приводящие к развитию функционального дефицита железа. Систематизируя причины дефицита железа при ХБП, можно выделить следующие значимые факторы:
1. Активация цитокиновых каскадов и переключение большей части потока железа в сторону внутриклеточного депонирования.
2. Снижение доступности железа эритропоэзу через гепсидиновый механизм.
3. Снижение доступности железа эритропоэзу, опосредованное факторами гипоксии.
4. Снижение выработки эритроферрона.
5. Потеря железа при массивной протеинурии.
6. Скрытые желудочно-кишечные кровотечения на фоне уремии.
7. Перманентные ятрогенные кровопотери при процедурах гемодиализа.
В типичном случае нормальные запасы железа у пациента с ХБП поддерживаются с помощью парентеральных препаратов железа. При достижении безопасного уровня ферритина и насыщения трансферрина железом важным механизмом, повышающим доступность железа эритропоэзу, выступает активация синтеза эритроферрона ядерными эритроидными предшественниками, что устраняет несоответствие величины доставки железа в костномозговые островки эритропоэза, в которых на фоне стимуляции рчЭПО активируется синтез Hb. Эритроидные предшественники получают железо в виде Н-ферритина из макрофагов и через рецепторы трансферрина 1 (TFR1). Данные МРТ сканирования и гистологии костного мозга пациентов, получавших гемодиализ и рчЭПО, показали, что у них существенно возрастает содержание запасов железа в пределах костного мозга, тогда как до эры рчЭПО повышенные запасы железа регистрировались в селезенке и печени, но не в костном мозге [41]. Данные обсервационных исследований показывают отсутствие рисков при уровне ферритина сыворотки до 800 мкг/л и выше и насыщения трансферрина железом до 40–50% [42, 43]. Повышение ферритина может быть связано как с применением препаратов железа, так и с интеркуррентной инфекцией, но при отсутствии воспаления уровень ферритина сыворотки перестает ассоциировать с неблагоприятными исходами [44]. Недостаточными для переноса данных в клиническую практику также оказались ссылки на исследования перегрузки железом паренхиматозных органов, оценка которых производилась с помощью МРТ без связи с клинической картиной перегрузки и ее исходами [45].
В конечном итоге можно констатировать, что поддержание баланса железа у больных тХБП, как правило, соответствует его потерям. У пациента с тХБП, получающего гемодиализ через нативную артериовенозную фистулу, они достигают в среднем 1,5 г, а у пациента с катетером – 2,5 г в год [45]. Возрастание потребности в железе необходимо рассматривать с позиции нестабильной ситуации, благоприятной в случае роста уровня Hb на этапе коррекции анемии и неблагоприятной в случае роста потери железа или нарастания функционального дефицита. Эти случаи следует анализировать на уровне как индивида, так и отдельно взятого диализного центра.
Эриптоз
Снижение длительности жизни эритроцитов – клинически неявный, но важный фактор НА [46–48]. Он регистрируется при ХБП 3-й ст. Если при ХБП 1-й ст. длительность жизни эритроцитов равна 120±50 дней, то при ХБП 3-й ст. она достоверно снижается до 90±32 дней, а при ХБП 5-й ст. – до 60±24 дней [49, 50]. Этот фактор также ассоциируется с потребностью назначения эритропоэзстимулирующих препаратов (ЭСП) [51]. Эриптоз инициируют уремия, воспаление, оксидативный стресс и гипоксия. Механизмы его развития включают нарушение регуляции ионных каналов, накопление внутриклеточного Ca(II), активацию кальций-активируемых протеаз и разрушение цитоскелета эритроцитов, нарушение реполяризации клеточной мембраны, перемещение на ее поверхность фосфатидилсерина, запускающего эритрофагоцитоз, и снижение экспрессии CD47, препятствующего захвату эритроцитов макрофагами [45]. Следовательно, при тХБП в зрелых эритроцитах происходят изменения, приводящие к утрате стабильности и эластичности наружной мембраны, запускающие механизм активного захвата функционально неполноценных эритроцитов макрофагами, которые их утилизируют, предотвращая выход свободного Hb в кровь.
Эндогенный эритропоэтин
Отличительной чертой НА является неадекватная тяжести анемии продукция эндогенного ЭПО. На ранних стадиях ХБП воздействие факторов, угнетающих эритропоэз, уравновешивается пропорциональной активацией синтеза ЭПО, но начиная с ХБП 4-й ст. его синтез не позволяет компенсировать темп снижения содержания Hb, что напрямую связано с развитием нефросклероза и снижением чувствительности кислородного сенсора почек к анемии.
Гипоксией индуцируемый фактор
Кислородный сенсор, запускающий стабилизацию гипоксией индуцируемого фактора (ГИФ), чутко реагирует на парциальное давление кислорода в почечной паренхиме. Парциальное давление кислорода зависит от его поступления и расходования. В нормальных условиях главный потребитель кислорода в почках – это эпителий проксимальных почечных канальцев. В случае снижения их активности на фоне нефросклероза снижается потребление кислорода и система реагирования на снижение Hb перестает работать, т.к. парциальное давление кислорода в расчете на сниженную функцию клеток значимо не снижается. В прошлом главная роль в снижении ЭПО отдавалась фактору нефросклероза, уменьшающего число клеток, способных его синтезировать, но, зная о пластичности реагирования фибробластподобных клеток, способных быстро перестроиться на продукцию ЭПО, этот фактор, вероятно, становится менее значимым [52]. Ответом на этот вопрос может быть определение величины пула клеток, синтезирующих ЭПО, на фоне введения ингибиторов пролилгидроксилаз. Известны случаи нормализации уровня Hb у пациентов с тХБП в случае повышения уровня ГИФов, что сопровождается активацией синтеза ЭПО в печени [53, 54]. Выделяют следующие механизмы блокады и синтеза эндогенного ЭПО:
- трансформация фибробластов, продуцирующих ЭПО, в миофибробласты;
- снижение потребности в кислороде почечной паренхимы на фоне фиброза;
- торможение синтеза и стабилизации ГИФов;
- подавление транскрипции гена ЭПО.
Необходимо отметить, что далеко не все факторы блокады синтеза ЭПО напрямую связаны со снижением парциального давления кислорода в тканях. Известны механизмы, которые связаны с воспалением (влияют на экспрессию генов эритропоэтина и ГИфов), содержанием железа (выступает кофактором пролилгидрокислаз, снижая длительность стабильного состояния ГИФов) и запуском NRF2 сигнального пути.
НА и резистентность
Современная эра лечения НА началась после завершения клинических испытаний 3-й фазы рчЭПО-a в 1989 г. С этого времени накоплен обширный материал, ставший основой клинических рекомендаций с уровнем доказательности и убедительности, равным 1А. Не умаляя достоинства препаратов рчЭПО при лечении НА, более подробно остановимся на вопросах, которые относятся к проблеме резистентности к этим препаратам.
Под резистентностью (гипореактивностью) к терапии НА препаратами рчЭПО подразумевают недостаточный ответ или его отсутствие на введение препарата. Этот ответ зависит от соблюдения базовых условий терапии тХБП – адекватный режим заместительной почечной терапии и своевременное восполнение запасов железа.
Особого внимания заслуживает рассмотрение подходов к определению критериев резистентности. До публикации данных клинических исследований, в которых определялись риски использования высоких доз рчЭПО для нормализации уровня Hb, под резистентностью подразумевалось состояние, когда повышение дозы препарата не приводило к дальнейшему росту уровня Hb. Возрастание рисков развития осложнений при высоких дозах рчЭПО привело к снижению доз вводимого препарата, а также к пониманию необходимости оценивать соотношение пользы и вреда при избранной тактике лечения НА. В рекомендациях NICE 2011 г. (Великобритания) на административном уровне был впервые введен термин «безо-пасная доза препарата», который стал использоваться как ведущий критерий для решения клинического вопроса о том, насколько оправданно превышение дозы введения препарата, не рассматривая его с позиции резистентности. В литературе можно найти расчеты максимальной дозы рчЭПО безотносительно коррекции на массу тела пациента до вычисления т.н. индексов резистентности. В отечественных рекомендациях вопросу резистентности также уделено должное внимание. Первичную резистентность к ЭСП рекомендуют констатировать при отсутствии повышения уровня Hb в течение первого месяца после применения стандартной дозы рчЭПО, рассчитанной по массе тела. Вторичная резистентность констатируется в случае, если после периода стабилизации уровня Hb на исходной дозе рчЭПО возникает необходимость повышения дозы препарата на 50%, что позволяет поддерживать прежде достигнутый уровень Hb [55]. В национальных рекомендациях также упоминается понятие дозы, повышать которую без особых причин не следует.
Анализ статистических данных регистрации резистентности свидетельствует о том, что ее встречаемость зависит от принятых критериев определения. Так, по критерию резистентности 300 МЕ/кг/нед. рчЭПО, или 1,5 мкг/кг дарбэпоэтина, резистентность (невозможность достичь целевого уровня Hb) определялась у 5–10% пациентов [56]. Но в других исследованиях, где критерии резистентность могли различаться и быть менее строгими, ее встречаемость колеблется в пределах от 5 до 20% [57].
Отсутствие единых критериев резистентности затрудняет анализ литературы, посвященной этой проблеме. Проще всего оценивать эффективность применения препарата с позиции достижения целевого уровня Hb. Но неэффективность терапии рчЭПО у части пациентов отмечалась с самого начала его использования. Среди пациентов, включенных в первое клиническое исследование 3-й фазы ЭПО-α, отсутствие эффекта было отмечено менее чем у 5% пациентов, причиной чему были миелофиброз, фиброзирующий остеит, остеомиелит, а также значимые острые или хронические кровопотери [58]. Спустя десятилетия похожие результаты были получены во французском эпидемиологическом исследовании, в котором отмечено, что среди пациентов с уровнем Hb ниже 100 г/л в течение года не отвечают на терапию 95,3%, достигая уровня 100–130 г/л [59]. Но при практике проведения одномоментных исследований теоретически невозможно достичь результатов, при которых 95% пациентов имели бы уровень Hb выше 100 г/л. Связано это с тем, что уровень Hb у пациента с тХБП подвержен постоянным колебаниям, что связано с влиянием внешних аппаратурных, средовых и внутренних биологических факторов. Среди них необходимо выделить сопутствующие заболевания и осложнения, повышающие кровопотери, воспаление, нарушения питательного статуса, преходящее снижение адекватности диализа, госпитализации и т.п. Это приводит к изменению дозы рчЭПО и нарастанию резистентности. Например, было показано, что повышение уровня СРБ сопровождается снижением уровня Hb и нарастанием дозы рчЭПО, а также возрастанием доли пациентов с резистентностью с 7,6 до 12,3% [60].
Важно отметить обратимость таких состояний, и если рассматривать данные статистики, то можно сделать вывод, что число пациентов, не отвечающих на терапию (не выявленные или инкурабельные причины резистентности), обычно не превышает 5%. В работе, в которой в основу исследования положено отсутствие достижения целевого уровня Hb в течение 4 месяцев от начала терапии, было показано, что доля пациентов, не достигших целевого уровня Hb, составляет менее 5% [61]. О том же свидетельствуют данные DOPPS 2018 г. (N=26,656), которые подтвердили, что при наблюдении в течение 12 месяцев доля пациентов с резистентностью составила 4,4% [62]. Интересно и то, что [63] за время наблюдения 42% пациентов из общей группы как минимум в течение 1 месяца побывали в группе максимальной резистентности, а медиана длительности эпизода резистентности составила 2 месяца. В этой работе регистрировались факторы, ассоциирующиеся с развитием резистентности. К ним были отнесены СРБ, низкое насыщение трансферрина железом, снижение альбумина сыворотки и недавняя госпитализация.
Если обобщать данные, имеющие отношение к причинам, выявленным в первом клиническом исследовании рчЭПО (заболевания крови, гиперпаратиреоз, инфекция и массивные кровопотери), то в настоящее время к ним добавлены более чувствительные маркеры диагностики этих состояний, а также парциальная красноклеточная аплазия костного мозга, обусловленная появлением антител к рчЭПО (табл. 2).
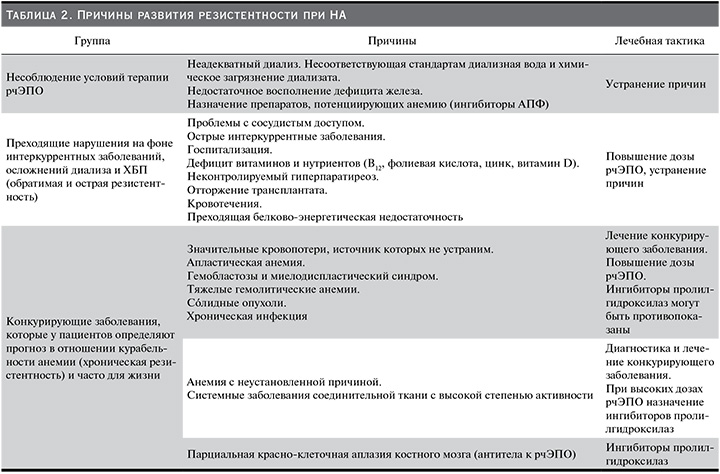
С методической точки зрения, вероятно, также следует добавить организацию лечебного процесса, т.к. литературные источники показывают преимущества в плане достижения цели и доз рчЭПО при лечении НА с привлечением клинического фармаколога [64].
Обоснование тактики терапии резистентной НА
От новых модальностей терапии в клинической практике ожидают большей безопасности и эффективности, особенно в тех случаях, когда стандартная терапия не позволяет добиваться цели в пределах среднетерапевтических доз препарата. В этом отношении НА, резистентная к рчЭПО, могла бы быть образцовым маркером пользы применения ингибиторов пролилгидроксилаз. По данным литературы, получены определенные результаты при использовании ингибиторов пролилгидроксилаз – уменьшение потребности в железе за счет снятия функционального блока [65], отсутствие необходимости коррекции дозы препарата на фоне воспаления [66]. Отмечен их положительный эффект у пациентов с признаками резистентности [67, 68]. Тем не менее вопросы показаний и обоснованности рисков их применения в ситуации резистентности практически никем не затрагиваются.
Причины развития резистентности при НА представлены основными группами:
1) несоблюдение условий терапии рчЭПО;
2) преходящие нарушения на фоне развития тяжелых сопутствующих заболеваний, осложнений диализа и ХБП (острая резистентность);
3) конкурирующие заболевания, которые определяют прогноз в отношении курабельности анемии (хроническая резистентность) и часто – жизни.
Такой подход к рассмотрению причин развития резистентности облегчает выбор тактики обследования и лечения НА у пациента с ХБП (табл. 2).
Так, в случае выявления причин из первой группы основное внимание должно быть уделено их устранению, т.е. обеспечению базовых условий противоанемической терапии: адекватная доза диализа, оптимальные запасы железа и его назначение (ферритин сыворотки – 200–800 мкг/л, TSAT – 20–40%), минимизация воспалительной активности (ультрачистый диализат, биосовместимый расходный материал, нативная фистула, строгое соблюдение правил асептики и антисептики). Устранение этих факторов позволяет некоторым пациентам обходиться без ЭСП.
Вторая группа причин – преходящие события, которые обратимы и укладываются примерно в 2–4 месяца. Как указывалось выше, доля таких пациентов на протяжении года наблюдения может доходить до 40%. Для диализных пациентов, вероятно, наиболее частыми причинами острой резистентности являются инфекция (факторы риска – уремия, катетеры, белково-энергетическая недостаточность и воспаление) и дисфункция сосудистого доступа (нередко сочетание), сопровождающиеся виражом маркеров воспаления. В этих случаях использование ингибиторов пролилгидроксилаз не оправданно, т.к. их использование может повышать риски инфекции и тромбозов [69, 70].
Третья группа причин, по сути, включает отдельные нозологические состояния, приводящие к анемии, и в этой группе выбор ЭСП определяется его эффективностью и безопасностью в каждой отдельно рассматриваемой ситуации, что выходит далеко за рамки обзора. Показанием к назначению ингибиторов пролилгидроксилаз в этой группе пациентов, бесспорно, является парциальная красно-клеточная аплазия, которая среди резистентных к рчЭПО пациентов встречается не столь редко, но требует выявления антител к эритропоэтину [71]. Каждый из пациентов с ХБП, относящихся к третьей группе резистентности, требует отдельного рассмотрения с целью уточнения объема дополнительных исследований и выработки тактики коррекции НА.
Заключение
НА – это яркий пример успешного применения патогенетического подхода к лечению осложнений ХБП. Значимые звенья патогенеза НА, такие как уремия и воспаление, эриптоз, дефицит железа и ЭПО, поддаются коррекции, что позволяет достигать целевого уровня Hb. Адекватно корректируя уремию, дефицит железа и эритропоэтина, можно опосредованно влиять на воспаление и эриптоз. При тХБП трудно устранимым фактором развития резистентности к ЭСП выступает воспаление, выраженность которого опосредована сопутствующими неблагоприятными факторами. Использование новых модальностей лечения НА помимо безопасности будет ставить вопрос об эффективности в условиях резистентности. Мы считаем, что каждый случай резистентности должен рассматриваться с позиции выявления причины и дальнейшего выбора апробированной и патогенетически обоснованной терапии.



