Введение
Хроническая болезнь почек (ХБП) во всем мире признана ведущей проблемой общественного здравоохранения. Ее действие на сердечно-сосудистые риски и развитие терминальной хронической почечной недостаточности напрямую оказывает влияние на глобальное бремя заболеваемости и смертности [1]. Прогрессирующие структурно-функциональные изменения в сердечно-сосудистой системе (ССС) при ХБП обусловливают плохой прогноз заболевания [2]. Среди многочисленных «почечных» факторов сердечно-сосудистого риска при ХБП весьма важную роль играет цитокиновый статус [3].
К цитокинам относят интерфероны, колониестимулирующие факторы, хемокины, трансформирующие ростовые факторы, фактор некроза опухоли a (ФНО-а), интерлейкины (ИЛ) и др. Повреждающие эффекты цитокинов проявляются при их избыточной, долговременной и генерализованной продукции, при нарушении равновесия между прои противовоспалительными типами цитокинов [3]. При ХБП начало воспалительного ответа и основные этапы его развития происходят с участием иммунокомпетентных клеток в присутствии цитокинов, которые продуцируются клетками иммунной системы в ответ на стимуляцию инфекционными антигенами, в т.ч. вирусами, и играют весьма важную патогенетическую роль в возникновении сердечно-сосудистых осложнений [1, 2].
Субклиническое воспаление эндотелия сосудистой стенки рассматривается как важное звено патогенеза артериальной гипертензии (АГ), атеросклероза и, возможно, прогрессирования ренальной дисфункции [4]. Поэтому изучение цитокинового профиля и его взаимосвязь со структурно-функциональными изменениями ССС при ХБП остаются актуальной задачей для оценки прогноза заболевания и эффективности ренои кардиопротективной терапии, в т.ч. и у пациентов, перенесших COVID-19.
Цель исследования. Дать характеристику цитокиновой модели развития сердечно-сосудистых изменений у больных ХБП, перенесших новую коронавирусную инфекцию.
Материал и методы
Проведено клиническое наблюдение и обследование 150 больных ХБП, перенесших COVID-19. Наблюдение и обследование больных осуществлялись на базе Тюменского кардиологического научного центра и Тюменского ГМУ (кафедра пропедевтической и факультетской терапии). У наблюдаемых больных коронавирусная инфекция протекала в среднетяжелой (31%) и легкой (69%) формах. Больные ХБП, перенесшие COVID-19, были разделены на 2 группы: больные ХБП без сердечно-сосудистых заболеваний (ССЗ; 65 человек) и больные ХБП, имевшие ССЗ (85 человек).
Возраст больных составил 56 [50,00; 62,00] лет в группе без ССЗ и 58 [52,00; 63,00] лет c CCЗ. Из ССЗ во второй группе 53,4% пациентов имели АГ, 15,5% – ишемическую болезнь сердца, 31,1% – нарушения ритма сердца; сердечная недостаточность по NYHA 1–2-й ст. имелась у 67,3% пациентов. Группы значимо различались по уровню систолического (САД), диастолического (ДАД) артериального давления (АД), частоте сердечных сокращений, индексу массы тела (р<0,001 соответственно для всех параметров), с более высокими показателями во второй группе. Исходно в первой группе объем поражения легких более 50% был в 20,0%, во второй – в 47,6% случаев. По стадиям ХБП больные распределились следующим образом: С1 – 56,4%, С2 – 43,6% в группе без ССЗ и С1 – 52,5% и С2 – 47,5% в группе с ССЗ. Пациентам обеих исследуемых групп проводили клинико-лабораторное и инструментальное исследования в момент госпитализации и через 3 месяца после выписки из стационара. В данной работе представлены показатели через 3 месяца после выписки из стационара.
Всем больным проведены клиническое, лабораторное и инструментальное обследования (суточное мониторирование АД, эхокардиография – Эхо-КГ). Больные осмотрены терапевтом, кардиологом, нефрологом. Специальные методы исследования включили определение уровней цитокинов (ИЛ-1, -6, -8, ФНО-а, TgFβ1), вчСРБ – иммунотурбидиметрическим методом на полуавтоматическом анализаторе открытого типа «Clima MC-15», Испания; Д-димера, фибрингена, ферритина, натрийуретического пептида (NT-proBNP), цистатина С, микроальбуминурии (МАУ) на анализаторе «Destiny Plus», Ирландия; скорость клубочковой фильтрации (СКФ) по формуле CKD-EPI. Всем пациентам исходно в стационаре при госпитализации проведена компьютерная томография органов грудной клетки. Статистический анализ проводился с помощью пакета прикладных программ IBM SPSS Statistics, 21. В зависимости от распределения при сравнении показателей в независимых группах использовали t-критерий Стьюдента или U-критерий Манна–Уитни. При нормальном распределении данные представляли как среднее М и стандартное отклонение (SD), при распределении, отличном от нормального, данные представлены в виде медианы (Me) и интерквартильного размаха [25%; 75%]. Парным критерием Стьюдента или критерием Вилкоксона рассчитывали динамику между связанными группами. Результаты оценивались как статистически значимые при двустороннем уровне, р<0,05.
Результаты
Как показали проведенные исследования (табл. 1), у наблюдаемых больных ХБП с ССЗ через 3 месяца после перенесенной коронавирусной инфекции отмечено повышение уровней ИЛ-1 (p<0,003) , -6 (p<0,001), ФНО-а (p<0,004), а также тенденция к повышению уровня трансформирующегося фактора роста β (TgFβ1; p<0,702) и снижению уровня ИЛ-8 (p<0,301) по сравнению с больными ХБП без ССЗ. Кроме того, у больных ССЗ отмечается значительное повышение, более чем в 2 раза, уровня вчСРБ, а также в меньшей степени Д-димера, фибриногена и ферритина по сравнению с таковыми у больных без ССЗ.
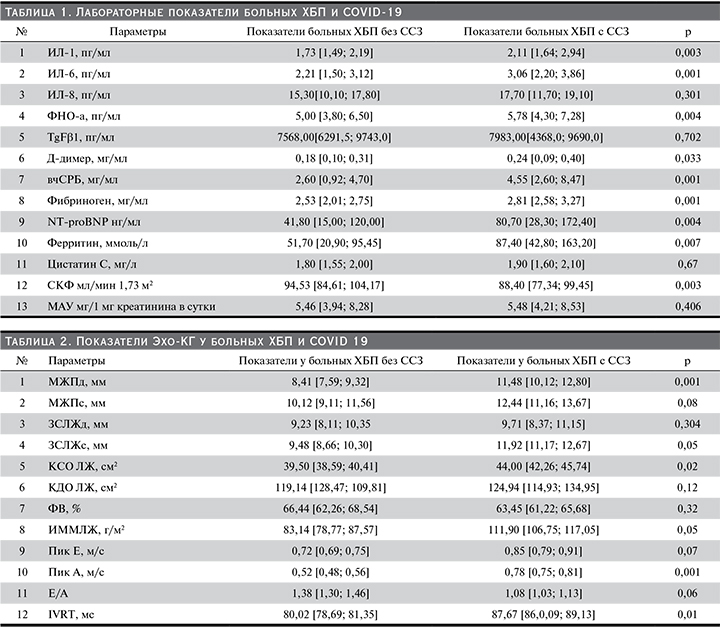
Уровень NT-proBNP у наблюдаемых больных ССЗ в течение 3 месяцев наблюдения увеличился почти в 2 раза по сравнению с больными без ССЗ (р<0,004), а СКФ снизилась на 6,5% (p<0,003), что свидетельствует о нарастании сердечной и почечной недостаточности в группе больных ХБП с ССЗ. Кроме того, нами отмечена тенденция к увеличению уровней цистатина С (p<0,67) и МАУ (p<0,406) в группе больных ССЗ по сравнению с группой без ССЗ.
Суточное мониторирование АД показало увеличение у наблюдаемых больных ССЗ средних значений САД (131±2,6 и 161,3,8 мм рт.ст. у больных без ССЗ и с ССЗ соответственно; р<0,001) и ДАД (83,2±1,8 и 96,2±2,8 мм рт.ст. соответственно; р<0<001), а также скорости утреннего подъема САД (13,1±1,2 и 19,4±1,4 мм рт.ст. соответственно; р<0,001) и ДАД (9,2±0,5 и 14,1±0,7 мм рт.ст. соответственно; р<0,001).
Эхо-КГ-исследование показало (табл. 2) увеличение толщины межжелудочковой перегородки (МЖП) в диастолу, задней стенки левого желудочка (ЗСЛЖ) в систолу, индекса массы миокарда левого желудочка (ИММЛЖ), а также конечного систолического объема левого желудочка (КСО ЛЖ) у пациентов с ХБП и ССЗ по сравнению с больными ХБП без сердечно-сосудистой патологии. При сравнении показателей трансмитрального кровотока в наблюдаемых группах больных получены достоверные различия: у больных ХБП и ССЗ скорость позднего наполнения ЛЖ (Пик А) и время изоволюмического расслабления (IVRT) были существенно выше, чем в группе без ССЗ (табл. 2), что свидетельствует о нарушении диастолической функции ЛЖ.
Обсуждение
При ХБП начало воспалительного ответа и основные этапы его развития проходят с участием иммунокомпетентных клеток. Известно, что ренин-ангиотензин-альдостероновая система может стимулировать продукцию ряда цитокинов, способствующих прогрессированию нефросклероза и присоединению сердечнососудистых осложнений. Кроме того, показано, что уровень провоспалительных цитокинов коррелирует с активностью ХБП и степенью морфологических изменений в почечной ткани [5, 6].
К настоящему времени установлено, что такие провоспалительные цитокины, как ИЛ-1, И-6, ФНО-а, ассоциируются с высокой частотой развития осложнений при ХБП и рассматриваются в качестве иммунологических маркеров сердечно-сосудистого риска [7]. Кроме того, ФНО-а является сильным активатором перекисного окисления липидов и системы свертывания крови, усиливает тромбогенную и вазоконстриктивную активность эндотелия, снижает синтез оксида азота, что в конечном итоге приводит к прогрессированию эндотелиальной дисфункции, повышению жесткости артериального русла и формированию сердечно-сосудистых осложнений [8]. Показано, что у пациентов с АГ и гипертрофией ЛЖ повышалось содержание ФНО-а и ИЛ-6, без существенного повышения концентрации СРБ и ИЛ-1 [10]. В наших исследованиях у пациентов с ХБП и ССЗ также отмечено увеличение уровней ФНО-а и ИЛ-6 на фоне повышенных показателей ИЛ-1 и вчСРБ.
В условиях коронавирусной инфекции у пациентов с ХБП еще более усиливается неблагоприятное влияние провоспалительных цитокинов на состояние ССС и ренальную дисфункцию, особенно при т.н. цитокиновом шторме, что в итоге может приводить к острому почечному повреждению (ОПП) и неблагоприятному исходу заболевания [11]. По данным ряда авторов, половина пациентов, у которых развилось ОПП, умирают во время госпитализации, а среди выживших после развития ОПП пациентов потребность в диализе после выписки была связана исключительно с наличием предшествовавшей ХБП, особенно 4-й и 5-й стадий [12, 13]. В наших исследованиях продолжается дальнейшее наблюдение за пациентами с ХБП, перенесшими новую коронавирусную инфекцию, в точках 6-го и 12-го месяцев с целью уточнения частоты потребности в заместительной почечной терапии.
В наших исследованиях также обнаружено существенное нарушение состояния ССС у наблюдаемых пациентов с изменением морфометрических показателей сердца, нарушением диастолической функции ЛЖ, а также показателей суточного мониторирования АД, что может служить предиктором неблагоприятного прогноза заболевания.
Заключение
Таким образом, патологические процессы, лежащие в основе ХБП, сопровождаются ростом уровня провоспалительных цитокинов, что способствует ускорению кардиоваскулярных осложнений, в т.ч. посредством эндотелиальной дисфункции. Наслоение коронавирусной инфекции в значительной степени усиливает неблагоприятные изменения ССС и ренальную дисфункцию у пациентов с ХБП. С учетом того, что инфекции COVID-19, вероятно, будут продолжаться, существует настоятельная необходимость разработки новых методов ведения пациентов с ХБП и коронавирусной инфекцией, в т.ч. рекомендаций по применению новых противовирусных препаратов и методов нефро-и кардиопротекции.



