Введение
Пациенты с острым коронарным синдромом (ОКС), в т. ч. с подъемом сегмента ST (инфарктом миокарда [ИМ]) составляют значительную часть среди экстренно госпитализируемых по поводу сердечно-сосудистых заболеваний. Актуальность проблемы ОКС подчеркивается в авторитетных рекомендациях профессиональных обществ, в т. ч. Всеросийского научного общества кардиологов [1]. Несмотря на достигнутые успехи в лечении этой категории пациентов, проблема снижения их госпитальной и отдаленной смертности остается достаточно серьезной [2, 3], что требует совершенствования подходов к оценке прогноза и выделению достоверных прогностических маркеров.
Результаты эпидемиологических исследований демон стрируют высокую частоту почечной дисфункции у больных, госпитализированных по поводу ИМ [4–6]. В свою очередь у пациентов с хронической болезнью почек (ХБП) чаще, чем в общей популяции, встречается ишемическая болезнь сердца [7], а риск сердечно-сосудистой смерти у них максимален [8–10]. Нарушения фильтрационной функции почек при ИМ нередко своевременно не распознают, хотя сам факт их наличия влияет в т. ч. на тактику ведения пациентов: им реже назначают ингибиторы АПФ, бета-блокаторы, антитромбоцитарные препараты, статины, выполняют тромболизис [6, 11]. Неблагоприятная проностическая роль ухудшения фильтрационной функции почек в целом установлена и не вызывает сомнений [12, 13], однако ее детерминанты требуют дальнейшего уточнения. Целью настоящего исследования стало определение прогностической роли почечной дисфункции у больных инфарктом миокарда с подъемом сегмента ST.
 Материал и методы
Материал и методы
Проанализированы истории болезни 350 пациентов (188 [53,7 %] мужчин и 162 [42,3 %] женщин в возрасте от 35 до 94 лет; средний возраст – 63,8 ± 12,5 лет) с заключительным клиническим диагнозом “инфаркт миокарда с подъемом сегмента ST”, пролеченных в ГУЗ Республики Коми “Кардиологический диспансер” в 2003–2009 гг. Критерии включения в исследование: заключительный клинический диагноз “инфаркт миокарда с подъемом сегмента ST”, установленный с 2003 по 2009 г., проживание пациентов на территории обслуживания ГБУЗ “Сыктывкарская городская поликлиника № 3”. В исследование не включали пациентов с ОКС без подъема сегмента ST, злокачественными новообразованиями, острыми нарушениями мозгового кровообращения в предшествующие 3 месяца, а также подвергшихся аортокоронарному шунтированию.
В базу данных внесена информация из заключительного клинического диагноза о классе тяжести Killip, осложнениях инфаркта и сопутствующих заболеваниях пациентов; из истории болезни выписаны анамнестические данные, результаты осмотра, лабораторных и инструментальных методов исследования, исход заболевания в стационаре (выписан или умер). Для оценки функции почек учитывали сывороточный уровень креатинина (мг/дл) или рассчитывали скорость клубочковой фильтрации (СКФ) по формуле MDRD [16].
В соответствии с Национальными клиническими рекомендациями “Функциональное состояние почек и прогнозирование сердечно-сосудистого риска” [8] функцию почек считали нормальной при СКФ более 90, умеренно сниженной – при СКФ 60–89 мл/мин/1,73 м²; наличие у пациентов хронической болезни почек (ХБП) устанавливали при уровне СКФ ниже 60 мл/мин/1,73 м²: ХБП III стадии – СКФ 30–59, IV – 15–29, V стадии – менее 15 мл/мин/1,73 м². В зависимости от значений СКФ пациенты разделены на 5 групп: 1-я группа – c СКФ > 90 мл/мин/1,73 м², 2-я – c СКФ от 60 до 89 мл/мин/1,73 м², 3-я – с СКФ от 30 до 59 мл/мин/1,73 м², 4-я – с СКФ 15–29 мл/мин/1,73 м² и 5-я группа – c СКФ менее 15 мл/мин/1,73 м².
Информация о событиях, происшедших с пациентами после инфаркта миокарда до 2010 г. (дата и причина смерти, развитие инфаркта, инсульта), отслеживалась по каждому пациенту в кабинете статистики Сыктывкарской городской поликлиники № 3. Формирование базы данных и ее обработка осуществлены в программе Microsoft Excel 2010.
Статистическую обработку полученных результатов проводили с использованием статистических пакетов программ Excel, BIOSTAT, SPSS 13.0 for Windows, XLSTAT 2012. Применены стандартные параметры описательной статистики. Проверка статистической гипотезы о нормальности распределения осуществлена с использованием критерия Шапиро–Уилка. Сравнение величин с интервальной шкалой измерения, представленных в виде среднего арифметического значения ± стандартное отклонение, осуществлено с помощью t-критерия Стьюдента для независимых выборок. Корреляционный анализ количественных признаков выполнен по Пирсону с расчетом коэффициента корреляции (r). Дискретные величины представлены в виде частот (процент наблюдений к общему числу обследованных). Для сравнения дискретных величин в независимых группах использован критерий Пирсона χ2 для частотной таблицы 2 х 2 с введением поправки на непрерывность (по Йетсу), z-критерий. При сопоставлении смертности в двух группах оценивалось отношение шансов и доверительный интервал. Для выявления факторов, связанных с развитием неблагоприятных событий, выполнен пошаговый многофакторный анализ методом логистической регрессии; изучаемые факторы включали в многофакторный анализ в том случае, если их связь с исходом имела уровень значимости р < 0,05. Оценка отдаленной выживаемости проведена с использованием метода Каплана–Майера и многофакторного регрессионного анализа. Для всех проведенных анализов различия считали достоверными при двустороннем уровне значимости р < 0,05.

Результаты и обсуждение
Клиническая характеристика больных с ИМ без подъема сегмента ST представлена в табл. 1.
Креатининемия находилась в диапазоне от 0,61 до 3,89 мг/дл (в среднем 1,20 ± 0,39 мг/дл). Расчетный уровень СКФ находился в пределах от 5,1 до 176,3 мл/мин/1,73 м² (в среднем 70,79 ± 27,1 мл/мин/1,73 м²).
Численность групп и клиническая характеристика больных с различной степенью почечной дисфункции представлены в табл. 2.
Пациенты с умеренным снижением функции почек, по нашим наблюдениям, представляют наиболее значительную группу больных инфарктом миокарда, составляющую почти половину всех больных (2-я группа). Нормальная функция почек наблюдалась лишь среди 21,1% больных ИМ, а у третьей части больных имело место существенное снижение почечной функции, классифицируемое как ХБП (3-я и 4-я группы).
У части больных с нормальным значением креатинина отмечено умеренное снижение СКФ, что можно объяснить пожилым возрастом и преобладанием женщин в структуре больных.
Увеличение возраста больных ассоциировалось со снижением функции почек; при сравнении возраста больных ИМ с ХБП и не имевших ХБП получены статистически значимые различия (р < 0,001). Обращает внимание уменьшение доли мужчин по мере снижения функции почек: 89,2% – в группе с нормальной СКФ, 5,6% – у представителей 4-й группы (r = 0,990, р = 0,009).
Ухудшение функции почек было ассоциировано с увеличением частоты обнаружения артериальной гипертензии. Распространенность сахарного диабета также была выше в группах больных ИМ с ХБП по сравнению с больными ИМ с сохранной функцией почек (р < 0,05); выявлена более высокая распространенность ХСН III и IV ФК (NYHA) в группах больных ИМпST с ХБП по сравнению с больными ИМ с СКФ более 60 мл/мин/1,75 м2 (р < 0,01). По мере снижения функции почек отмечены нарастание дислипидемии, снижение гемоглобина, недостоверный рост гликемии и снижение уровня тропонинов, снижение сократительной функции сердца. Выявлена статистически значимая корреляция между степенью почечной дисфункции и тяжестью течения инфаркта миокарда, частотой развития осложнений.
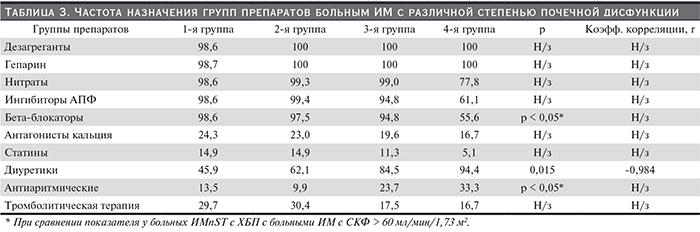
Особенности лечения больных с различной степенью почечной дисфункции представлены в табл. 3.
Больные ИМ с подъемом сегмента ST получали медикаментозную терапию в соответствии с общепринятыми рекомендациями. В то же время по мере нарастания почечной дисфункции реже назначались ингибиторы АПФ и бета-адреноблокаторы, реже проводилась тромболитическая терапия, отмечалось недостоверное уменьшение частоты назначения гепарина и нитратов; при этом больные с нарушением функции почек чаще нуждались в назначении диуретиков и антиаритмических препаратов. По-видимому, это обусловлено ростом числа пожилых больных с полиморбидной патологией и сердечной недостаточностью по мере ухудшения функции почек.
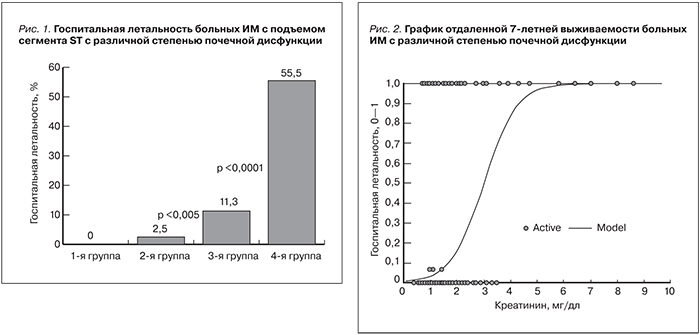
Госпитальная летальность больных ИМ с подъемом сегмента ST с различной степенью почечной дисфункции представлена на рис. 1.
Выявлена статистически значимая корреляция между степенью почечной дисфункции и частотой развития летального исхода в стационаре; наибольшая летальность наблюдалась в 4-й группе больных.
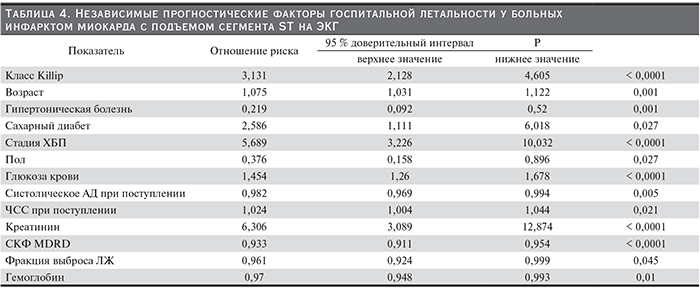
В целях определения прогностической роли почечной дисфункции с поправкой на другие факторы, а также для оценки связи различных факторов, определяемых при поступлении больных в стационар, со смертельным исходом во время пребывания в стационаре был проведен регрессионный анализ методом логистической регрессии. Показатели с низкой прогностической значимостью были исключены из дальнейших исследований. По результатам анализа определены независимые прогностические факторы смерти в стационаре (табл. 4).
Наиболее сильная связь с летальным исходом во время пребывания в стационаре выявлена среди следующих факторов: класс тяжести ИМ Killip, возраст, гипертоническая болезнь, уровень креатинина и глюкозы, а также показатели, производные от уровня креатинина: СКФ и стадия ХБП. Таким образом, дисфункция почек сохраняет свое определяющее прогностическое значение с поправкой на другие не менее важные прогностические факторы.
С целью выявления пограничного уровня креатинина, превышение которого ассоциируется с ростом госпитальной летальности, проведен регрессионный анализ методом логистической регрессии.
Зависимость, связывающая вероятность летального исхода с уровнем креатинина (мг/дл), показана на графике логистической кривой (рис. 2).
При построении модели, характеризующей вероятность летального исхода в стационаре у больных ИМ с различным уровнем креатинина, выявлено резкое увеличение риска госпитальной летальности при уровне креатинина выше 1,5 мг/дл, что говорит о важной прогностической роли данного показателя в оценке риска летального исхода.
Влияние почечной дисфункции на отдаленную выживаемость больных ИМ с подъемом сегмента ST оценивалась на протяжении 7 лет после перенесенного инфаркта миокарда с использованием метода Каплана–Майера. Общее число летальных исходов в группах больных с различной степенью почечной дисфункции за 7 лет после ИМ представлено в табл. 5.
Смертность больных в отдаленный период также была напрямую связана со степенью снижения функции почек. Если в 1-й и 2-й группах 7-летняя выживаемость составила ¾ от числа больных ИМ, то в группе 3 через 7 лет остались в живых только половина больных, а в 4-й группе – лишь 5 %. Различия между показателями отдаленной смертности больных ИМ с ХБП и без ХБП статистически значимы (р < 0,0001).

Средняя продолжительноть жизни больных ИМ с подъемом сегмента ST с различной степенью почечной дисфункции представлена в табл. 6.
Продолжительность жизни больных 1-й и 2-й групп после ИМ существенно не различалась, но прогрессивно снижалась при нарастании степени почечной дисфункции (r = 0,975, р = 0,025).
График отдаленной 7-летней выживаемости больных ИМ с различной степенью почечной дисфункции показан на рис. 3.
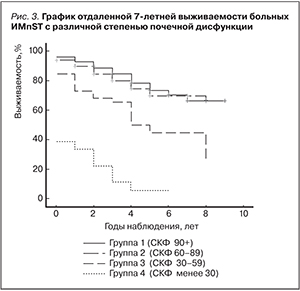 Выявлено значительное снижение отдаленной выживаемости больных ИМ с СКФ 30–59 мл/мин/1,73 м2 и еще более резкое снижение показателя – при СКФ менее 30 мл/мин/1,73 м2. Этот факт наглядно демонстрирует важную прогностическую роль почечной дисфункции при определении отдаленного прогноза у больных инфарктом миокарда.
Выявлено значительное снижение отдаленной выживаемости больных ИМ с СКФ 30–59 мл/мин/1,73 м2 и еще более резкое снижение показателя – при СКФ менее 30 мл/мин/1,73 м2. Этот факт наглядно демонстрирует важную прогностическую роль почечной дисфункции при определении отдаленного прогноза у больных инфарктом миокарда.
Таким образом, результаты настоящего исследования демонстрируют, что нарушения фильтрационной функции почек часто встречаются среди пациентов с острым ИМ. Нарушение функции почек больных ИМ ассоциируется с более старшим возрастом, женским полом, наличием хронической сердечной недостаточности и сахарного диабета [11, 14]. Нами продемонстрирована прямая корреляция между степенью снижения почечной функции у больных ИМ, распространенностью артериальной гипертензии и постинфарктного кардиосклероза, нарушением липидного и углеводного обменов, нарастанием анемии и систолической дисфункции, выявлены особенности медикаментозной терапии больных ИМ с подъемом сегмента ST с нарушением функции почек в реальной клинической практике.
Таким образом, наличие прямой ассоциации между степенью почечной дисфункции, госпитальной и отдаленной летальностью при ИМ свидетельствует о существенном значении дисфункции почек как самостоятельного предиктора неблагоприятного прогноза для больных ОКС. Оценка сывороточной концентрации креатинина у больных ОКС обязательно должна дополняться расчетом СКФ, значение которой может рассматриваться в качестве самостоятельного прогностического маркера. Повсеместное внедрение метода расчета СКФ у больных ОКС в повседневной лечебной практике позволит адекватно своевременно выявить даже умеренное нарушение фильтрационной функции почек и внести коррекцию в терапию пациента, тем самым позволив снизить число неблагоприятных исходов. Грамотная интерпретация величины СКФ приобретает, таким образом, особое значение для больных ОКС.



