Введение
Хроническая болезнь почек (ХБП) является одной из ведущих причин утраты трудоспособности и преждевременной смерти. Настоящая исследовательская работа посвящена анализу преемственности факторов риска развития, раннего выявления и клинико-функциональных особенностей ХБП у пациентов с хронической обструктивной болезнью легких (ХОБЛ) в условиях низкогорья, решению проблемы раннего выявления клинико-функциональных особенностей у пациентов, имеющих диагноз ХОБЛ, наличие признаков ХБП, а также своевременного направления к нефрологу. Это дает возможность начать более ранние комплексные меры, которые включат повышение осведомленности врачей различных специальностей о роли ХБП. Проведение поэтапного периодического скрининга ХБП у пациентов с ХОБЛ в группах высокого риска обеспечивает их преемственность на более ранних этапах лечебно-профилактических мероприятий за счет своевременного направления к нефрологу на основании принятых критериев.
Расширение нефрологической службы, в первую очередь амбулаторной, а также стационарной во всех регионах Кыргызской Республики (КР), раннее выявление ренального повреждения у пациентов с ХОБЛ, в дальнейшем правильная терапия, а также своевременное направление к нефрологу обеспечат лучший прогноз лечения пациентов и улучшат качество жизни пациентов данной когорты.
ХОБЛ – заболевание, частота которого неуклонно имеет тенденцию к росту и, по прогнозам Всемирной организации здравоохранения (ВОЗ), в 1990–2020 гг. ХОБЛ по смертности может переместиться с 6-го на 2-е место, по заболеваемости – с 12-го места на 5-е [1]. Крупные эпидемиологические исследования показывают, что ХОБЛ имеет высокую и более выраженную тенденцию к системным проявлениям, увеличивая риск развития сердечно-сосудистых заболеваний в 2, а то и в 3 раза [2]. В КР число лиц, страдающих ХОБЛ, по данным ВОЗ, составляет около 200 тыс., но, как думают эксперты, оно может быть больше в 3 и даже в 4 раза. Данная ситуация вполне может быть связана с тем, что многие не придают должного и более пристального внимания появлению симптомов на ранних этапах развития патологического процесса. Таким образом, происходит обращение к специалистам на более поздних проявлениях заболевания, что в свою очередь обусловливает тот факт, что во многих случаях процесс становится запущенным и приводит к тому, что в процесс начинают вовлекаться другие системы организма.
Проблема ренальной патологии во всем мире в настоящее время является весьма острой и достаточно актуальной, что в определенной мере говорит о пандемии ХБП [3]. По статистическим данным ВОЗ, ежегодно в мире от заболеваний мочеполовой системы умирают около 830 тыс. человек. Болезни ренальной системы занимают 14-е место как причина летальных исходов и 17-е место как причина, приводящая к потере трудоспособности в развивающихся странах [4].
Изучая результаты различных скрининговых обследований, проведенных в таких странах, как Соединенные Штаты Америки [3], Норвегия [5], Австралия [6], а также в ряде других стран, было установлено, что хронические патологические процессы со стороны ренальной системы выявляются более чем у 10% всего населения. Столь высокая распространенность обусловлена рядом факторов, прежде всего вовлечением почек в патологический процесс при широком спектре заболеваний со стороны внутренних органов, в частности сахарного диабета (СД), артериальной гипертензии (АГ), атеросклероза, а также обусловлено таким фактором, как старение населения. Так, частота выявления патологии почек имеет тенденцию существенного увеличения с возрастом.
Также стоит отметить, что почки могут поражаться при нерациональном использовании ряда широко применяемых лекарственных средств: нестероидных противовоспалительных средств, антибиотиков группы аминогликозидов, противовирусных, радиоконтрастных препаратов и др. [7]. ХБП является нозологическим понятием, которое может быть применимо к любой патологии почек. При этом патологический процесс со стороны ренальной системы наблюдается в течение 3 месяцев и более и проявляется изменениями в анализах мочи и/или крови либо нарушениями структуры и/или функции почек. Введение термина ХБП и ее классификации обусловлено рядом соображений, среди которых первостепенную роль играют данные о тесной связи стадии болезни с риском определенных, в т.ч. сердечно-сосудистых, осложнений, а также определяется степенью гомеостатических и метаболических нарушений, что в свою очередь определяет прогноз и тактику ведения больного на определенных этапах патологического процесса.
Раннее выявление ХБП и своевременное обращение к специалисту-нефрологу рассматриваются в современной литературе как один из факторов, который обеспечивает лучшую выживаемость пациентов [8, 9]. В то же время имеются доказательства того, что позднее поступление под наблюдение специалиста, в данном случае нефролога, существенно увеличивает риск летального исхода, продолжительность госпитализации больных и стоимость лечения. В свою очередь это приводит к низкому качеству жизни и плохим лабораторным показателям к началу заместительной почечной терапии [10, 11].
Раннее и своевременное выявление ХБП у пациентов с ХОБЛ дает возможность проводить пpофилактику либо коppекцию наpушений фосфоpно-кальциевого обмена, анемии, метаболических нарушений, свойственных хронической почечной патологии. Однако еще более важно то, что раннее выявление ХБП позволяет назначать нефропротективную терапию, которая приводит к замедлению прогрессирования почечной дисфункции. Следовательно, за счет этого возможно не только добиться отсрочки начала диализа, но и значительной части пациентов избежать развития терминальной почечной недостаточности и связанных с ней осложнений. Был проведен анализ как в общей группе пациентов с учетом степени их тяжести, так и в группе контроля.
Изучая различные источники факторов риска в развитии почечной дисфункции у лиц, страдающих ХОБЛ, мы нашли работы, в которых отображены факторы риска развития ХБП именно у пациентов с ХОБЛ, такие как возраст, курение, повышенный индекс массы тела (ИМТ) и др. Как известно, эти факторы риска могут усугублять прогноз заболевания и приводить к ухудшению прогноза заболевания в будущем [12–14].
Из немногочисленных международных исследований стало известно, что более ранним маркером ренального повреждения, а именно фильтрационного барьера клубочков, является умеренно увеличенная альбуминурия (УУА). Данный показатель УУА у пациентов, которые страдают АГ, СД, имеет тесную взаимную параллель с сердечно-сосудистыми факторами риска, что приводит к повышению риска развития и увеличению частоты коронарной болезни сердца, что в дальнейшем значительно ухудшает прогноз заболевания [15].
Имеются данные исследований, которые непосредственно описывают и подчеркивают непрерывную связь между кардиоваскулярной и несердечно-сосудистой смертностью, с одной стороны, и УУА, с другой [16–20]. Имеются лишь единичные исследования УУА и ее значимости при патологии со стороны респираторной системы, в частности при ХОБЛ. Данные исследований, проведенных E. Vulcun et al. [21], сообщают об УУА и ее большей частоте встречаемости среди больных ХОБЛ, а также отмечают ее тесную линейную связь со степенью насыщения гемоглобина кислородом.
Заведомо сходные данные отмечают C. Casanova et al. [22]. Авторы данных исследований подчеркивают тот факт, что особенностями, отвечающими за взаимосвязь УУА со степенью гипоксии при различной степени тяжести ХОБЛ и ее дальнейшие значения в сфере прогноза при данной нозологии, в настоящее время не полностью выясненные, а также в полном объеме изученные.
Данная исследовательская работа предполагает более детальное изучение определения факторов риска развития ХБП у пациентов с ХОБЛ в условиях низкогорья, определение частоты и величины УУА у пациентов с ХОБЛ в условиях низкогорья, а также изучение функционального аспекта состояния ренальной системы у больных ХОБЛ в зависимости от степени их тяжести.
Материал и методы
В исследовании приняли участие 82 пациента (38 мужчин и 44 женщины). Исследование проводилось в условиях низкогорья (Токмок, КР), расположенного в 762 м над уровнем моря.
Исследуемые пациенты имели ХОБЛ различной степени тяжести. Средний возраст больных составил 60,53±15,48 года.
Постановку диагноза ХОБЛ и оценку степени тяжести проводили в соответствии с критериями Global Initiative for Chronic Obstructive Lung Disease (GOLD, 2011). Степень тяжести и ее оценку устанавливали одновременно с определением клинических симптомов, характерных для каждой из них соответственно (кашель, одышка в покое и после физической активности, наличие мокроты).
В проведенной работе был изучен и проанализирован такой неотъемлемый показатель, как функция внешнего дыхания (ФВД). В данный параметр входят такие показатели, как объем форсированного выдоха за 1-ю секунду (ОФВ1), индекс Тиффно, объем форсированного выдоха за 1-ю секунду/форсированная жизненная емкость легких (ОФВ1/ФЖЕЛ, %), моментная объемная скорость выдоха при 25%, 50, 75% л/с (МОС25, МОС50, МОС75 л/с).
Таким образом, все больные были разделены на три группы после выявления у них степени тяжести ХОБЛ. Первую группу составили 27 больных ХОБЛ легкой степени тяжести. Во вторую группу включили 32 пациента со средней степенью тяжести ХОБЛ, в третью группу вошли 23 пациента с тяжелым течением бронхообструктивного синдрома. Обследованные пациенты, вошедшие в данные группы, были сопоставимыми между собой по полу и возрасту. Контрольная группа (КГ) состояла из 10 здоровых лиц, они также были сопоставимыми по полу и возрасту с группой испытуемых пациентов.
С учетом факторов риска развития ХБП определяли такие параметры, как возраст пациентов, индекс массы тела (ИМТ), рассчитанный по определенной формуле, индекс курящего человека (ИКЧ) – основной показатель, используемый для расчета частоты табакокурения, а также анамнестические данные касательно массы тела при рождении.
Для выявления характера раннего повреждения со стороны ренальной системы проводили анализ с помощью Альбу-теста microalbuphan (Erbalachema), где определяли параметры УУА.
Функциональную оценку ренальной системы осуществляли при помощи расчета скорости клубочковой фильтрации (рСКФ). Одновременно проводили анализы на выявление белка в моче, лейкоцитов, эритроцитов, а также креатинина сыворотки крови и концентрации общего белка. Кроме того, учитывались данные анамнеза, которые включали данные, характерные для почечной патологии, такие как изменение цвета мочи, преобладание ночного диуреза над дневным, учащенное мочеиспускание или, наоборот, уменьшение количества диуреза,
При помощи программ Statistica 6.0. и SPSS Statistics проводилась обработка полученных статистических данных. Данные обработки представлены в виде средней величины±стандартное отклонение. Также учитывались критерии Шапиро–Уилка и Лильефорса, с помощью которых определяли значимую нормальность распределения. Достоверность в сфере различий данных между группами выясняли с помощью непараметрического критерия Манна–Уитни и параметрического t-критерия Стьюдента. Использовали критерии Крускала–Уолиса при множественных сравнениях. Проводили дисперсионный анализ с вычислением коэффициента F и последующим post-hoc-анализом; достоверными считались различия при p<0,05.
Результаты исследования
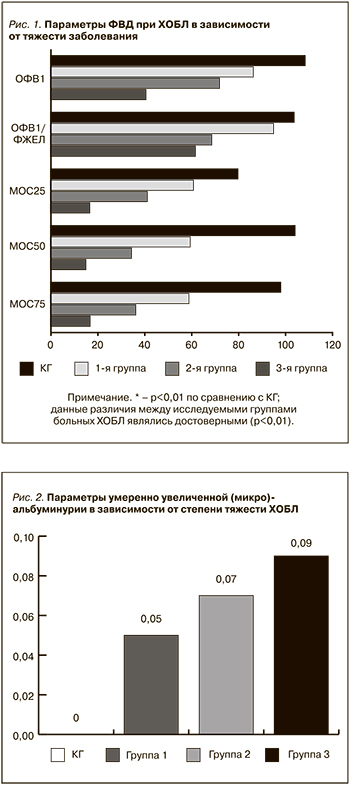 Результаты анализируемых групп больных по ФВД, представлены на рис. 1.
Результаты анализируемых групп больных по ФВД, представлены на рис. 1.
Ожидаемые результаты подтвердились, их значения в исследовании бронхиальной проходимости у пациентов с хроническим обструктивным синдромом оказались значительно снижены по сравнению с группой здоровых лиц (p<0,01) (рис.1). По мере дальнейшего прогрессирования патологического процесса отмечалось закономерное ухудшение вентиляционных индексов (p<0,01).
Также был проведен корреляционный анализ факторов риска ХБП у пациентов с ХОБЛ в условиях низкогорья как в общей группе пациентов с учетом степени их тяжести, так и в КГ. На основании полученных результатов можно сделать вывод, согласно которому у жителей низкогорья, в частности Токмока, фактором риска развития ХБП у пациентов с ХОБЛ оказался возраст (данный признак занял первое место в развитии почечной дисфункции). Так, в первой группе с легким течением ХОБЛ средний возраст составил 53,04±2,523 года, у пациентов со среднетяжелым течением хронического обструктивного синдрома средний возраст составил 60,53±2,737 года, у пациентов с тяжелым течением ХОБЛ средний возраст составил 62,00±1,693 года. Данные представлены в таблице.
Таким образом, уровень УУА у больных 2-й группы составил 0,07±0,04 г/л, что имело тенденцию к подъему по сравнению с таковым у пациентов с легким течением хронического обструктивного синдрома (0,05±0,03 г/л; р>0,05). Также выявлено, что у пациентов с тяжелым течением ХОБЛ регистрировались более высокие показатели УАА, которые отмечались на уровне 0,09±0,03 г/л и были аналогичными среди больных как 1-й (р<0,001), так и 2-й групп (р<0,05) соответственно (рис. 2).
Больные, страдавшие хроническим обструктивным синдромом, по сравнению с пациентами КГ имели более низкие показатели фильтрационной функции, что выражалось в уменьшении рСКФ и параллельном росте концентрации креатинина в сыворотке крови. Значительное прогрессивное ухудшение ренальной функции выявлялось по мере утяжеления бронхообструктивного синдрома.
В исследовании получены следующие динамические показатели рСКФ: при легком течении ХОБЛ они составили 98,0±11,3 мл/мин/1,73 м², при среднетяжелом – 68,8±7,4 и при тяжелом течение были зафиксированы на уровне 64,5±5,5 мл/мин/1,73 м² соответственно (p<0,01). Данные по содержанию креатинина сыворотки крови (p<0,01) представлены в динамике на рис. 3.
В проведенном исследовании прослеживается неуклонное нарастание степени повреждения почечного фильтра. Увеличение количества белка в моче сопутствует прогрессированию бронхообструктивного синдрома (0,39±0,09 г/л, 0,74±0,28 и 2,02±0,60 г/л на 1–3-й стадиях ХОБЛ соответственно; p<0,01 между группами и p<0,001 по сравнению с КГ). Также одномоментно прослеживали параллельное снижение концентрации общего белка сыворотки крови пациентов с ХОБЛ (p<0,01) (рис. 3).
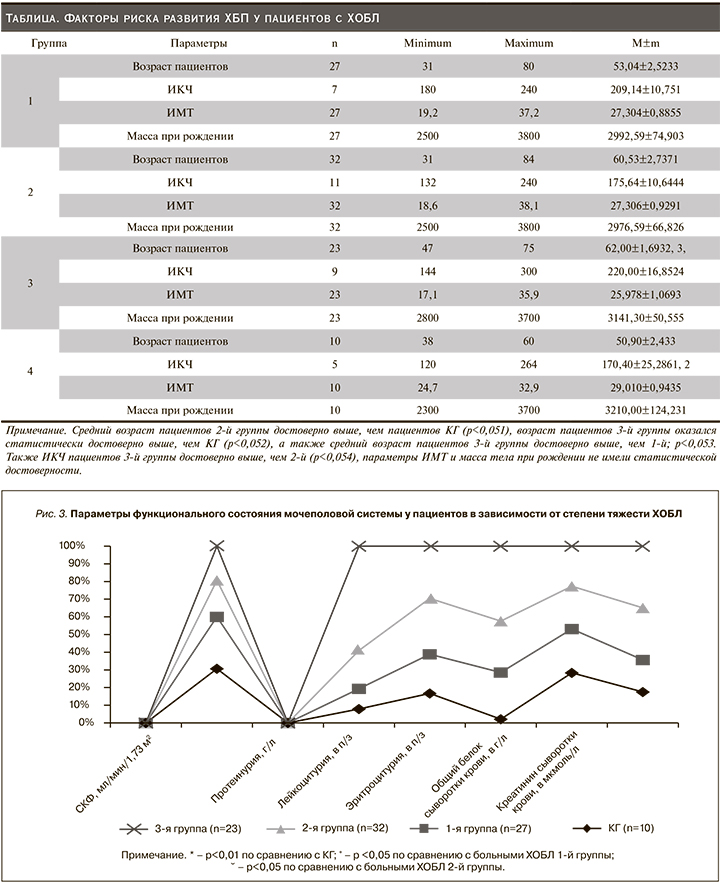
Продемонстрировано увеличение числа лейкоцитов и эритроцитов у исследуемых пациентов с ХОБЛ (p<0,01). Более высокие показатели в мочевом осадке зарегистрированы у пациентов с тяжелым течением патологического процесса (рис. 3).
Заключение
В исследованиях, посвященных проблеме ХОБЛ с системными проявлениями, показано, что у данных пациентов отчетливо прослеживаются изменения функционального характера со стороны ренальной системы, а также имеются такие факторы риска развития ХБП, как возраст и табакокурение. Более актуальным представляется, на наш взгляд, факт обнаружения прямой ассоциации степени УУА с эволюцией ХОБЛ. Это в будущем позволит рассматривать ее в качестве маркера тяжести течения заболевания.
Выявлено прогрессивное нарастание УУА в условиях низкогорья (Токмок) по мере утяжеления течения ХОБЛ, что в свою очередь совпадает с данными ряда публикаций, посвященных линейной взаимосвязи степени гипоксемии при данном заболевании с нарушением фильтрационного барьера клубочков [21–23]. Данное положение согласуется с полученными ранее результатами, которые непосредственно подчеркивают линейное снижение фильтрационной способности почек по мере нарастания тяжести хронического обструктивного синдрома в условиях низкогорья (Токмок) [24].
Обнаруженные на ранних этапах факторы риска развития ХБП, а также признаки патологии ренальной системы у больных ХОБЛ требуют проведения дополнительного обследования, что послужит в будущем профилактике и дальнейшей корректной медикаментозной нефропротективной терапии на более ранних этапах.
Выводы
1. Выявление на ранних этапах статистически достоверных факторов развития ХБП, таких как пожилой возраст, курение пациентов с ХОБЛ, имеет большое значение в развитии возможных последствий со стороны других органов и систем.
2. Умеренно увеличенная альбуминурия является наиболее ранним маркером проявления почечного повреждения при ХОБЛ, отмечается у пациентов с легким течением, а далее имеет тенденцию к нарастанию по мере прогрессирования ХОБЛ.
3. Более существенные и значимые изменения показателей ренальной функции наблюдаются у пациентов с ХОБЛ в условиях низкогорья и коррелируют со степенью бронхиальной обструкции.



